
【题目】探究氢氧化铝的两性,最适宜的试剂是( )
A.AlCl3、氨水、稀盐酸B.![]() 、氨水、稀盐酸
、氨水、稀盐酸
C.Al、NaOH溶液、稀盐酸D.![]() 溶液、NaOH溶液、稀盐酸
溶液、NaOH溶液、稀盐酸
【答案】D
【解析】
既能与酸反应,又能与强碱反应的氢氧化物属于两性氢氧化物,但氢氧化铝只能溶于碱中的强碱,据此分析。
A、由于氢氧化铝只能溶于碱中的强碱,故探究氢氧化铝的两性,不能用氨水,选项A错误;
B、由于氢氧化铝只能溶于碱中的强碱,故探究氢氧化铝的两性,不能用氨水,选项B错误;
C、Al与NaOH溶液反应生成偏铝酸钠和氢气,偏铝酸钠溶液中滴加少量盐酸产生氢氧化铝沉淀,氢氧化铝沉淀会溶于过量的盐酸,操作步骤较多,不是最适宜的试剂,选项C错误;
D、Al2(SO4)3溶液和少量NaOH溶液反应生成氢氧化铝沉淀,继续滴加氢氧化钠溶液沉淀溶解,向氢氧化铝沉淀加稀盐酸沉淀也溶解,说明氢氧化铝具有两性,选项D正确。
答案选D。


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:
【题目】著名化学家徐光宪在稀土领域贡献突出,被誉为“稀土界的袁隆平”。钇是稀土元素之一,我国蕴藏着丰富的钇矿石(Y2FeBe2Si2O10),工业上通过如下工艺流程制取氧化钇,并获得副产物铍。
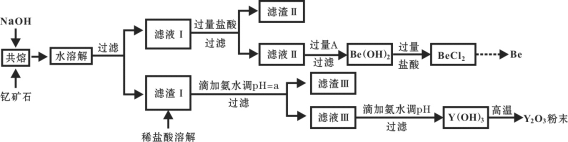
已知:ⅰ.钇(Y)的常见化合价为+3价;
ⅱ.铍和铝处于元素周期表的对角线位置,化学性质相似;
ⅲ.Fe3+、Y3+形成氢氧化物沉淀时的pH如下表:
离子 | 开始沉淀时的pH | 完全沉淀时的pH |
Fe3+ | 2.1 | 3.1 |
Y3+ | 6.0 | 8.3 |
(1)将钇矿石与NaOH共熔的反应方程式补充完整:
__Y2FeBe2Si2O10+__NaOH+____ ![]() __Y(OH)3 +__Fe2O3 + __Na2SiO3 + __Na2BeO2 + __H2O
__Y(OH)3 +__Fe2O3 + __Na2SiO3 + __Na2BeO2 + __H2O
(2)滤渣Ⅱ的主要成分是____________。
(3)试剂A可以是___________。
A.NaOH溶液 B.氨水 C.CO2 D.CaO
(4)用氨水调节pH=a时,a的取值范围是_____________________。
(5)计算常温下Y3+ +3H2O![]() Y(OH)3+3H+的平衡常数K=________。(常温下Ksp [Y(OH)3] = 8.0×10-23)
Y(OH)3+3H+的平衡常数K=________。(常温下Ksp [Y(OH)3] = 8.0×10-23)
(6)滤液Ⅲ加入氨水产生沉淀的离子方程式为_______________。
(7)从BeCl2溶液中得到BeCl2固体的操作是________。
(8)常见的由BeCl2固体生产Be的工业方法有两种:①电解法:电解NaCl-BeCl2混合熔融盐制备Be;②热还原法:熔融条件下,钾还原BeCl2制备Be。以上两种方法你认为哪种更好并请说明理由_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W为短周期主族元素,在周期表中的相对位置如图,下列说法正确的是( )

A. 若HmXOn为强酸,则X的氢化物溶于水一定显酸性(m、n均为正整数)
B. 若四种元素均为金属,则Z的最高价氧化物对应的水化物一定为强碱
C. 若四种元素均为非金属,则W的最高价氧化物对应的水化物一定为强酸
D. 若四种元素中只有一种为金属,则Z与Y两者的最高价氧化物对应的水化物能反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浩瀚的大海蕴藏着丰富的化学资源,从海水中提取物质,已日益受到人们的重视。
(1)从海水提取溴,一般要经过______、氧化和_______三个步骤。常用的氧化剂是氯气,反应的离子方程式为___________________________。
(2)从海带中提取碘,除试管、烧杯、漏斗、玻璃棒、带铁圈的铁架台、酒精灯、坩埚、泥三角、坩埚钳、托盘天平,还缺少的玻璃仪器有_______________________________________。
(3)将灼烧后的海带灰溶解、过滤,为检验滤液中有I-,取1mL滤液,先加_______,再滴加_____________,并不断振荡,观察到溶液变蓝。提取碘水中的碘,可选用的萃取剂有________________。(选填编号)
a. 裂化汽油 b. 甲苯 c. 酒精 d. 四氯化碳
(4)为了预防碘缺乏病,国家规定食盐中应含有一定量的碘酸钾。利用下列原理可测定食盐中的含碘量(质量分数):IO3-+5I-+6H+→3I2+3H2O,I2+2S2O32-→2I-+S4O62-。称ag食盐样品,配成250mL溶液,取出25.00mL。加入过量的硫酸酸化KI,若滴定消耗bmol/L的硫代硫酸钠溶液vmL,则该食盐中的含碘量为______(写出表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于工业合成氨反应N2+3H22NH3+Q(Q>0),下列判断正确的是( )
A.3体积![]() 和足量
和足量![]() 反应,必定生成2体积
反应,必定生成2体积![]()
B.使用合适的催化剂,可以提高提高原料的利用率
C.![]() 左右比室温更有利于向合成氨的方向进行
左右比室温更有利于向合成氨的方向进行
D.及时使氨液化、分离的主要目的是提高![]() 和
和![]() 的利用率
的利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列四种溶液:①c(H+)=10-3mol·L-1的醋酸 ②0.01mol·L-1的盐酸 ③0.1mol·L-1的NaOH溶液 ④c(OH-)=1mol·L-1氨水溶液。由水电离出的氢离子浓度之比为
A. 1000∶100∶10∶1 B. 11∶12∶1∶0
C. 11∶12∶13∶14 D. 3∶2∶13∶14
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液的电导率越大,导电能力越强。用0.100 mol·L-1的NaOH溶液滴定10.00 mL浓度均为0.100 mol·L-1 的盐酸和CH3COOH溶液。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是

A. 曲线②代表滴定CH3COOH溶液的曲线
B. A点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.5 mol·L-1
C. 在相同温度下,A、B、C三点溶液中水的电离程度:B<A<C
D. D点溶液中:c(Cl-)=2c(OH-)-2c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是 ( )
A. 含有AgCl和AgI固体的悬浊液:c(Ag+)>c(C1-)=c(I-)
B. 在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大
C. AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同
D. CaCO3 难溶于稀硫酸,但可溶于醋酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. 醋酸溶解水垢中的CaCO3: CaCO3 + 2H+= Ca2++ H2O + CO2↑
B. 惰性电极电解饱和MgCl2溶液: Mg2++2Cl- + 2H2O ![]() Mg(OH)2↓ + H2↑ + Cl2↑
Mg(OH)2↓ + H2↑ + Cl2↑
C. 苯酚钠溶液中通入少量的CO2:![]() +H2O+CO2→
+H2O+CO2→ +
+![]()
D. 用银氨溶液检验乙醛中的醛基:CH3CHO+![]() +2OH-
+2OH-![]() CH3COONH4+H2O+2Ag↓+3NH3↑
CH3COONH4+H2O+2Ag↓+3NH3↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com