
【题目】常温下,下列四种溶液:①c(H+)=10-3mol·L-1的醋酸 ②0.01mol·L-1的盐酸 ③0.1mol·L-1的NaOH溶液 ④c(OH-)=1mol·L-1氨水溶液。由水电离出的氢离子浓度之比为
A. 1000∶100∶10∶1 B. 11∶12∶1∶0
C. 11∶12∶13∶14 D. 3∶2∶13∶14
【答案】A
【解析】
根据溶液中水的离子积Kw=c(H+)×c(OH),其中c(H+)是溶液中所有的氢离子的浓度,c(OH)是溶液中所有的氢氧离子的浓度,且在任何溶液中,由水电离的氢离子与氢氧根离子浓度相等,酸溶液中OH-全部来自水电离,碱溶液中H+全部来自水电离,据此分析作答。
根据常温下水的离子积为1×10-14 可知:
(1)c(H+)=10-3 mol·L-1的醋酸中,由水电离出的氢氧根离子浓度c(OH) = ![]() = 1×10-11 mol/L,故由水电离的氢离子浓度等于c(OH) = 1×10-11 mol/L;
= 1×10-11 mol/L,故由水电离的氢离子浓度等于c(OH) = 1×10-11 mol/L;
(2)0.01mol·L-1的盐酸中,由水电离出的氢氧根离子浓度c(OH) = ![]() = 1×10-12 mol/L,故由水电离的氢离子浓度等于c(OH) = 1×10-12 mol/L;
= 1×10-12 mol/L,故由水电离的氢离子浓度等于c(OH) = 1×10-12 mol/L;
(3)0.1mol·L-1的NaOH溶液中,由水电离出的氢离子浓度为:![]() = 1×10-13 mol/L;
= 1×10-13 mol/L;
(4)c(OH-)=1 mol·L-1氨水溶液中,由水电离出的氢离子浓度为:![]() =1×10-14 mol/L;
=1×10-14 mol/L;
则四种溶液中由水电离出的氢离子浓度之比为:1000:100:10:1,故A项正确;
答案选A。


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】将1molN2气体和3molH2气体在2L的恒容容器中,并在一定条件下发生如下反应:N2(g)+3H2(g) ![]() 2NH3(g),若经2s后测得NH3的浓度为0.6mol·L-1,现有下列几种说法:其中不正确的是
2NH3(g),若经2s后测得NH3的浓度为0.6mol·L-1,现有下列几种说法:其中不正确的是
A. 用N2表示的反应速率为0.15mol·L-1·s-1 B. 2s时H2的转化率为40%
C. 2s时N2与H2的转化率相等 D. 2s时H2的浓度为0.6mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F是一种关节炎止痛药,合成F的一种传统法的路线如下:
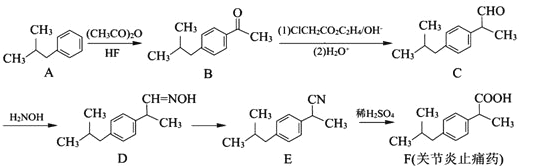
(1)B中含氧官能团的名称为_________。
(2)C→D的反应可分为两步,其反应类型为_________、_________。
(3)写出比F少5个碳原子的同系物X的结构简式:_______________(写一种);X有多种同分异构体,满足下列条件的X的同分异构体共有_______________种。
①属于芳香族化合物;②苯环上只有1个取代基;③属于酯类物质;
(4)写出E转化为F和无机盐的化学方程式:______________________。
(5)已知:①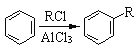
② 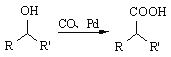 (R1、R2表示烃基)
(R1、R2表示烃基)
合成F的一种改良法是以2—甲基—1—丙醇[(CH3)2CHCH2OH)]、苯、乙酸酐[(CH3CO)2O]为原料来合成,写出有关的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:H2C=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH__________________
CH3CH2OH__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有甲、乙、丙、丁四个装置,下列说法不正确的是
A. 装置甲可作为制取NO2的发生装置
装置甲可作为制取NO2的发生装置
B. 装置乙可作为制取NO的收集装置
装置乙可作为制取NO的收集装置
C.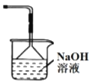 装置丙可作为制取Cl2的尾气吸收装置
装置丙可作为制取Cl2的尾气吸收装置
D. 装置丁可用于除去NH3中H2O
装置丁可用于除去NH3中H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究氢氧化铝的两性,最适宜的试剂是( )
A.AlCl3、氨水、稀盐酸B.![]() 、氨水、稀盐酸
、氨水、稀盐酸
C.Al、NaOH溶液、稀盐酸D.![]() 溶液、NaOH溶液、稀盐酸
溶液、NaOH溶液、稀盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是同学们熟悉的物质:
①O2 ②H2O2 ③MgCl2 ④H2SO4 ⑤Na2CO3⑥NH4Cl ⑦CO2 ⑧Ne ⑨Na2O2 ⑩NaOH
(1)这些物质中,属于共价化合物的是__(填序号,下同);只含有离子键的是__;不含化学键的是__。
(2)写出下列物质的结构式:
①O2__;②H2O2__;⑦CO2__。
(3)写出下列物质的电子式
⑥NH4Cl__;⑩NaOH__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸晶体的组成可表示为H2C2O4·xH2O,为了测定x值,进行下述实验:
①称取n g草酸晶体配成100.00 mL水溶液;
②取25.00 mL所配制的草酸溶液置于锥形瓶中,加稀硫酸,用浓度为a mol·L-1的KMnO4溶液滴定,已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O
试回答下列问题:
(1)实验中不考虑铁架台等夹持仪器外,需要的仪器有(填序号)___________,还缺少的仪器有(填名称)____________。
A.托盘天平(带砝码,镊子) B.滴定管 C. 100mL容量瓶 D.烧杯E.漏斗 F.锥形瓶 G.玻璃棒 H.烧瓶
(2)实验中KMnO4溶液应装在____式滴定管中,滴定终点的判断依据是_________________
(3)若在滴定前没有用amol·L-1的KMnO4溶液对滴定管进行润洗,则所测得的x值会___________(偏大、偏小、无影响)。
(4)若滴定终点读数时目光仰视,则计算出的x值可能_______________(填偏大、偏小、无影响)。
(5)滴定过程中用去V mL a mol·L-1的KMnO4溶液,则所配制的草酸的物质的量浓度为_______mol·L-1 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.化合物 Mg5Al3(OH)19(H2O)4 可作环保型阻燃材料,受热时按如下化学方程式分解:2Mg5Al3(OH)19(H2O)4![]() 27H2O↑+10MgO+3Al2O3
27H2O↑+10MgO+3Al2O3
(1)写出该化合物作阻燃剂的两条依据___________。
(2)用离子方程式表示除去固体产物中 Al2O3 的原理___________
(3)已知 MgO可溶于NH4Cl的水溶液,用化学方程式表示其原理_____________。
Ⅱ.磁性材料 A(M=296g/mol)是由两种元素组成的化合物,某研究小组按如图流程探 究其组成:

请回答:
(4)A的化学式为_____。C 中呈黄色的离子对应元素在元素周期表中的位置为__________。
(5)已知化合物 A 能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下,该气体对氨气的相对密度为2),该气体分子的电子式为_____。写出该反应的离子方程式_________。
(6)写出F→G反应的化学方程式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是
A.达到化学平衡时,4v正(O2)=5v逆(NO)
B.若单位时间内生成n mol NO的同时,消耗n mol NH3,则反应达到平衡状态
C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.化学反应速率关系是:2v正(NH3)=3v逆(H2O)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com