
【题目】2一氨-3—氯苯甲酸是白色晶体,其制备流程如下:
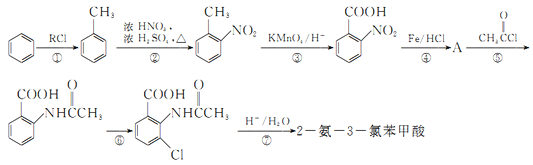
已知:
回答下列相关问题
(1)![]() 的名称是__________,2-氨-3-氯苯甲酸中含N官能团的电子式为__________。
的名称是__________,2-氨-3-氯苯甲酸中含N官能团的电子式为__________。
(2)反应①中R代表的是_____________,反应②的反应类型为_____________。
(3)如果反应③中KMnO4的还原产物为MnSO4,请写出该反应的化学方程式_____________。
(4)A的结构简式为_____________,⑥的反应条件为_____________。
(5)符合下列条件的同分异构体的结构简式为_____________。
a.式量比![]() 大42的苯的同系物;
大42的苯的同系物;
b.与酸性KMnO4反应能生成二元羧酸
c.仅有3种等效氢
(6)事实证明上述流程的目标产物的产率很低;据此,研究人员提出将步骤⑥设计为以下三步,产率有了一定提高。
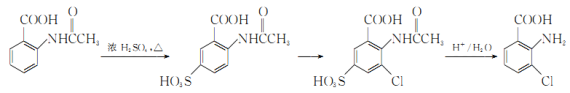
分析产率提高的原因是_____________。
【答案】甲苯 ![]() —CH3 取代反应
—CH3 取代反应 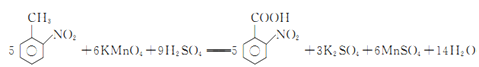
 Fe和Cl2
Fe和Cl2 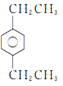 占位,减少5号位上H原子的取代
占位,减少5号位上H原子的取代
【解析】
由制备流程可知,苯与CH3Cl发生信息反应②生成甲苯,甲苯与浓硫酸和浓硝酸在加热条件下发生硝化反应生成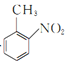 ,
, 发生氧化反应生成
发生氧化反应生成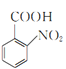 ,
, 与铁、盐酸发生还原反应生成A,则A为
与铁、盐酸发生还原反应生成A,则A为 ,
, 发生信息1反应生成
发生信息1反应生成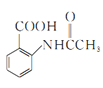 ,
, 在铁作催化剂的条件下,与氯气发生取代反应生成
在铁作催化剂的条件下,与氯气发生取代反应生成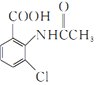 ,
, 在酸性条件下水解生成2一氨-3—氯苯甲酸。
在酸性条件下水解生成2一氨-3—氯苯甲酸。
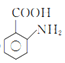
(1)![]() 的名称是甲苯;2-氨-3-氯苯甲酸的结构简式是
的名称是甲苯;2-氨-3-氯苯甲酸的结构简式是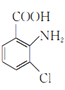 ,其含氮官能团为氨基,氨基的电子式为
,其含氮官能团为氨基,氨基的电子式为![]() ,故答案为:甲苯;
,故答案为:甲苯;![]() ;
;
(2)反应①为苯与CH3Cl反应生成甲苯,则R为—CH3;反应②为甲苯与浓硫酸和浓硝酸混酸在加热条件下发生硝化反应生成 ,故答案为:—CH3;
,故答案为:—CH3; ;
;
(3)反应③中,KMnO4与![]() 发生氧化还原反应,KMnO4被还原为MnSO4,
发生氧化还原反应,KMnO4被还原为MnSO4,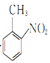 被氧化为
被氧化为![]() ,反应的化学方程式为
,反应的化学方程式为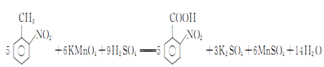 ,故答案为:
,故答案为: ;
;
(4) 与铁、盐酸发生还原反应生成A,则A为
与铁、盐酸发生还原反应生成A,则A为 ,反应⑥为
,反应⑥为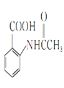 在铁作催化剂的条件下,与氯气发生取代反应生成
在铁作催化剂的条件下,与氯气发生取代反应生成 ,故答案为:
,故答案为: ;Fe和Cl2;
;Fe和Cl2;
(5)由a可知该物质比甲苯多3个—CH2—,由b可知该物质苯环上有2个取代基,其中取代基为—CH3和—CH2CH2CH3,在苯环上有邻、间、对3种同分异构体,取代基为—CH3和—CH(CH3)2,在苯环上有邻、间、对3种同分异构体,取代基为2个—CH2CH3,在苯环上有邻、间、对3种同分异构体,共9种,其中有3中等效氢的结构简式为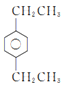 ,故答案为:
,故答案为: ;
;
(6)产率提高的原因是:占位可减少5号位上H原子的取代,减少副反应产物的生成,使得产率有了一定提高。故答案为:占位,减少5号位上H原子的取代。


 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】已知在酸性溶液中可发生如下反应: R2O72-+ 6Fe2+ + 14H+ =6Fe3+ +2Rn+ +7H2O,则Rn+中R的化合价是
A. +3 B. +4 C. +5 D. +6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2014年12月科学家发现了迄今为止最轻的冰——“冰十六”,它是水的一种结晶形式,有着像笼子一样、可以困住其他分子的结构。下列有关叙述中不正确的是
A.冰的密度比液态水小B.冰与干冰由不同分子构成
C.“冰十六”可以包合气体分子D.液态水转变成“冰十六”是化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电镀工业上,为了提高镀锌的效果,通常采用Zn(CN)42-溶液代替Zn2+溶液进行电解。请回答下列问题:
(1)元素锌在周期表中的位置为_____________,基态Zn的价电子排布式为_____________。
(2)Zn(CN) 42-所含元素中,电负性最大的元素是_____________,Zn(CN) 42-中含有的化学键类型有σ键和_____________。
(3)CN-中C的杂化类型为_____________,与CN-互为等电子体的单质为_____________。
(4)H2CO3与HNO3的酸性相差较大,请解释其原因_____________。
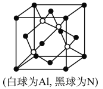
(5)N和Al可组成一种新型半导体材料AlN;AlN具有耐高温,耐磨性能。其晶体类型为_____________,其晶体结构如图,已知晶胞边长为apm,则AlN的密度为_____________(用含a、NA的代数式表示)g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二酸(![]() )又名草酸,是生物体的一种代谢产物;现设计如下实验探究草酸分解反应的产物。
)又名草酸,是生物体的一种代谢产物;现设计如下实验探究草酸分解反应的产物。
资料查阅:
Ⅰ.草酸熔点为102℃,150~160℃升华,157℃时开始分解。在人体中C2O42-容易与钙离子形成草酸钙导致肾结石。
Ⅱ.PdCl2溶液可用于检验CO,反应的化学方程式为CO+PdCl2+H2O====CO2+2HCl+Pd(黑色粉末)。
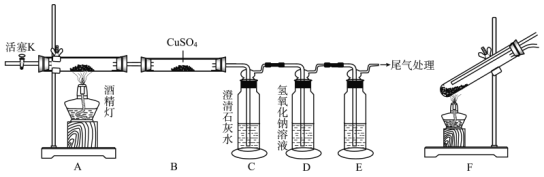
(1)A中盛放草酸的玻璃仪器的名称是_____________,实验中观察到B中CuSO4粉末变蓝,相关化学方程式为_____________。
(2)装置E中的试剂为_____________,当观察到_____________(填现象),可以证明有CO气体生成。
(3)下面是该实验过程中的相关操作,正确的操作顺序为_________(填入下列步骤的字母)。
A.向装置中通入适量N2 B.点燃酒精灯 C.检查装置气密性
D.装入相关试剂 E.再次通入N2并熄灭酒精灯
(4)为准确证眀A有CO2气体产生,需取少量C中沉淀于试管中,滴加过量盐酸并观察是否有气泡产生,其目的是_____________,草酸分解反应的化学方程式为_____________。
(5)实验过程中,学生提出装置A应改为装置F,请结合信息分析其原因是_____________;如果草酸粉末溅入眼睛里,应立即_____________,然后就医。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)选择下列某种答案的字母序号,填入下表的空格。
A.同位素 B.同系物 C.同分异构体 D.同种物质
① | ② | ③ | ④ | |
物质 |
| 16O与18O | 苯与对二甲苯 | 1—丁炔与1,3-丁二烯 |
相互关系 | _______ | _______ | _______ | _______ |
(2)按要求表达下列有机物
①乙烯的电子式:__________________;②2—甲基丙烷的结构简式:________________;
③1,2—二溴乙烷的结构简式:______________;④顺-2-戊烯的结构简式:_________;
⑤分子式为C6H12,核磁共振氢谱显示只有一组吸收峰的烯烃的结构简式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合溶液中Al2(SO4)3与MgSO4的物质的量浓度之比为( )

A. 1∶2 B. 3∶1
C. 2∶1 D. 6∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①2FeCl3+2KI=2FeCl2+2KCl+I2②2FeCl2+Cl2=2FeCl3判断下列物质的氧化能力由大到小的顺序是
A. Fe3+ > Cl2 > I2 B. Cl2 > Fe3+ > I2
C. I2 > Cl2 > Fe3+ D. Cl2 > I2 > Fe3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com