
【题目】2014年12月科学家发现了迄今为止最轻的冰——“冰十六”,它是水的一种结晶形式,有着像笼子一样、可以困住其他分子的结构。下列有关叙述中不正确的是
A.冰的密度比液态水小B.冰与干冰由不同分子构成
C.“冰十六”可以包合气体分子D.液态水转变成“冰十六”是化学变化
 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
【题目】下列过程的能量变化符合下图所示的是

A. 酸碱中和反应
B. CH4在O2中燃烧
C. NH4Cl晶体与Ba(OH)28H2O晶体混合搅拌
D. CaO溶于水生成Ca(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(8分)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中,T所处的周期序数与主族序数相等。请回答下列问题:

(1)T的原子结构示意图为________。
(2)元素的非金属性(原子的得电子能力):Q________W(填“强于”或“弱于”)。
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为__________________________。
(4)原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是__________________。
(5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2 L的甲气体与0.5 L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成R的含氧酸盐只有一种,则该含氧酸盐的化学式是________________。
(6)在298K下,Q、T的单质各1 mol完全燃烧,分别放出热量a kJ和b kJ。又知一定条件下,T的单质能将Q从它的最高价氧化物中置换出来,若此置换反应生成3 mol Q的单质,则该反应在298K下的ΔH=________(注:题中所涉单质均为最稳定单质)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组设计的实验室制取并提纯乙酸乙酯的方案如下所示
已知:①氯化钙可与乙醇形成CaCl26C2H5OH;
②有关有机物的沸点如下表所示
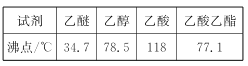
③2CH3CH2OH![]() CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
I.制备过程:装置如图所示,A中盛有浓硫酸,B中盛有9.5mL无水乙醇和6mL冰醋酸,D中盛有饱和碳酸钠溶液。
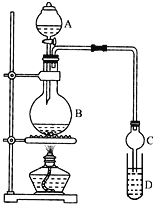
(1)实验过程中滴加大约3mL浓硫酸,B的容积最合适的是_____(填字母代号)
A. 25 mL B 50 mL C. 250 mL D. 500 mL
(2)球形干燥管的主要作用是_______________。
(3)饱和碳酸钠溶液的作用是______(填字母代号)。
A.消耗乙酸并溶解乙醇
B.碳酸钠溶液呈碱性,有利于乙酸乙酯的水解
C.加速乙酸乙酯的生成,提高其产率
D.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中的更小,有利于分层析出
II.提纯方法:
①将D中混合液进行分离。
②有机层用5mL饱和食盐水洗涤,再用5mL饱和氯化钙溶液洗涤,最后用水洗涤。有机层倒入一干燥的烧瓶中,选用合适的干燥剂干燥,得到粗产品。
③将粗产品蒸馏,收集77.1℃时的馏分,得到纯净、干燥的乙酸乙酯。
(4)第①步分离混合液时,选用的主要玻璃仪器的名称是_____________。
(5)第②步中用饱和食盐水洗去碳酸钠后,再用饱和氯化钙溶液洗涤,主要洗去粗产品中的______(填物质名称)。再加入_______(此空从下列选项中选择,四种物质均有吸水性)干燥
A.浓硫酸 B.碱石灰 C.无水硫酸钠 D.生石灰
(6)加热有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,一个可能的原因是_____________________________________________。
(7)若实验所用乙酸的质量为2.4g,乙醇的质量为2.1g,得到纯净的产品的质量为2.64g,则乙酸乙酯的产率是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实,不能用勒夏特列原理解释的是
A. 溴水中有如下平衡:Br2+H2OHBr+HBrO,加入AgNO3溶液后,溶液颜色变浅
B. 合成NH3反应,为提高NH3的产率,理论上应采取相对较低温度的措施
C. 氯气在水中的溶解度大于在饱和食盐水中的溶解度
D. 对CO(g)+NO2(g)CO2(g)+NO(g)平衡体系增大压强可使颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氯是人类研究的重要课题,目前工业合成氨的原理为:N2(g) + 3H2(g) 2NH3(g) ΔH=-93.0kJ/mol
(1)某温度下,在2 L密闭容器中发生上述反应,测得数据如下
时间/h 物质的量/mol | 0 | 1 | 2 | 3 | 4 |
N2 | 2.0 | 1.83 | 1.7 | 1.6 | 1.6 |
H2 | 6.0 | 5.49 | 5.1 | 4.8 | 4.8 |
NH3 | 0 | 0.34 | 0.6 | 0.8 | 0.8 |
①0~2 h内,v(N2)=____________。
②平衡时,H2的转化率为____;该温度下,反应2NH3(g)N2(g) + 3H2(g) 的平衡常数K=___(mol/L)2。
③若保持温度和体积不变,起始投入的N2、H2、NH3的物质的量分别为a mol、b mol、c mol,达到平衡后,NH3的浓度与上表中相同的为_______(填选项字母)。
A.a=l、b=3、c=0 B.a=4、b=12、c=0
C.a=0、b=0、c=4 D.a=l、b=3、c=2
(2)另据报道,常温、常压下,N2在掺有少量氧化铁的二氧化钛催化剂表面能与水发生反应,生成NH3和O2。已知:H2的燃烧热ΔH=-286.0kJ/mol,则用N2与水反应制NH3的热化学方程式为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶体和溶液的特征区别是( )
A. 胶体属于介稳体系 B. 胶体粒子的大小在1nm~100nm之间
C. 胶体具有丁达尔效应 D. 胶体粒子不能透过滤纸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2一氨-3—氯苯甲酸是白色晶体,其制备流程如下:
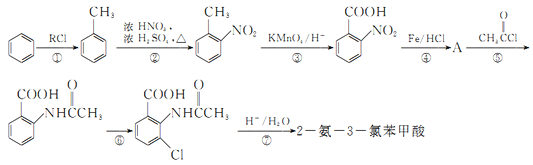
已知:
回答下列相关问题
(1)![]() 的名称是__________,2-氨-3-氯苯甲酸中含N官能团的电子式为__________。
的名称是__________,2-氨-3-氯苯甲酸中含N官能团的电子式为__________。
(2)反应①中R代表的是_____________,反应②的反应类型为_____________。
(3)如果反应③中KMnO4的还原产物为MnSO4,请写出该反应的化学方程式_____________。
(4)A的结构简式为_____________,⑥的反应条件为_____________。
(5)符合下列条件的同分异构体的结构简式为_____________。
a.式量比![]() 大42的苯的同系物;
大42的苯的同系物;
b.与酸性KMnO4反应能生成二元羧酸
c.仅有3种等效氢
(6)事实证明上述流程的目标产物的产率很低;据此,研究人员提出将步骤⑥设计为以下三步,产率有了一定提高。
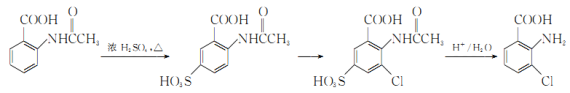
分析产率提高的原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某人设计淀粉利用方案如下图所示:其中A是乙烯能催熟水果,B是高分子化合物,D是有水果香味的物质。请回答以下问题:

(1)“C6H12O6”的名称是________,工业上由石蜡制取A的方法称作____。C中含有官能团名称是____________;
(2)A→B反应类型为_________________;C→D反应类型为_________________;
(3)写出下列转化的化学方程式
①A→B:__________________;
②C→D:___________________________;
③CH3CH2OH→CH3CHO:_________________________。
(4)已知A能使酸性高锰酸钾褪色,还原产物为Mn2+,写出该氧化还原反应的离子方程式____________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com