
| 弱酸化学式 | CH3COOH | HClO | H2CO3 |
| 电离平衡常数 | 1.8×10-5 | 3.0×10-8 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
| A、等物质的量的Na2CO3和CH3COOH两种溶液混合,一定 有:c(Na+)+c(H+)=2c(CO32-)+c (HCO3-)+c (CH3COO-) |
| B、常温下,已知酸H2A存在如下平衡:H2A?H++HA-;HA-?H++A2-(Ka1=5.9xl0-2,Ka2=6.4xl0'6),则NaHA溶液中水的电离程度一定大于纯水中水的电离程度 |
| C、相同浓度的CH3COONa和NaClO混合溶液中各离子浓度大小关系是:c (Na+)>c (ClO-)>c (CH3COO-)>c (OH-)>c (H+) |
| D、常温下,在O.lmol/LCH3COOH溶液中滴加O.lmol/LNaOH的溶液发生反应,当c(CH3COOH):c (CH3COO-)=5:9时,此时溶液pH=5 |
| c(H+)×c(CH3COO-) |
| c(CH3COOH) |
| c(H+)×c(CH3COO-) |
| c(CH3COOH) |


科目:高中化学 来源: 题型:
A、O原子的轨道表示式为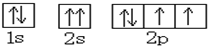 |
B、H2O的电子式为 |
| C、Ca原子的电子排布式为 1s22s22p63s23p63d2 |
D、K原子的原子结构示意图为 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 俗称“一滴香”的有毒物质被人食用后会损伤肝脏,还能致癌“一滴香”的分子结构如图所示,下列说法正确的是( )
俗称“一滴香”的有毒物质被人食用后会损伤肝脏,还能致癌“一滴香”的分子结构如图所示,下列说法正确的是( )| A、该有机物的分子式为C7H6O3 |
| B、1mol该有机物最多能与2molH2发生加成反应 |
| C、该有机物能发生取代、加成和氧化反应 |
| D、该有机物的一种芳香族同分异构体能发生眼镜反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1-溴丙烷与NaOH醇溶液共热 |
| B、乙醇与浓H2SO4共热至140℃ |
| C、溴乙烷与NaOH水溶液共热 |
| D、乙醇与NaOH醇溶液共热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 将反应5IO3-+I-+6H+?3I2+3H2O设计成如图所示的原电池.开始时向甲烧杯中加入少量浓硫酸,电流计指针发生偏转,一段时间后,电流计指针回到零,再向甲烧杯中滴入几滴浓NaOH溶液,电流 计指针再次发生偏转.下列判断不正确的是( )
将反应5IO3-+I-+6H+?3I2+3H2O设计成如图所示的原电池.开始时向甲烧杯中加入少量浓硫酸,电流计指针发生偏转,一段时间后,电流计指针回到零,再向甲烧杯中滴入几滴浓NaOH溶液,电流 计指针再次发生偏转.下列判断不正确的是( )| A、开始加入少量浓硫酸时,乙中石墨电极上发生氧化反应 |
| B、开始加入少量浓硫酸时,同时在甲、乙烧杯中都加入淀粉溶液,只有乙烧杯中溶液变蓝 |
| C、电流计读数为零时,反应达到化学平衡状态 |
| D、两次电流计指针偏转方向相反 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、K+、SO42-、OH- |
| B、Na+、K+、Cl-、HCO3- |
| C、Na+、Cu2+、CO32-、Br- |
| D、Na+、Mg2+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 稀硫酸 |
| 足量NaOH |
| 蒸干、灼烧 |
| 一定条件 |
| 120℃ | 300℃ | 480℃ | |
| 化学式 | KxFey(C2O4)Z | KxFeyO(C2O4)Z-1 | KxFeyO2(C2O4)Z-2 |
| 质量 | 4.370g | 3.650g | 2.930g |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、利用图1制取并收集干燥的氨气 |
| B、利用图2制取Fe(OH)2,使用煤油的目的是防止生成的Fe(OH)2被空气氧化 |
| C、利用图3制取并收集NO2气体 |
| D、利用图4用酒精制取无水乙醇 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com