
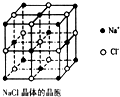
 纳米材料的表面微 粒占总微粒数的比例极大,这是它有许多特殊性质的原因.假设某氯化钠纳米颗粒的大小和形状恰好与氯化钠晶胞的大小和形状相同(如图所示),则这种纳米颗粒的表面微粒数与总微粒数的比值为( )
纳米材料的表面微 粒占总微粒数的比例极大,这是它有许多特殊性质的原因.假设某氯化钠纳米颗粒的大小和形状恰好与氯化钠晶胞的大小和形状相同(如图所示),则这种纳米颗粒的表面微粒数与总微粒数的比值为( )| A、7:8 | B、13:14 |
| C、25:26 | D、26:27 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
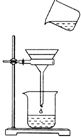 已知粗盐中含有泥沙,硫酸钠、氯化钙杂质,在进行提纯的过程中,某学生设计了如图所示的实验操作.回答下列问题:
已知粗盐中含有泥沙,硫酸钠、氯化钙杂质,在进行提纯的过程中,某学生设计了如图所示的实验操作.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、a<b | B、a=b |
| C、a>b | D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等浓度等体积的强酸与强碱溶液混合后,溶液的pH=7 |
| B、pH=2的盐酸与pH=12的氨水等体积混合后所得溶液显中性 |
| C、pH=10的Ba(OH)2溶液和pH=13的NaOH溶液等体积混合后溶液的pH=10.7(已知lg2=0.3) |
| D、将10mLpH=a的盐酸与100mLpH=b的Ba(OH)2溶液混合后恰好中和,则a+b=13 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.2mol |
| B、0.6mol |
| C、0.8mol |
| D、1.0mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
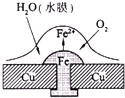 已知铅蓄电池的总反应PbO2+Pb+2H2SO4═2PbSO4+2H2O,图为铁铆钉铆在铜板上,有关叙述不正确的是( )
已知铅蓄电池的总反应PbO2+Pb+2H2SO4═2PbSO4+2H2O,图为铁铆钉铆在铜板上,有关叙述不正确的是( )| A、如图,铁铆钉发生吸氧腐蚀,在铁钉附近滴加K3[Fe(CN)6]溶液,可观察铁钉附近有蓝色沉淀产生 |
| B、铅蓄电池充电时,阳极电极反应为PbSO4+2H2O-2e-=PbO2+4H++SO42- |
| C、铅蓄电池放电时,电路中每转移2mol电子,消耗1mol硫酸 |
| D、铅蓄电池放电时,内电路硫酸根离子向铅极移动,正极附近溶液的pH增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、44.8 L氟化氢气体分解成22.4 L的氢气和22.4 L的氟气吸收270 kJ热量 |
| B、1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量大于270 kJ |
| C、相同条件下,1mol氢气与1mol氟气的能量总和高于2mol氟化氢气体的能量 |
| D、2mol H-F键的键能比1mol H-H键和1mol F-F键的键能之和大270 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入NaHCO3 |
| B、加入AgNO3固体 |
| C、加入FeCl3固体 |
| D、降温 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com