
【题目】下表为元素周期表中的一部分,表中列出8种元素在周期表中的位置,按要求回答下列问题。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ④ | ⑥ | ||||||
3 | ① | ② | ③ | ⑤ | ⑦ | ⑧ |
(1)在①~⑧元素中化学性质最不活泼的元素的名称是____,金属性最强的元素的名称是____。
(2)③、④、⑥三种元素中的原子半径最小的是_____________(填元素符号)。
(3)①、②、③三种元素形成的离子,离子半径由大到小的顺序是____(用离子符号填写)。
(4)④与⑥形成的化合物的电子式为_____________。
(5)写出①和③两种元素的最高价氧化物对应的水化物相互反应的离子方程式:____。
【答案】氩 钠 O Na+、Mg2+、Al3+ ![]() Al(OH)3+OH-=AlO2-+2H2O
Al(OH)3+OH-=AlO2-+2H2O
【解析】
根据元素周期表的结构,可知这8种元素从①到⑧分别为Na、Mg、Al、C、Si、O、Cl、Ar,结合元素结构与性质分析解答。
从①到⑧分别为Na、Mg、Al、C、Si、O、Cl、Ar;
(1)在①~⑧元素中化学性质最不活泼的元素是稀有气体元素氩,金属性最强的元素位于周期表的左下方,是钠;
(2)③、④、⑥三种元素中,碳和氧核外有两层电子,Al核外有三层电子,所以碳和氧的原子半径小于Al,氧的质子数大于碳,当电子层数相同时,质子数越多,半径越小,所以氧的原子半径小于碳,故原子半径最小的是O;
(3)①、②、③三种元素形成的离子分别为Na+、Mg2+、Al3+,它们的电子层数均为2层,当电子层数相同时,质子数越多,离子半径越小,所以离子半径由大到小的顺序是Na+、Mg2+、Al3+;
(4)④与⑥形成的化合物为CO2,电子式为![]() ;
;
(5)①和③两种元素的最高价氧化物对应的水化物分别为NaOH和Al(OH)3,两者相互反应的离子方程式为:Al(OH)3+OH-= AlO2-+2H2O。


科目:高中化学 来源: 题型:
【题目】一定条件下,在密闭容器中充入CO2与H2进行反应:2CO2(g)+6H2(g) ![]() CH3OCH3(g)+3H2O(g) ΔH。采用催化剂甲和催化剂乙分别发生上述反应,测得反应进行相同时间时CO2的转化率α(CO2)随反应温度T的变化曲线如下图所示(忽略温度对催化剂活性的影响):
CH3OCH3(g)+3H2O(g) ΔH。采用催化剂甲和催化剂乙分别发生上述反应,测得反应进行相同时间时CO2的转化率α(CO2)随反应温度T的变化曲线如下图所示(忽略温度对催化剂活性的影响):
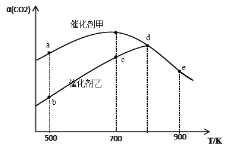
下列叙述正确的是
A. 该可逆反应的ΔH>0
B. 催化剂甲作用下反应的活化能比催化剂乙作用下反应的活化能大
C. 500K下达到平衡时,反应在催化剂甲作用下的转化率比在催化剂乙作用下的转化率高
D. d、e两点反应已经达到平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知乙酸中的氧都是18O,则乙酸和乙醇在一定条件下反应,经过足够长的时间后,体系中含有18O的物质是
A. 只有乙酸
B. 只有乙酸乙酯
C. 乙酸、乙酸乙酯、水
D. 乙酸乙酯、乙醇、水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为硬脂酸甘油酯在碱性条件下水解的装置图。进行皂化反应的步骤如下:
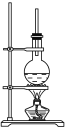
(1)在烧瓶中装入7~8 g硬脂酸甘油酯,然后加入2~3 g的NaOH、5 mL H2O和10 mL酒精。加入酒精的作用是________________________________________________________。
(2)图中长玻璃导管的作用是_______________________________________。
(3)该反应的化学方程式是______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学通过如下流程制备氧化亚铜:
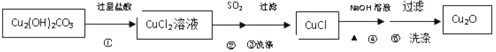
已知:![]() 难溶于水和稀硫酸;
难溶于水和稀硫酸;![]()
下列说法错误的是
A.步骤②中的![]() 可用
可用![]() 替换
替换
B.在步骤③中为防止![]() 被氧化,可用
被氧化,可用![]() 水溶液洗涤
水溶液洗涤
C.步骤④发生反应的离子方程式为:![]()
D.如果![]() 试样中混有
试样中混有![]() 和
和![]() 杂质,用足量稀硫酸与
杂质,用足量稀硫酸与![]() 试样充分反应,根据反应前、后固体质量可计算试样纯度
试样充分反应,根据反应前、后固体质量可计算试样纯度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用煤化工产品![]() 合成高分子材料I的路线如下:
合成高分子材料I的路线如下:
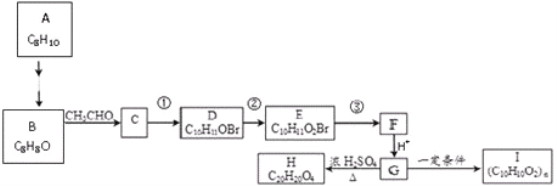
已知:(1)B、C、D都能发生银镜反应,G的结构简式为
(2)![]()
![]()
根据题意完成下列填空:
(1)A的结构简式为__________________。
(2)实验空由A制得B可以经过三步反应,第一步的反应试剂及条件为![]() /光照,第二步是水解反应,则第三步的化学反应方程式为____________________。
/光照,第二步是水解反应,则第三步的化学反应方程式为____________________。
(3)①的反应类型为_______________反应。
(4)③的试剂与条件为__________________________。
(5)I的结构简式为___________;请写出一个符合下列条件的G的同分异构体的结构简式____________。
①能发生银镜反应 ②能发生水解反应
③苯环上一氯取代物只有一种 ④羟基不与苯环直接相连
(6)由乙醇为原料可以合成有机化工原料1-丁醇(![]() ),写出其合成路线________________。(合成路线需用的表示方式为:
),写出其合成路线________________。(合成路线需用的表示方式为:![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把0.4molX气体和0.6molY气体混合于2L密闭容器中,使它们发生如下反应:4X(g)+5Y(g) ![]() nZ(g)+6W(g)。2min末已生成0.3molW,若测知以Z的浓度变化表示的反应速率为0.05mol/(L·min),试计算
nZ(g)+6W(g)。2min末已生成0.3molW,若测知以Z的浓度变化表示的反应速率为0.05mol/(L·min),试计算
(1)前2min内用W的浓度变化表示的平均反应速率为_______________。
(2)2min末时Y的浓度为_____________________________。
(3)化学反应方程式中n=_____________________________。
(4)2min末,恢复到反应前温度,体系内压强是反应前压强的__________倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为部分短周期非金属元素的性质或原子结构,已知A﹣D的原子序数依次增大。
元素编号 | 元素性质或原子结构 |
A | A原子所处的周期数、族序数、原子序数均相等 |
B | 核外电子有6种不同运动状态 |
C | 最简单氢化物的水溶液呈碱性 |
D | 基态原子的s轨道电子数等于p轨道电子数 |
请结合表中信息完成下列各小题(答题时用所对应的元素符号):
(1)写出C原子的电子排布图________。
(2)A,B,C,D的第一电离能由大到小的顺序为________。
(3)用电离方程式表示C的最简单氢化物的水溶液呈碱性的原因________。按照共价键理论,分子中每个原子的最外电子层电子数均已饱和,已知ABCD分子可能有三种不同结构,它们的结构可以从其他物质的结构中获得启发。
(4)ABC的结构式是______,向其中插入一个D原子,若形成配位键(用→表示)则ABCD的结构式为_______,分子中C的原子的杂化类型是______;若无配位键则ABCD的结构式为______分子中D原子的杂化类型为________。
(5)BD2的电子式是________将D原子换成等电子的 ![]() 所得ABCD的结构式为_______,分子中C原子的杂化类型是_______。
所得ABCD的结构式为_______,分子中C原子的杂化类型是_______。
(6)在ABCD的三种可能结构中B原子的杂化类型________(填“相同”或“不相同”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com