
【题目】利用下列各组中的物质作用制备和收集少量相应气体,能采用如图实验装置的是:①浓氨水与固体氢氧化钠②浓硫酸与食盐③过氧化氢溶液与二氧化锰④稀硝酸与铜片⑤镁条与稀硫酸⑥电石与水 ( )

A.①②③⑥B.①②⑥C.②③D.全部
【答案】C
【解析】
①浓氨水易挥发,固体氢氧化钠溶于水放热,导致溶液温度升高,使得氨气在水中的溶解度进一步减少,以气体的形式逸出,制得氨气,所以能用图中的左图部分制备,由于氨气的密度比空气的平均密度小,只能用向下排空气法收集,而图中的收集装置为向上排空气法,故①错误;
②浓硫酸与食盐可生成氯化氢气体,且气体密度比空气大,可用向上排空气法收集,故②正确;
③过氧化氢溶液在二氧化锰催化作用下可制得氧气,且氧气密度比空气大,可用向上排空气法收集,故③正确;
④稀硝酸与铜片反应生成NO,NO易与空气中氧气反应生成NO2,则NO不能用排空气法收集,故④错误;
⑤镁条与稀硫酸反应生成氢气,氢气的密度比空气密度小,只能用向下排空气法收集,故⑤错误;
⑥电石与水反应生成乙炔,乙炔的密度比空气密度略小,一般用排水法收集,肯定不能用向上排空气法收集,故⑥错误;
②③正确,故答案为C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在一定温度下,CO和CH4燃烧的热化学方程式分别为
2CO(g)+O2(g)=2CO2(g) ΔH=-566kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890kJ/mol
1molCO和3molCH4组成的混合气体,在相同条件下完全燃烧时,释放的热量为( )
A.2912kJB.2953kJC.3236kJD.3867kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸是一种常见的弱酸,请回答:
(1)已知某温度时,醋酸的电离平衡常数Ka=1.6×10-5。
①醋酸的起始浓度为0.010mol/L,平衡时c(H+)=______(提示:醋酸的电离平衡常数很小,平衡时的c(CH3COOH)可近似视为仍等于0.010mol/L
②pH=1的醋酸与pH=l的盐酸等体积混合,混合后溶液中c(CH3COO-)=_______。
(2)日常生活中常用醋酸除水垢,但工业锅炉的水垢中常含有CaSO4,需先用________(填化学式)溶液处理,而后用盐酸去除。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2008年12月15日,全球第一款不依赖专业充电站的双模电动车--比亚迪F3DM双模电动车在深圳正式上市.比亚迪F3DM双模电动车代表着“科技![]() 绿色明天”,运用了众多高新科技,开启了电动车的新时代,同时也实现了中国力量领跑世界.镍镉
绿色明天”,运用了众多高新科技,开启了电动车的新时代,同时也实现了中国力量领跑世界.镍镉![]() 可充电电池在现代生活中有广泛应用.已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:
可充电电池在现代生活中有广泛应用.已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:![]() 有关该电池的说法正确的()
有关该电池的说法正确的()
A.充电过程是化学能转化为电能的过程
B.充电时阳极反应:![]()
C.放电时负极附近溶液的酸性增强
D.放电时电解质溶液中的![]() 向正极移动
向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)①在BF3分子中,F—B—F的键角是________,B原子的杂化轨道类型为________,BF3和过量NaF作用可生成NaBF4,BF![]() 的立体构型为________;
的立体构型为________;
②在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为________,层间作用力为________。
(2)①Y2X2(C2H2)分子中Y原子轨道的杂化类型为______,1 mol Y2X2含有σ键的数目为______。
②元素Y(C)的一种氧化物与元素Z(N)的一种氧化物互为等电子体,元素Z的这种氧化物的分子式为________。
③化合物ZX3(NH3)的沸点比化合物YX4(CH4)的高,其主要原因是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【题目】一定温度下,反应N2(g)+3H2(g)![]() 2NH3(g)达到化学平衡状态的标志是
2NH3(g)达到化学平衡状态的标志是
A. c(N2):c(H2):c(NH3)=1:3:2
B. N2、H2和NH3的物质的量分数不再改变
C. N2与H2的物质的量之和是NH3的物质的量的2倍
D. 单位时间里每增加lmolN2,同时增加3molH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A.向NaHCO3溶液中加入足量的Ba(OH)2:2HCO3-+Ba2++2OH-=BaCO3↓+ CO32-+2H2O
B.向亚硫酸钠溶液中滴入少量新制的氯水:3SO32-+ Cl2+H2O= SO42-+2Cl-+2HSO3-
C.电解KI溶液阴极电极反应2H2O-4e-= O2↑+4H+
D.Fe2O3固体投入到少量HI溶液中:Fe2O3+6H++6I-=2Fe2++3I2+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酸性氢氧燃料电池电解苦卤水![]() 含
含![]() 、
、![]() 、
、![]() 、
、![]() 的装置如图所示
的装置如图所示![]() 、b为石墨电极
、b为石墨电极![]() ,下列说法正确的是
,下列说法正确的是
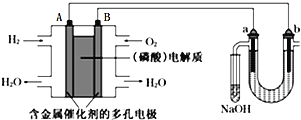
A.电池工作时,B极反应式为![]()
B.电解时,电子流动路径是:A极![]() 外电路
外电路![]() 极
极![]() 溶液
溶液![]() 极
极![]() 极
极
C.NaOH溶液充分吸收后所得溶液可制作漂白水
D.当电池中消耗![]() 标准状况
标准状况![]() 时,a极周围也会产生
时,a极周围也会产生![]() 标准状况
标准状况![]() 气体
气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法正确的是
A.常温下,10 mL pH=1的醋酸溶液中含有的氢离子数为0.001NA
B.合成氨反应中,1 mol N2与4 mol H2反应生成的NH3分子数为2NA
C.用碱性锌锰干电池作电源电解饱和食盐水,当消耗MnO2 8.7g时,可制得标况下氯气2.24L(不考虑氯气的溶解;电池工作时MnO2转化为MnOOH)
D.常温常压下,18.4 g NO2和N2O4的混合气体中含有的氮原子总数为0.8NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com