
【题目】【题目】一定温度下,反应N2(g)+3H2(g)![]() 2NH3(g)达到化学平衡状态的标志是
2NH3(g)达到化学平衡状态的标志是
A. c(N2):c(H2):c(NH3)=1:3:2
B. N2、H2和NH3的物质的量分数不再改变
C. N2与H2的物质的量之和是NH3的物质的量的2倍
D. 单位时间里每增加lmolN2,同时增加3molH2
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】用浓盐酸和MnO2制取Cl2的装置如下,某小组欲证明产生的气体中含有HCl。
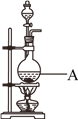
(1)Cl2的电子式是__________,A中反应的离子方程式为____________________。
(2)甲同学将A中产生的气体通入下列溶液:
实验序号 | 试剂 | 现象 |
a | 紫色石蕊溶液 | |
b | AgNO3 | 出现白色沉淀 |
①实验a中的现象为__________。
②不能证明产生的气体中含有HCl的实验是__________(填字母序号)
(3)已知将HCl气体通入饱和食盐水中有白色固体析出。乙同学将A中产生的气体通入饱和食盐水中,有白色固体析出,但实验不能证明气体中含有HCl,结合化学用语解释其原因:_______________________________________________________________________________
(4)已知:2S2O32-+I2=S4O62-+2I-。丙同学将A中产生的气体通入蒸馏水中,得到溶液X,进行以下实验证明气体中含有HCl。
实验I.测定X中溶解的Cl2。取25.00mL溶液X,加入过量KI溶液,然后用0.04mol·L-1Na2S2O3溶液滴定生成的I2,达滴定终点时消耗Na2S2O3溶液VmL。
实验II.测定X中Cl元素重量。另取25.00mL溶液X,选用适当的还原将溶解的Cl2全部还原为Cl-,再用0.10mol·L-1AgNO3溶液滴定说的溶液中的CI-。
①X中的HClO不会影响实验I的测定结果,原因是__________。
②由I、II中实验数据可证明A中产生的气体中含有HCl,则II中0.10mol·L-1AgNO3溶液的体积应大于__________mL(用含V的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素及其化合物在生活及生产中有很多重要用途。
Ⅰ.SiC、BN、GaAs 等是人工合成半导体的材料,具有高温、高频、大功率和抗辐射等优点。请回答:
(1)第一电离能:Ga_______As(填“>”、 “<”、“=”)。
(2)B、C、N的电负性由小到大排列为_______
Ⅱ.卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(1)拟卤素(CN)2、(SCN)2与卤素单质结构相似、性质相近,分子中所有原子都满足 8 电子结构。(SCN)2对应的酸有两种,测得硫氰酸(H—S—C≡N )的沸点低于异硫氰酸(H—N=C=S),其原因是_______。
(2)卤化物 RbICl2在加热时会分解为晶格能相对较大的卤化物 A 和卤素互化物或卤素单质,A 的化学式为_______;I3+属于多卤素阳离子,其空间构型为_______
(3)卤素互化物如IBr、ICl等与卤素单质结构和性质相似。Cl2、IBr、ICl沸点由高到低的顺序为_______。
(4)请推测①HC1O4、②HIO4、③H5IO6[可写成(HO)5IO]三种物质的酸性由强到弱的顺序为_______(填序号)。
(5)CaC2晶体的晶胞结构与 NaCl 晶体的相似(如图所示),CaC2晶体中的哑铃形 C22﹣的存在,使晶胞沿一个方向拉长。此晶体中 1 个 C22﹣周围距离最近的Ca2+为_______个;若该晶胞的边长为a、a、b(pm),则该晶体的密度为_______g·cm-3(写出表达式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物甲、乙用于制备化妆品,二者合成路线如下(部分产物及条件略):

已知:
 (-R、-R'代表烃基或-H)
(-R、-R'代表烃基或-H)
(1)D的结构简式是_______________________。
(2)化合物A能与浓溴水反应产生白色沉淀。
①“E→F”的反应类型是_______________。
②“F→有机化合物甲”的化学方程式是________________________。
③化合物A的结构简式是_________________________。
(3)化合物C的分子式为C3H6O,核磁共振氢谱显示只有一种化学环境的氢。C的结构简式是__________________________。
(4)化合物W的相对分子质量为106,关于B与W的说法,正确的是________________。
a. 互为同系物
b. 可以用酸性KMnO4溶液鉴别
c. 相同物质的量的B和W与H2完全反应,消耗H2物质的量不同
(5)M、N中均只含一种官能团,N中含有四个甲基。X的结构简式是________________。
(6)N的同分异构体在相同的反应条件下也能满足上述合成路线,写出满足上述合成路线的N的同分异构体_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质的叙述正确的是( )
A. 液态HCl不导电,所以HCl是非电解质
B. NH3的水溶液能够导电,所以NH3是电解质
C. 液态Cl2不导电,所以Cl2是非电解质
D. 熔融NaCl可以导电,所以NaCl是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增加。K、L、M、N均是由这些元素组成的二元化合物,甲、乙分别是元素X、Y的单质,甲是固体,乙是气体,K是主要的大气污染物之一,0.05mol·L-1丙溶液的pH为1,上述物质的转化关系如下图所示。下列说法正确的是( )

A. 原子半径:W<X<Y<Z B. 元素的非金属性:Y>Z>X
C. 原子最外层电子数:W<X<Y<Z D. K、L、M、N四种物质中沸点最高的是N
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按题目要求答题:
(1)(CH3)2CHCH(CH3)2的系统命名是_________
(2)写出甲苯与浓硫酸、浓硝酸的混合酸在100℃发生取代反应的化学方程式:_____
(3)支链只有一个乙基且相对分子质量最小的烷烃的结构简式________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度和压强下,将装有N2和NO2混合气体的试管倒立在水中,经足够的时间后,试管内气体的体积缩小为原体积的3/5,则原混合气体中N2和NO2体积比是
A. 2/3 B. 3/2 C. 3/5 D. 5/3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com