
����Ŀ���л�������ס��������Ʊ���ױƷ�����ߺϳ�·�����£����ֲ��P�����ԣ���

��֪��
 ��-R��-R'����������-H��
��-R��-R'����������-H��
��1��D�Ľṹ��ʽ��_______________________��
��2��������A����Ũ��ˮ��Ӧ������ɫ������
�١�E��F���ķ�Ӧ������_______________��
�ڡ�F���л�������ס��Ļ�ѧ����ʽ��________________________��
�ۻ�����A�Ľṹ��ʽ��_________________________��
��3��������C�ķ���ʽΪC3H6O���˴Ź���������ʾֻ��һ�ֻ�ѧ�������⡣C�Ľṹ��ʽ��__________________________��
��4��������W����Է�������Ϊ106������B��W��˵������ȷ����________________��
a. ��Ϊͬϵ��
b. ����������KMnO4��Һ����
c. ��ͬ���ʵ�����B��W��H2��ȫ��Ӧ������H2���ʵ�����ͬ
��5��M��N�о�ֻ��һ�ֹ����ţ�N�к����ĸ�����X�Ľṹ��ʽ��________________��
��6��N��ͬ���칹������ͬ�ķ�Ӧ������Ҳ�����������ϳ�·�ߣ�д�����������ϳ�·�ߵ�N��ͬ���칹��_________________________________________��
���𰸡� CH��CH �ӳɷ�Ӧ��ԭ��Ӧ 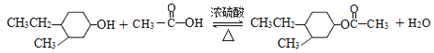
![]() a b
a b 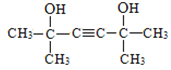
![]()
����������1��CaC2��ˮ��Ӧ����CH��CH����DΪCH��CH��
��2��CH��CH��H2�ӳɵõ�CH2=CH2������F���ķ�Ӧ���������Ľṹ��֪��F������Ϊ������Ӧ��������FΪ![]() ����ϩ��A��Ӧ�õ�E��E��H2�ӳɵõ�F��A����Ũ��ˮ��Ӧ������ɫ��������A���б��������ǻ����ٸ���F��̼ԭ�������Ʋ�AΪ
����ϩ��A��Ӧ�õ�E��E��H2�ӳɵõ�F��A����Ũ��ˮ��Ӧ������ɫ��������A���б��������ǻ����ٸ���F��̼ԭ�������Ʋ�AΪ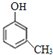 ����E��F��ӦΪ�����������ļӳɣ�����EΪ
����E��F��ӦΪ�����������ļӳɣ�����EΪ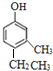 ��
��
�ٸ���������������E��F��Ϊ�ӳɷ�Ӧ���������ӳ�Ҳ�ɳ�Ϊ��ԭ��Ӧ��
�ڡ�F������Ϊ������Ӧ����Ӧ����ʽΪ��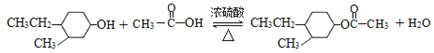 ��
��
�۸�����������A�Ľṹ��ʽΪ�� ��
��
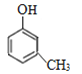
��3��C�ķ���ʽΪC3H6O���˴Ź���������ʾֻ��һ�ֻ�ѧ�������⣬��CΪ![]() ��
��
��4����D+C��X������CH��CH + ![]() ��X����������֪��Ϣ��֪�÷�ӦΪ�ӳɷ�Ӧ��X�к���̼̼˫�����ǻ���M��N�о�ֻ��һ�ֹ����ţ�����X��M���ķ�Ӧ�м���һ�ֹ����ţ��ٽ����M��N���ķ�Ӧ�����Ʋ⣬M�к����ǻ�����X��M���ķ�Ӧ�м�����̼̼˫���� ������X��M��Ϊ̼̼�����ļӳɷ�Ӧ����M��N��Ϊ�ǻ��ķ�Ӧ��M��N������֪��Ϣ�еĵ�һ���ӳɷ�Ӧ���ʿ��ƶ�M�к��б�����N�к���̼̼˫����������M��N��Ϊ���ǻ�����ȥ��Ӧ����X��M��N��̼�ĹǼ���ͬ��N�к���4��������X��M��Ҳ����4������������ȲӦ��2���ӱ�ͪ�����ӳ�����X����XΪ
��X����������֪��Ϣ��֪�÷�ӦΪ�ӳɷ�Ӧ��X�к���̼̼˫�����ǻ���M��N�о�ֻ��һ�ֹ����ţ�����X��M���ķ�Ӧ�м���һ�ֹ����ţ��ٽ����M��N���ķ�Ӧ�����Ʋ⣬M�к����ǻ�����X��M���ķ�Ӧ�м�����̼̼˫���� ������X��M��Ϊ̼̼�����ļӳɷ�Ӧ����M��N��Ϊ�ǻ��ķ�Ӧ��M��N������֪��Ϣ�еĵ�һ���ӳɷ�Ӧ���ʿ��ƶ�M�к��б�����N�к���̼̼˫����������M��N��Ϊ���ǻ�����ȥ��Ӧ����X��M��N��̼�ĹǼ���ͬ��N�к���4��������X��M��Ҳ����4������������ȲӦ��2���ӱ�ͪ�����ӳ�����X����XΪ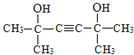 ��X�������ӳɵõ�M��MΪ
��X�������ӳɵõ�M��MΪ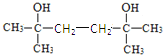 ��M������ȥ��Ӧ�õ�N��NΪ(CH3)2C=CH-CH=C(CH3)2��
��M������ȥ��Ӧ�õ�N��NΪ(CH3)2C=CH-CH=C(CH3)2��
����ϩ+B��W������W����Է�������Ϊ106���ٸ����ҵĽṹ��Ϣ����֪WΪ![]() ��BΪ
��BΪ![]() ��W��B�ṹ���ƣ��ҷ���ʽ���2��CH2����W��B��ͬϵ��ұ���ʹ����KMnO4��Һ��ɫ���������ܣ����Կ���������KMnO4��Һ����������W��B�������ӳɶ��DZ����ļӳɣ���ͬ���ʵ�����B��W��H2��ȫ��Ӧ������H2���ʵ�������ͬ�ġ���ѡa��b��
��W��B�ṹ���ƣ��ҷ���ʽ���2��CH2����W��B��ͬϵ��ұ���ʹ����KMnO4��Һ��ɫ���������ܣ����Կ���������KMnO4��Һ����������W��B�������ӳɶ��DZ����ļӳɣ���ͬ���ʵ�����B��W��H2��ȫ��Ӧ������H2���ʵ�������ͬ�ġ���ѡa��b��
��5��������������֪��X�Ľṹ��ʽ�ǣ�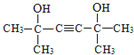 ��
��
��6������ϳ�·�ߵ�N��ͬ���칹����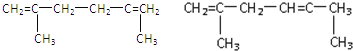 ��
��


 ȫ�ŵ�����Ԫ�ƻ�ϵ�д�
ȫ�ŵ�����Ԫ�ƻ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.Ħ���ǹ��ʿ�ѧ�罨����õ�һ��������
B.�����Ϲ涨��0.012 kg̼ԭ�������е�̼ԭ����ĿΪ1Ħ��
C.�������Ƶ�Ħ��������40g
D.������Ħ��������g/molΪ��λʱ����ֵ�ϵ���������Է�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ�Ǿ����Դ���⣬�Ӻ�ˮ����ȡʳ�κ���Ĺ������£�
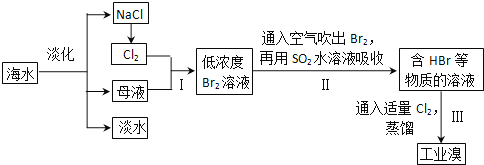
(1)��ȥ����������(Mg2+��SO42-��Ca2+)�������ҩƷ˳����ȷ����__________��
A��NaOH��Һ��Na2CO3��Һ��BaCl2��Һ�����˺������
B��BaCl2��Һ��NaOH��Һ��Na2CO3��Һ�����˺������
C��NaOH��Һ��BaCl2��Һ��Na2CO3��Һ�����˺������
D��Na2CO3��Һ��NaOH��Һ��BaCl2��Һ�����˺������
(2)����I���ѻ��Br2������II���ֽ�Br2��ԭΪBrһ����Ŀ���Ǹ�����������Ӧ�Ļ�ѧ����ʽ��______________________��
(3)ij��ѧС���ͬѧΪ���˽�ӹ�ҵ�����ᴿ��ķ������������й����ϣ�Br2�ķе�Ϊ59�档����ˮ���ж��Ժ�ǿ��ʴ�ԡ����Dzι��������̺����������ʵ��װ�ã�
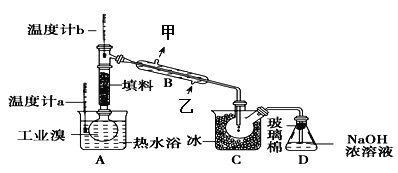
��ͼ������B��������______����ȴˮ�ij���Ϊ_______����ס����ҡ�)��
��Dװ�õ�������________________��
(4)��֪ij��Һ��Clһ��Brһ��Iһ�����ʵ���֮��Ϊ2��3��4������ʹ��Һ�е�Clһ��Brһ��Iһ�����ʵ���֮�ȱ��4��3��2����ôҪͨ��C12�����ʵ�����ԭ��Һ��Iһ�����ʵ�����____________(��ѡ��)��
A��1/2 B��1/3 C��1/4 D��1/6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Դ���ִ���ᷢչ��֧��֮һ��
��1����ѧ��Ӧ�е������仯����Ҫ����Ϊ�����ı仯��
�����з�Ӧ�У����ڷ��ȷ�Ӧ����_________������ĸ����
a��Ba(OH)2��8H2O��NH4Cl��Ͻ���
b����������ʯ��ʯ
c���������ᷴӦ
��ijͬѧ������ͼ��ʾʵ�飬����ϡ�������ռ���Һ�кͷ�Ӧ�������仯��ʵ���������Ӧ�¶����ߣ��ɴ��жϸ÷�Ӧ��_____________��������������������������Ӧ�������ӷ���ʽ��__________________________��
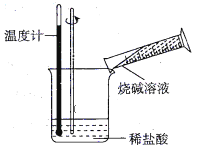
��2���������ִ����Ӧ����㷺����Դ֮һ����ͼ��ʾ��ԭ���װ���У�������____���������ܹ��۲쵽��������________�������ĵ缫��Ӧʽ��____________��ԭ��ع���һ��ʱ���������п6.5 g����ų�����_______g��
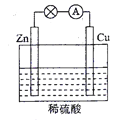
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ܶ���С�Ľ������������IJ�ͬ������﮿����ͷų�������ӣ��ʳ�������������ܵ�ء���֪﮵Ľ����Խ����ƺ�þ֮�䣬��ұ�������Ӧ���õķ�����
A. ��ⷨ B. �Ȼ�ԭ�� C. �ȷֽⷨ D. ���ȷ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��˳�����Ʊ�������֬��ԭ��M�Լ�ɱ����N�ĺϳ�·�����£�

��֪��

��1��CH2=CH-CH=CH2��������___________________________��
��2����Ӧ��ķ�Ӧ������______________________��ѡ����ĸ����
a. �Ӿ۷�Ӧ b. ���۷�Ӧ
��3��˳ʽ�ۺ���P�Ľṹʽ��__________________��ѡ����ĸ����
a.  b.
b.  c.
c. 
��4��A����Է�������Ϊ108��
�� ��Ӧ��Ļ�ѧ����ʽ��_____________________________________��
�� 1 mol B��ȫת����M������H2��������___________g��
��5����Ӧ��Ļ�ѧ����ʽ��__________________________________________��
��6��A��ijЩͬ���칹������ͬ�ķ�Ӧ������Ҳ������B��C��д������һ��ͬ���칹��Ľṹ��ʽ___________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ŀ��һ���¶��£���ӦN2(g)+3H2(g)![]() 2NH3(g)�ﵽ��ѧƽ��״̬�ı�־��
2NH3(g)�ﵽ��ѧƽ��״̬�ı�־��
A. c(N2):c(H2):c(NH3)=1:3:2
B. N2��H2��NH3�����ʵ����������ٸı�
C. N2��H2�����ʵ���֮����NH3�����ʵ�����2��
D. ��λʱ����ÿ����lmolN2��ͬʱ����3molH2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������10mL0.1mol/LNaOH��Һ�м���0.1mol/L��һԪ��HA����ҺpH�ı仯������ͼ��ʾ������˵����ȷ����

A. a����ʾ��Һ��c(A-)+c(HA)=0.1mol/L
B. a��b������ʾ��Һ��ˮ�ĵ���̶Ȳ�ͬ
C. pH=7ʱ��c(Na+)=c(A-)
D. b����ʾ��Һ��c(HA)>c(A-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���������

A. X��Y��Ӧ����Ϊ������Ӧ
B. X��Y��Z����ʹ������Ȼ�̼��Һ��ɫ
C. Y��Z��Ϊͬ���칹��
D. �����ʵ�����X��Z�ֱ�������Na��Ӧ������Na�����ʵ���֮��Ϊ2:1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com