
下列解释事实的方程式错误的是
A.测得0.1 mol·L-1氨水的pH为11:NH3·H2O NH4+ +OH-
NH4+ +OH-
B.将Na块投入水中,产生气体:2Na+2H2O=2NaOH+H2↑
C.用CuCl2溶液做导电实验,灯泡发光:CuCl2 Cu2++2Cl-
Cu2++2Cl-
D.将1 mol·L-1FeCl3溶液滴入沸水中,得到透明红褐色液体:FeCl3+3H2O Fe(OH)3(胶体)+3HCl
Fe(OH)3(胶体)+3HCl
C
【解析】
试题分析:A、测得0.1 mol·L-1氨水的pH为11是因为NH3H2O发生了电离,生成了OH,电离方程式为:NH3·H2O NH4+ +OH-,故A正确;B、将Na块投入水中,Na与H2O发生反应生成了H2,化学方程式为:2Na+2H2O=2NaOH+H2↑,故B正确;C、用CuCl2溶液做导电实验,灯泡发光,发生电解反应,电解方程式为:CuCl2
NH4+ +OH-,故A正确;B、将Na块投入水中,Na与H2O发生反应生成了H2,化学方程式为:2Na+2H2O=2NaOH+H2↑,故B正确;C、用CuCl2溶液做导电实验,灯泡发光,发生电解反应,电解方程式为:CuCl2 Cu+Cl2↑,故C错误;D、将1 mol·L-1FeCl3溶液滴入沸水中,得到透明红褐色液体,生成了Fe(OH)3胶体,化学方程式为:FeCl3+3H2O
Cu+Cl2↑,故C错误;D、将1 mol·L-1FeCl3溶液滴入沸水中,得到透明红褐色液体,生成了Fe(OH)3胶体,化学方程式为:FeCl3+3H2O Fe(OH)3(胶体)+3HCl,故D正确。
Fe(OH)3(胶体)+3HCl,故D正确。
考点:本题考查方程式的书写。


科目:高中化学 来源:2014-2015学年河北省唐山市高三上学期期末理综化学试卷(解析版) 题型:填空题
【化学——选修2化学与技术】(15分)
红矾钠(重铬酸钠:Na2Cr2O7·2H2O)是重要的基本化工原料,应用领域十分广泛。
(1)实验室中红矾钠可用铬铁矿(主要成分:FeO·Cr2O3)利用以下过程来制取。

①步骤I中反应的化学方程式为:4FeO·Cr2O3(s)+8Na2CO3(s)+7O2= 8Na2CrO4(s)+2Fe2O3(s)+8CO2
该反应的化学平衡常数的表达式为 。在常温下该反应速度极慢,下列措施中能使反应速率增大的是 。
A.升高温度 B.通入过量的空气
C.将原料粉碎 D.增加纯碱的用量
②步骤II中所得溶液显碱性,其中除含有Na2C rO4外还含有铝、硅元素的化合物,它们的化学式可能是 。
③步骤III需将溶液的pH调至7~8并煮沸,其目的是 。
④步骤Ⅳ中发生反应的离子方程式为:____。
(2)将红矾钠与KC1固体1:2(物质的量比)混合溶于水后经适当操作可得到K2Cr2O7晶体,反应方程式为:Na2CrO4 +2KCl= K2Cr2O7 +2NaCl(已知NaCl的溶解度受温度影响小,K2Cr2O7的溶解度受温度影响大),基本实验步骤为:①溶解;② ;③____ 。
④冷却、结晶,过滤,得到K2Cr2O7晶体。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省等三校高三上学期联考化学试卷(解析版) 题型:选择题
在25℃时,用蒸馏水稀释1 mol/L的醋酸溶液至0.01 mol/L,随溶液的稀释,下列说法正确的是
A.溶液中所有离子浓度均减小
B.pH的变化值等于2
C.溶液中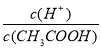 保持增大趋势
保持增大趋势
D.分别与足量的Mg粉反应,0.01 mol/L的醋酸溶液产生的氢气较少
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省等三校高三上学期联考化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.HClO的结构式:H—Cl—O
B.氨气分子的比例模型
C.原子核内有10个中子的氧原子:
D.H2与H+互为同位素
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省宁德市高三上学期期末化学试卷(解析版) 题型:填空题
(7分)用如图所示装置做“铜与浓硝酸反应”的实验。

(1)从试剂瓶中取出一小块铜片放入试管中,需用的仪器是 。
(2)棉花应蘸 溶液(填化学式)。
(3)试管中除了溶液变成绿色外,还会出现的现象是 (填序号)。
A.有红棕色气体生成,上下颜色相同
B.有红棕色气体生成,上部颜色较浅
C.有红棕色气体生成,下部颜色较浅
(4)实验结束后,对试管内残留物的处理方法是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省宁德市高三上学期期末化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.11.2 L CO2所含分子数为0.5 NA
B.1 L 0.1 mol·L-1的Na2S溶液中离子数为0.3 NA
C.0.5 mol FeBr2与足量氯气反应转移的电子数为NA
D.14.2 g Na2SO4固体中阴离子所带电荷数为0.2 NA
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省咸宁市高一上学期期末考试化学(B)试卷(解析版) 题型:实验题
某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。

(1)实验室用装置A制备SO2。某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是: 。
(2)实验室用装置E制备Cl2,其反应的化学方程式为:
MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
若有6 mol的HCl参加反应,则转移的电子总数为 。
(3)反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是: ;停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为 ,由此,你得出的结论是 。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1∶1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)____________。
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省咸宁市高一上学期期末考试化学(B)试卷(解析版) 题型:选择题
化学是一门以实验为基础的科学,掌握基本的实验方法和操作技能是做好化学实验的基础,下列有关化学实验基本知识的描述不正确的是
A.丁达尔效应可用于区别FeCl3饱和溶液和Fe(OH)3胶体
B.过滤和蒸发操作中均用到玻璃棒,但玻璃棒的作用不相同
C.萃取和洗气过程均发生的是物理变化
D.植物油和水的混合物可以用分液的方法分离
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省荆门市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列气体中,既可用浓硫酸干燥,又可用固体NaOH干燥的是
A.Cl2 B.O2 C.SO2 D.NH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com