
取一小块金属钠放在燃烧匙里加热,下列对实验现象的描述正确的是( )
①金属钠熔化 ②在空气中燃烧,火焰为紫色 ③燃烧后得到白色固体 ④燃烧时火焰为黄色 ⑤燃烧后生成淡黄色固体物质
A.①② B.①②③
C.①④⑤ D.④⑤
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
下列反应中,不属于四种基本反应类型,但属于氧化还原反应的是( )
|
| A. | 2Na+2H2O=2NaOH+H2↑ | B. | CH4+2O2 |
|
| C. | 2KClO3 | D. | CaCO3+2HCl=CaCl2+H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知在1×lO5 Pa、298 K条件下,2 mol氢气燃烧生成水蒸气放出484 kJ热量,下列热化学方程式正确的是
A. H2O(g)=H2(g)+ 1/2O2 (g)△H=+242 kJ.mol-1 B. 2H2(g)+O2(g)=2H2O(l) △H= -484 kJ.mol-l
C. H2(g)+ 1/2O2(g)=H2O(g) △H=+242 kJ.mol-l D. 2H2(g) + O2(g) = 2 H2O(g) △H= -484 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.电解精炼铜时,若转移了NA个电子,则阴极析出32 g铜
B.标准状况下,33.6 L三氧化硫中含有1.5 NA个三氧化硫分子
C.1mol Cl2与过量的铁反应,转移3NA个电子
D.1 mol FeCl3跟水反应,完全转化为氢氧化铁胶体后,其中胶体粒子的数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上设计将VOSO4中的K2SO4、SiO2杂质除去并回收得到V2O5的流程如下:
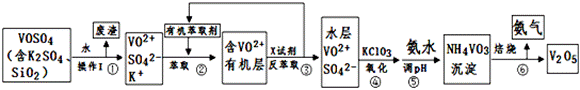 请回答下列问题:
请回答下列问题:
(1)步骤①所得废渣的成分是 (写化学式)
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):
R2(SO4)n (水层)+2nHA(有机层) 2RAn(有机层)+nH2SO4 (水层)
2RAn(有机层)+nH2SO4 (水层)
②中萃取时必须加入适量碱,其原因是 。
③中X试剂为 。
(3)④的离子方程式为 。
(4)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
结合上表,在实际生产中,⑤中加入氨水,调节溶液的最佳pH为 。
若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)< 。
(已知:25℃时,Ksp[Fe(OH)3]=2.6×10-39)
该工艺流程中,可以循环利用的物质有 和 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于Na2CO3和NaHCO3性质的说法错误的是( )
A.热稳定性:NaHCO3<Na2CO3
B.与同浓度盐酸反应的剧烈程度:NaHCO3<Na2CO3
C.相同温度时,在水中的溶解性:NaHCO3<Na2CO3
D.等物质的量浓度溶液的pH:NaHCO3<Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
CO2与SO2都是酸性氧化物,具有一定的相似性。Na2O2和CO2能反应,某化学兴趣小组的同学据此认为Na2O2和SO2也能反应,为此设计了如下实验装置来验证Na2O2和SO2反应的产物。
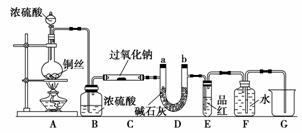
如图安装仪器,检查装置气密性后添加药品并滴入适量浓硫酸。回答下列问题:
(1)点燃A处酒精灯,不久可观察到烧瓶中产生大量气体,写出反应的化学方程式:____________________________;C处玻璃管管壁发热,管内药品的颜色变化是___________________________________________________________________。
(2)在反应过程中如何用较简便的操作证明反应产生了O2?____________________________________。
(3)E处用排水法收集气体,由什么现象可证明收集的气体中已不含SO3?________________________________________________________________________。
(4)待反应结束后,取C处玻璃管内的少量固体装入试管中,加水溶解时未产生气体,则如何证明产物中有Na2SO3?______________________________。
(5)待反应结束后,取C处玻璃管内的少量固体装入试管中,加入足量的盐酸,再加入氯化钡溶液,发现有白色沉淀生成,试分析产生沉淀的原因:________________________________________________________________________
________________________________________________________________________。
(6)有的同学认为:若将装置末端的烧杯换成量筒(或量气管),则可通过测定排水的体积来测定Na2O2药品的纯度。试判断该方案是否可行:________(填“是”或“否”),原因是________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
H-是负一价的阴离子,它可与NH3发生以下反应:H-+NH3= H2+NH2-,下列有关这个反应的说法中不正确的是
A. 该反应中NH3被还原 B.该反应中H-是还原剂
C.该反应中NH2-是还原产物 D.反应中被氧化和被还原的元素都是H元素
查看答案和解析>>
科目:高中化学 来源: 题型:
氢氟酸(HF)是一种弱酸。25℃时,向20mLO.1mol•L-1氢氟酸中加入VmL0.1mol•L-1NaOH溶液充分反应。已知: HF(aq)+OH-(aq)═F-(aq)+H2O(1) △H= - 67.7kJ•mol-1,
H+(aq)+OH-(aq)═H2O (1) △H═ - 57.3kJ•mol- 根据题意,下列判断或结论正确的是
A.氢氟酸的电离过程是吸热的
B.当V=20时,溶液中:c(F-)<c(Na+)=0.1mol•L-1
C.当V<20时,溶液中离子浓度关系可能为:c(Na+)=c(F-)
D.当V>20时,溶液中离子浓度关系一定为:c(Na+)>c(F-)>c(OH-)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com