
【题目】下列选项中,所用试剂不能达到鉴别的目的的是
A.用溴水鉴别苯和己烯B.用银氨溶液鉴别葡萄糖和乙醛
C.用金属钠鉴别乙醇和乙醛D.用碳酸钠溶液鉴别乙酸和乙酸乙酯
科目:高中化学 来源: 题型:
【题目】氢氧化镁是一种用途广泛、极具开发前景的环保材料,广泛应用在阻燃、废水中和、烟气脱硫等方面.镁硅酸盐矿石(主要成分Mg3Si2O5(OH)4 , 含氧化铝、氧化铁、氧化亚铁等杂质)可用于生产氢氧化镁,简要工艺流程如图1: 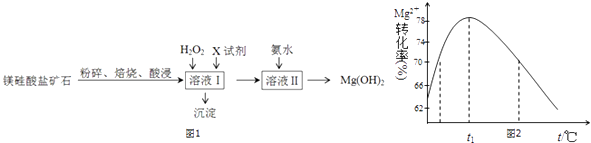
已知:几种金属阳离子的氢氧化物沉淀时的pH如下表所示:
Fe3+ | Al3+ | Fe2+ | Mg2+ | |
开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
(1)对矿石焙烧的目的是 .
(2)加入H2O2溶液反应的离子方程式是 .
(3)向溶液Ⅰ中加入的X可以是 , 作用是 .
(4)加入氨水时,Mg2+转化率随温度t的变化如图2所示: ①溶液Ⅱ中发生反应的离子方程式是 .
②t1前Mg2+转化率增大的原因是;
t1后Mg2+转化率下降的原因是(用化学方程式表示) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水中的溶解氧的含量是衡量水质的一个重要指标,某实验兴趣小组通过如下步骤来测量水中溶解氧的含量: 步骤一:向溶解氧测量瓶中注入20.00mL水样,再分别加入1mL 0.1molL﹣1MnSO4溶液和3mL NaOH和KI的混合溶液,充分反应.此时发生反应的化学方程式为:Mn2++2OH﹣═Mn(OH)2↓ 2Mn(OH)2+O2═2MnO(OH)2
步骤二:向上述混合物中加入1.5mL浓硫酸,充分反应后制沉淀完全溶解,此时溶液呈黄色.
步骤三:将溶液全部转移到容量瓶中,向其中滴加23滴淀粉溶液,溶液呈蓝色.用 0.005molL﹣1的Na2S2O3标准溶液滴定至蓝色恰好消失,共消耗Na2S2O3标准溶液3.60mL.此时发生反应为:I2+2Na2S2O3═2NaI+Na2S4O6
(1)25℃时,步骤一中当加入NaOH使溶液的pH=12时,此时溶液中的c(Mn2+)=molL﹣1 . (已知 KspMn(OH)2=2.06×10﹣13)
(2)写出步骤二中所发生反应的化学方程式:
(3)计算该水样中溶解氧的含量.(单位:mgL﹣1 , 请写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图分别是A,B两种物质的核磁共振氢谱,已知A,B两种物质都是烃类,都含有6个氢原子,试根据两种物质的核磁共振氢谱推测A,B有可能是下面的( ) 
A.A是C3H6 , B是C6H6
B.A是C2H6 , B是C3H6
C.A是C2H6 , B是C6H6
D.A是C3H6 , B是C2H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的方程式不正确的是( )
A.硫酸型酸雨的形成涉及反应:2H2SO3+O2 ![]() ?2H2SO4
?2H2SO4
B.SO2的水溶液显酸性:SO2+H2O?H2SO3?2H++SO32﹣
C.常温下,0.1mol/L醋酸溶液pH≈3:CH3COOH?CH3COO﹣+H+
D.Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s)?Mg2+(aq)+2OH﹣(aq),该固体可溶于NH4Cl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A | B | C | D |
钢闸门容易被腐蚀 | a、b均为惰性电极,b极反应是:O+4OH﹣﹣4e﹣=2H2O | 阴、阳两极生成的气体的物质的量之比是1:1 | 电池工作一段时间 |
|
|
|
|
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国成功研制出具有自主知识产权的治疗急性缺血性脑卒中的一类化学新药﹣丁苯酞(J),标志着我国在脑血管疾病治疗药物研究领域达到了国际先进水平.合成丁苯酞的一种路线如图所示. 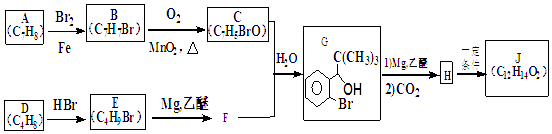
已知:① 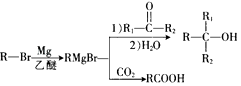
②C能发生银镜反应;
③J是一种酯,分子中除苯环外还含有一个五元环
回答下列问题:
(1)由A生成B的化学方程式为 , 其反应类型为
(2)C结构简式为
(3)下列说法正确的是
A.C能发生加成反应、聚合反应
B.D存在顺反异构
C.D的核磁共振氢谱有两个峰,且峰面积比为3:1
(4)J的结构简式为 , H在一定条件下还能生成高分子化合物K,H生成K的化学方程式为
(5)写出两种符合下列条件的G的同分异构体的结构简式 ①核磁共振氢谱有4组峰 ②能与FeCl3溶液发生显色反应
(6)参考题中信息和所学知识,写出由乙烯和化合物A合成邻甲基苯乙烯( 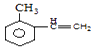 )的路线流程图(其他试剂任选)
)的路线流程图(其他试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳中含量(质量分数)最多的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X、Y的元素符号依次为 、 ;
(2)XZ2与YZ2分子的立体结构分别是 和 ;
(3)Q的元素符号是 ,它属于第 周期,它的核外电子排布式为 ,在形成化合物时它的最高化合价为 ;
(4)用氢键表示式写出E的氢化物溶液中存在的所有氢键 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中的甲图表示植物的淀粉酶与人的淀粉酶活性受pH影响的情况,乙图表示3种脱氢酶(A、B、C)的活性受温度影响的情况。下列叙述正确的是

①pH=5时,植物的淀粉酶的活性最高
②人的淀粉酶活性随pH的降低而渐渐升高
③乙图中,适宜温度范围最广的酶是B
④乙图中,无法确认C酶活性的最适温度
A.①② B.①③
C.①④ D.②
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com