
【题目】在强酸性无色透明溶液中,下列各组离子能大量共存的是( )
A.Fe3+、K+、Cl-、NO3-
B.Ag+、Na+、NO3-、Cl-
C.Zn2+、Al3+、SO42-、Cl-
D.Ba2+、NH4+、Cl-、HCO3-
科目:高中化学 来源: 题型:
【题目】(1)①根据图1所示,写出反应的热化学方程式______________________________。
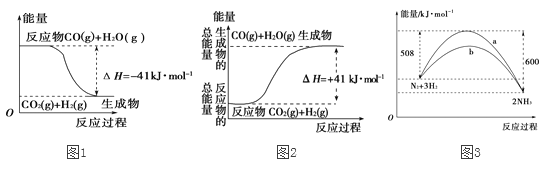
②根据图2所示情况,判断下列说法中正确的是 (____)
A.其热化学方程式为:CO(g)+H2O(g)===CO2(g)+H2(g) ΔH=+41kJ·mol-1
B.该反应为吸热反应
C.该反应为放热反应
D.当H2O为液态时,其反应热值小于41
(2)已知16 g固体硫完全燃烧时放出148.4 kJ的热量,该反应的热化学方程式是___________________。
(3)图3是某温度下,N2与H2反应过程中能量变化的曲线图。该反应的热化学方程式为:______________________________。a、b两条曲线分别代表生成由N2、H2合成氨的两个不同反应过程,其反应热△Ha ___△Hb(填“>”或“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过渡元素Ti、Mn、Fe、Cu等可与C、H、O形成多种化合物。请回答下列问题:
(1)根据元素原子的外围电子排布的特征,可将元素周期表分成五个区域,其中Mn属于________区。
(2)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。基态Ti2+中电子占据的最高能层符号为________,该能层具有的原子轨道数为________。BH![]() 的立体构型是________。
的立体构型是________。
(3)在Cu的催化作用下,乙醇可被空气中氧气氧化为乙醛,乙醛分子中碳原子的杂化方式是________,乙醛分子中HCO的键角________乙醇分子中HCO的键角(填“大于”、“等于”或“小于”)。
(4)电镀厂排放的废水中常含有剧毒的CN-,可在TiO2的催化下,先用NaClO将CN-氧化成CNO-,再在酸性条件下CNO-继续被NaClO氧化成N2和CO2。
①H、C、N、O四种元素的电负性由小到大的顺序为________________。
②与CN-互为等电子体微粒的化学式为________(写出一种即可)
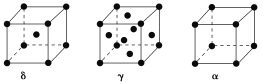
(5)单质铁有δ、γ、α三种同素异形体,三种晶胞中Fe原子的配位数之比为________,δ、γ、α三种晶胞的边长之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
A. 使用滴定管时,滴定管必须用待装液润洗2~3次
B. 滴定操作中,若用待测液润洗锥形瓶,将导致测定结果偏高
C. 用10 mL的量筒量取8.58 mL 0.10 mol·L-1的稀盐酸
D. 稀释浓硫酸时,将浓硫酸缓缓加入水中,并不断用玻璃棒搅拌
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. HClO2 →ClO2+Cl2+H2O(未配平), 1 mol HClO2分解时转移电子的物质的量为1 mol
B. 标准状况下,14 g CO、C2H4混合气体与11.2 L N2所含有的分子数都是0.5NA
C. 与金属Cu常温下反应放出气体的溶液可以存在的离子有:Fe2+、Al3+、SO42-、K+
D. 在燃煤时加入适量石灰石,可减少SO2的排放,其中发生的反应为2CaCO3+O2+2SO22CaSO3+2CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,不能达到预期目的是:
①苯、浓溴水、溴化铁混合制溴苯 ②苯酚浓溶液与稀溴水反应生成白色沉淀
③用溴水除去混在苯中的己烯,分液得到纯净的苯 ④乙醇和30%的硫酸共热到170℃制乙烯
A. ①②③④ B. ①②③ C. ①②④ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关反应原理的说法正确的是
A. 放热反应的反应速率总是大于吸热反应的反应速率
B. 化学反应速率越快可逆反应正向进行的程度越大
C. 纯银器表面在空气中因发生电化学腐蚀生成Ag2O而变暗
D. 应用盖斯定律可计算某些难以直接测量的反应的焓变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是部分短周期元素的单质及其化合物(或溶液)的转化关系,已知单质B2、C2、D2、E2在常温常压下都是气体,化合物G的焰色反应为黄色;化合物I、J、K通常状况下呈气态。下列说法正确的是

A. B氢化物的沸点高于其同主族其它元素氢化物的沸点
B. 原子半径大小:A>C>B>E>D
C. F中既含有离子键又含有极性共价键
D. G中的阴离子能抑制水的电离
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com