
【题目】25℃时,将浓度均为0 1mol·L-1、体积分别为V a和Vb的HA 溶液与BOH 溶液按不同体积比混合,保持Va+Vb=100mL,Va、Vb与混合液的pH 的关系如图所示。下列说法正确的是

A. a→c过程中水的电离程度始终增大
B. b点时,c(B+)=c(A+)=c(H+)=c(OH-)
C. c 点时, 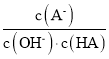 随温度升高而减小
随温度升高而减小
D. 相同温度下,Ka (HA)>Kb(BOH)
科目:高中化学 来源: 题型:
【题目】下来除杂方法不正确的是( )
物质 | 杂质 | 除杂试剂或方法 | |
A | Fe2(SO4)3 | FeSO4 | 通入 Cl2 |
B | FeSO4 | Fe2(SO4)3 | 加入铁粉 |
C | Na2CO3 | NaHCO3 | 加热 |
D | Mg | Al | NaOH溶液,过滤 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分,针对表中的①~⑩中元素,填写下列空格: 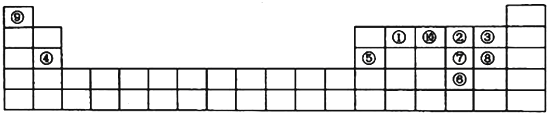
(1)在这10种元素中,非金属性最强的是(填序号);
(2)元素②⑧⑨以原子个数比1:1:1形成的化合物的结构式为 , 元素②与⑨形成的18e﹣化合物的电子式;
(3)②、⑨、⑩三种元素形成的化合物M中原子个数比为3:4:2,电子总数为42,M中含有的化学键类型有;
(4)比较元素⑦⑧形成的气态氢化物的稳定性:>(用化学式表示)
(5)元素⑤的氧化物与氢氧化钠溶液反应的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(NH4)2SO4是常见的化肥和化工原料,受热易分解.某兴趣小组拟探究其分解产物.
[查阅资料](NH4)2SO4在260℃和400℃时分解产物不同.
[实验探究]该小组拟选用下图所示装置进行实验(夹持和加热装置略)
实验1:连接装置A﹣B﹣C﹣D,检查气密性,按图示加入试剂(装置B盛0.5000mol/L盐酸70.00mL).通入N2排尽空气后,于260℃加热装置A一段时间,停止加热,冷却,停止通入N2 , 品红溶液不褪色.已知中和装置B中剩余盐酸需0.2000mol/L NaOH溶液25.00mL,且中和后的溶液中无SO42﹣ .
(1)仪器X的名称是;
(2)装置B内溶液吸收气体的物质的量是mol;
实验2:连接装置A﹣D﹣B,检查气密性,按图示重新加入试剂.通入N2排尽空气后,于400℃加热装置A至(NH4)2SO4完全分解无残留物,停止加热,冷却,停止通入N2 . 观察到装置A、D之间的导气管内有少量白色固体.经检验,该白色固体和装置D内溶液中有SO32﹣ , 无SO42﹣ . 进一步研究发现,气体产物中无氮氧化物.
(3)检验装置D内溶液中有SO32﹣ , 无SO42﹣的实验操作和现象是;
(4)装置B内溶液吸收的气体是;
(5)(NH4)2SO4在400℃分解的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列醛、酮的反应属于还原反应的是( )
A.醛的银镜反应
B.醛在空气中久置变质
C.由2-丁酮制备2-丁醇
D.乙醛与新制的氢氧化铜悬浊液加热有砖红色沉淀产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列将CH3CHO和CH3COOH分离的正确方法是( )
A.蒸馏
B.加入Na2CO3溶液后,通过萃取的方法分离
C.加入烧碱溶液后蒸馏出乙醛,再加入浓硫酸,蒸馏出乙酸
D.和Na反应后进行分离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
A. 11gT2O含有的电子数为5NA
B. 常温下,0.2L 0.5molL﹣1NH4NO3溶液的氮原子数小于0.2NA
C. 含4molHCl的浓盐酸与足量二氧化锰反应转移的电子总数为NA
D. 标准状况下,2.24L H2S全部溶于水所得溶液中HS﹣和S2﹣离子数之和为0.1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com