
分析 根据n=$\frac{V}{Vm}$计算混合气体的物质的量,令混合气体中CO和CO2的物质的量分别为xmol、ymol,根据二者质量之和与物质的量之和列放出计算x、y的值,再根据V=nVm计算CO的体积,根据m=nM计算CO2的质量.
解答 解:标准状况下,混合气体的物质的量为$\frac{22.4L}{22.4L/mol}$=1mol,
令混合气体中CO和CO2的物质的量分别为xmol、ymol,则:
x+y=1;
28x+44y=36
解得:x=0.5,y=0.5;
则CO所占的体积为:22.4L/mol×0.5mol=11.2L;
CO2的质量为:0.5mol×44g/mol=22g;
故答案为:11.2;22.
点评 本题考查物质的量的有关计算、混合物的有关计算等,比较基础,注意对基础知识的理解掌握,注意对公式的理解与运用.


科目:高中化学 来源: 题型:选择题
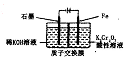 电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应Cr2O72-+6Fe2+l4H+═2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去,下列说法不正确的是( )
电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应Cr2O72-+6Fe2+l4H+═2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去,下列说法不正确的是( )| A. | 阳极反应为Fe-2e-=Fe2+ | |
| B. | 在阴极室,发生的电极反应为:Cr2O72-+6e-+7H2O=Cr(OH)3+8OH- | |
| C. | 在阳极室,pH增大会有Fe(OH)3沉淀生成 | |
| D. | 电路中每转移12 mol电子,最多有1 mol Cr2O72- 被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最高价氧化物对应水化物的碱性大小顺序一定是:X>Y | |
| B. | 离子半径和原子半径由大到小的顺序均为X>Y>Z>W | |
| C. | 氢化物的稳定性是Z<W | |
| D. | 还原性Z m->W(m+1)-,氧化性Xn+>Y(n+1)+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阿伏加德罗常数个硫酸分子里含有4molO | |
| B. | CH4的摩尔质量为16g | |
| C. | lmolFe的质量为56g/mol | |
| D. | lmolNH3为18g |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:丁>丙>乙>甲 | |
| B. | 乙元素在周期表中的位置为第三周期第Ⅳ族 | |
| C. | 1molA与足量B完全反应共转移1mol电子 | |
| D. | 1.0mol•L-1E溶液中阴离子总的物质的量小于0.1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3、Al(OH)3 | B. | AgCl、NaHCO3 | C. | NaHCO3、BaCO3 | D. | Na2SiO3、CuO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com