


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、2H2S+SO2→3S↓+2H2O |
| B、SO2+2Mg→2MgO+S |
| C、Cl2+SO2+2H2O→H2SO4+2HCl |
| D、SO2+2NaOH→Na2SO3+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4 mol/(L?s) |
| B、0.4 mol/(L?s) |
| C、2 mol/(L?s) |
| D、0.2 mol/(L?s) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCl中H-Cl键的极性和HF中H-F的极性 |
| B、乙烯CH2=CH2中碳碳σ键的键能和碳碳π键的键能 |
| C、1mol金刚石晶体中C-C键数目和1mol SiO2晶体Si-O键数目 |
| D、MgCl2晶体的熔点与AlCl3晶体的熔点 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将40 g NaOH溶解在1 L水中 |
| B、将200ml、2 mol?L-1HCl加水稀释配成2 L溶液 |
| C、将10 g NaOH溶解在少量水中,再加蒸馏水直到溶液体积为250 mL |
| D、将1 L 10 mol?L-1浓盐酸加入9 L水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X有三种同位素 |
| B、其中一种同位素的质量为80 |
| C、X2的平均相对分子质量为159 |
| D、质量数为79的同位素的原子百分数为50% |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
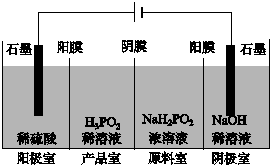 次磷酸(H3PO2)也是一种中强酸,具有强还原性,与足量NaOH反应生成NaH2PO2.H3PO2可用电渗析法制备,“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):
次磷酸(H3PO2)也是一种中强酸,具有强还原性,与足量NaOH反应生成NaH2PO2.H3PO2可用电渗析法制备,“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com