
����Ŀ����ҵ����������β���ŷų���SO2��NOx�ȣ����γ���������Ҫ���ء������ɿ����еĻҳ������ᡢ���ᡢ�л�̼�⻯����������γɵ�������
��1��NOx��SO2�ڿ����д�������ƽ�⣺2NO��g��+O2��g��2NO2��g����H=-113.0kJmol-1��2SO2��g��+O2��g��2SO3��g����H=-196.6kJmol-1��SO2ͨ���ڶ��������Ĵ����£���һ��������������SO3��
��д��NO2��SO2��Ӧ���Ȼ�ѧ����ʽΪ__��
�����¶����ߣ��÷�Ӧ��ѧƽ�ⳣ���仯������___��
��2�����2SO2+O22SO3��Ӧ��SO2��ת���ʣ��Ǽ���SO2�ŷŵ���Ч��ʩ��
��T�¶�ʱ����1L���ܱ������м���2.0molSO2��1.0molO2��5min��Ӧ�ﵽƽ�⣬���������ת����Ϊ50%���÷�Ӧ��ƽ�ⳣ����__��
���ڢ��������£���Ӧ�ﵽƽ��ı�������������ʹSO2��ת������ߵ���___������ĸ����
a.�¶Ⱥ�����������䣬����1.0molHe b.�¶Ⱥ�����������䣬����1.0molO2
c.��������������ʱ��������������� d.��������������ʱ�����ø�Ч����
e.��������������ʱ��������ϵ�¶�
���𰸡�NO2��g��+SO2��g��=SO3��g��+NO��g�� ��H=-41.8kJmol-1 ��С 2 bc
��������
(1) �� 2NO(g)+O2(g)![]() 2NO2(g) ��H=-113.0kJmol-1 ��
2NO2(g) ��H=-113.0kJmol-1 ��
2SO2(g)+O2(g)![]() 2SO3(g) ��H=-196.6kJmol-1 ��
2SO3(g) ��H=-196.6kJmol-1 ��
[��-��]/2�ã�SO2(g)+NO2(g)![]() NO(g)+SO3(g) ��H=-41.8kJmol-1
NO(g)+SO3(g) ��H=-41.8kJmol-1
����SO2(g)+NO2(g)![]() NO(g)+SO3(g) ��H=-41.8kJmol-1
NO(g)+SO3(g) ��H=-41.8kJmol-1
�ڸ÷�Ӧ������ӦΪ���ȷ�Ӧ���¶����ߣ�ƽ�������ƶ�����ѧƽ�ⳣ����С����Ϊ��С��
(2) �� 2SO2(g)+O2(g)![]() 2SO3(g)
2SO3(g)
��ʼ�� 2mol/L 1mol/L 0
�仯�� 1mol/L 0.5mol/L 1mol/L
ƽ���� 1mol/L 0.5mol/L 1mol/L
![]() ��Ϊ2
��Ϊ2
��a.�¶Ⱥ�����������䣬����1.0molHe����Ӧ�����������Ũ�Ȳ��䣬ƽ�ⲻ�ƶ������������ת���ʲ��䣻
b.�¶Ⱥ�����������䣬����1.0molO2�������˷�Ӧ��O2��Ũ�ȣ�ƽ�������ƶ������������ת��������
c.��������������ʱ������������������൱�ڼ�ѹ��ƽ�������ƶ������������ת��������
d.��������������ʱ�����ø�Ч�������Ի�ѧƽ�ⲻ����Ӱ�죬���������ת���ʲ��䣻
e.��������������ʱ��������ϵ�¶ȣ�ƽ�������ƶ������������ת���ʼ�С��
�ʴ�Ϊbc



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� NA ��ʾ�����ӵ�������ֵ������˵������ȷ����
A.��״���£�22.4L CCl4 ���е�ԭ����Ϊ 5NA
B.1.8g �� NH4+�к��еĵ�����Ϊ NA
C.���³�ѹ�£�32 g O2 �� O3 �Ļ������������ԭ����Ϊ 1.5 NA
D.7.1g Cl2 ����ˮ��ת�Ƶ�����ĿΪ 0.1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ![]() ��һ���ܱ������н��У����д�ʩ����ʹ��Ӧ����������ǣ� ��
��һ���ܱ������н��У����д�ʩ����ʹ��Ӧ����������ǣ� ��
����������![]() �������¶Ȣ�������䣬��ͨ��
�������¶Ȣ�������䣬��ͨ��![]() ����С�������ѹǿ��������䣬��ͨ��He��ѹǿ���䣬��ͨ��He
����С�������ѹǿ��������䣬��ͨ��He��ѹǿ���䣬��ͨ��He
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪij���Ҵ�ȼ�ϵ��ʾ��ͼ������ʱ������������ͼ��ʾ�������ж���ȷ����

A��X����
B���缫A��Ӧʽ��CH3CH2OH��12e��+3H2O=2CO2+12H+
C���缫���ϻ����ԣ�A��B
D��B�缫������ҺpH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2.32gNa2CO3��NaOH�Ĺ���������ȫ�ܽ���ˮ���Ƴ���Һ��Ȼ�������Һ����μ���1mol/L�����ᣬ�����������������CO2�����(��״��) ��ϵ��ͼ��ʾ������˵���д�����ǣ� ��
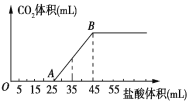
A.OA�η�����Ӧ�����ӷ���ʽΪ��H++OH-=H2O��CO32-+H+=HCO3-
B.A����Һ�е�����ΪNaCl��NaHCO3
C.�������NaOH������0.60g
D.������35mL����ʱ������CO2�����Ϊ224mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��WΪԭ��������������Ķ���������Ԫ�أ�Y��W������ϼ�֮��Ϊ8��X��Zͬ���壬��Z�ĺ˵������X��2��������˵����ȷ����( )
A.����̬�⻯����ȶ��ԣ�X>ZB.�����Ӱ뾶��![]()
C.��X��Y��ɵĻ������в������ۼ�D.����������Ӧˮ��������ԣ�Z>W
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧͨ������װ�òⶨM��Ʒ��ֻ��Fe��Al��Cu���и��ɷֵ�����������ȡ����������Ϊm g��M��Ʒ����ʵ��1����ͼ1����ʵ��2����ͼ2������ʵ�飬��ͬѧ˳�������ʵ�鲢�����������ֱ�ΪV1 mL��V2 mL�������㵽��״���£���
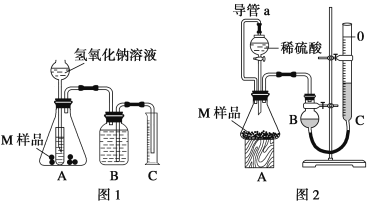
��1��д��ʵ��1�п��ܷ�����Ӧ�����ӷ���ʽ��____________��
��2����ʵ����Ҫ0.50 mol��L��1��NaOH��Һ480 mL����ش��������⣺
������ʱӦ��������ƽ����______g NaOH��Ӧѡ��________ ml����ƿ��
������NaOH��Һʱ��NaOH�����к���Na2O���ʻᵼ��������ҺŨ��________��������ƫ��������ƫС��������Ӱ��������
��3����ʵ��������ϡ��������98%��Ũ���ᣨ��=1.84g/cm3�����Ƶģ����Ũ��������ʵ���Ũ����_______��
��4������ʵ��2������ʱ��ȴ�����³�����ƽ���⣬��Ӧ���еIJ����ǣ� ___________��
��5��ʵ��2�е���a������_________��
��6��M��Ʒ��ͭ����������ѧ����ʽΪ����V1��V2 ��ʾ����_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ӣ��ṹ��ʽ��ͼ��ʾ�����׳�ʯ̿�ᡣ��һ����Ҫ�Ļ���ԭ�ϣ��㷺�������ʷ�ȩ��֬��Ⱦ�ϡ�ҽҩ��ũҩ�ȡ�����˵������ȷ���ǣ� ��
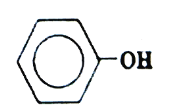
A.����������ԭ�ӿ��ܹ�ƽ��
B.���屽�ӷ��Ӽ�����γ����
C.![]() �÷��ӳ��ȼ�գ�������
�÷��ӳ��ȼ�գ�������![]()
D.![]() �÷����������������ӳɺ��ϵ�һ��ȡ������3��
�÷����������������ӳɺ��ϵ�һ��ȡ������3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2L���ܱ�������,�������·�Ӧ:2A(g)+ B(g) ![]() 2C(g)+D(g) ������������A��B����4 mol����ǰ10����A��ƽ����Ӧ�ٶ�Ϊ0.12 mol/��L������10����ʱ��������B�����ʵ������� ��
2C(g)+D(g) ������������A��B����4 mol����ǰ10����A��ƽ����Ӧ�ٶ�Ϊ0.12 mol/��L������10����ʱ��������B�����ʵ������� ��
A. 1.6 mol B. 2.8 mol
C. 2.4 mol D. 1.2 mol
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com