
| A、已知MgCO3的Ksp=6.82×10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)?c(CO32-)=6.82×10-6 | ||||
B、已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为α,Ka=
| ||||
| C、常温下,在0.10 mol?L-1的NH3?H2O溶液中加入少量NH4Cl晶体,能使NH3?H2O的电离程度减弱,溶液的pH减小 | ||||
D、室温时,M(OH)2(s)?M2+(aq)+2OH-(aq) Ksp=a c(M2+)=b mol?L-1时,溶液的pH等于14+
|


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:
| A、在同温同压时,相同体积的任何气体单质所含的原子数目相同 |
| B、NA个Fe(OH)3胶体粒子的质量为107g |
| C、标准状况下,22.4 LCO2和O2混合气体中含有的氧气分子数数为NA |
| D、常温常压下17g氨气所含电子数目为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑤⑥ | B、②④⑥ |
| C、②③④⑦ | D、①⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、两种元素组成的分子中一定只有极性键 |
| B、含有阴离子的化合物一定含有阳离子 |
| C、干冰升华时,分子内共价键会发生断裂 |
| D、金属元素和非金属元素形成的化合物一定是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AlCl3溶液中加入过量的浓氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| B、用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+=Cu2++2Fe2+ |
| C、大理石溶于醋酸中的反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
| D、钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解时以精铜作阴极 |
| B、电解时阴极发生还原反应 |
| C、粗铜连接电源负极,其电极反应有:Cu-2e-=Cu2+、Fe-2e-=Fe2+、Zn-2e-=Zn2+ |
| D、电解后,电解槽底部会形成含少量Ag、Pt等金属的阳极泥 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、150.0mL 1.0 mol/L NaCl溶液 |
| B、75.0mL 2.0 mol/L MgCl2溶液 |
| C、150.0mL 2.0 mol/LKCl溶液 |
| D、75.0 mL 1.0 mol/L A1C13溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCO3-+OH-=H2O+CO32- |
| B、NH3+H+=NH4+ |
| C、NH3?H2O?NH4++OH- |
| D、HCO3-+H2O?H2CO3+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
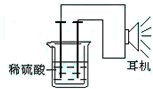 利用生活中或实验室中常用的物品,根据氧化还原反应知识和电学知识,自己动手设计一个原电池.请填写下列空白:
利用生活中或实验室中常用的物品,根据氧化还原反应知识和电学知识,自己动手设计一个原电池.请填写下列空白:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com