
【题目】具有手性碳原子的物质常具有光学活性。有机物A :CH3COOCH2—![]() 具有光学活性。但当A发生了下列一系列变化后,可能会失去光学活性。①与金属钠反应;②让酯在稀硫酸作用下水解;③在铜做催化剂的条件下与氧气催化氧化;④与乙酸发生酯化反应;⑤与浓硫酸共热发生消去反应;你认为能使A失去光学活性的一组是 ( )
具有光学活性。但当A发生了下列一系列变化后,可能会失去光学活性。①与金属钠反应;②让酯在稀硫酸作用下水解;③在铜做催化剂的条件下与氧气催化氧化;④与乙酸发生酯化反应;⑤与浓硫酸共热发生消去反应;你认为能使A失去光学活性的一组是 ( )
A. ①③④ B. ①②③④ C. ②③④⑤ D. ①③④⑤
科目:高中化学 来源: 题型:
【题目】已知 :2SO2(g)+ O2(g)![]() 2SO3(g) △H= -QkJ/mol,在温度一定、容积为2L的密闭容器中分别进行下列三个实验:充分作用后,测得实验1反应放出的热量为Q1kJ,实验2没有热量变化,则下列说法中不正确的是( )
2SO3(g) △H= -QkJ/mol,在温度一定、容积为2L的密闭容器中分别进行下列三个实验:充分作用后,测得实验1反应放出的热量为Q1kJ,实验2没有热量变化,则下列说法中不正确的是( )
实验编号 | SO2(g) | O2(g) | SO3(g) |
1. | 2mol | 1mol | 0mol |
2. | 1mol | 0.5mol | 1mol |
3. | 1mol | 0.8mol | 1.4mol |
A. 实验1放出的热量值为Q1=0.5Q B. 该条件下的平衡常数为4
C. 实验1中O2的转化率为50% D. 实验3反应放出热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学反应原理知识研究如何利用CO、SO2等污染物有重要意义。
(1)用CO可以合成甲醇。已知:
①CH3OH(g)+3/2O2(g)![]() CO2(g)+2H2O(l) ΔH=-764.5 kJ·mol-1
CO2(g)+2H2O(l) ΔH=-764.5 kJ·mol-1
②CO(g)+1/2O2(g)![]() CO2(g) ΔH=-283.0 kJ·mol-1
CO2(g) ΔH=-283.0 kJ·mol-1
③H2(g)+1/2O2(g)![]() H2O(l) ΔH=-285.8 kJ·mol-1
H2O(l) ΔH=-285.8 kJ·mol-1
则CO(g)+2H2 (g)![]() CH3OH(g) ΔH=________ kJ·mol-1。
CH3OH(g) ΔH=________ kJ·mol-1。
(2)下列措施中能够增大上述合成甲醇反应的反应速率的是________(填写序号)。
a. 使用高效催化剂 b. 降低反应温度
c. 增大体系压强 d. 不断将CH3OH从反应混合物中分离出来
(3)在一定压强下,容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示。

①p1________p2(填“大于”、“小于”或“等于”);
②100 ℃时,该反应的化学平衡常数K=_______;
③100℃时,达到平衡后,保持压强P1不变的情况下,再向容器中通入CO、H2和CH3OH各0.5a mol,则平衡_______ (填“向右”、“向左”或“不”移动)。
④在其它条件不变的情况下,再增加a mol CO和2a molH2,达到新平衡时,CO的转化率________(填“增大”、“减小”或“不变”)。
(4)在容积均为1L的密闭容器(a、b、c、d、e)中,分别充入1molCO和2molH2等量混合气体,在不同的温度下(温度分别为T1、T2、T3、T4、T5),经相同的时间,在t时刻,测得容器甲醇的体积分数如图所示。在T1- T2及T4- T5两个温度区间,容器内甲醇的体积分数的变化趋势如图所示,其原因是_______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】解释下列事实所用的方程式不合理的是
A. 硫酸酸化的KI淀粉溶液久置后变蓝:4I-+O2 +4H+=2I2+2H2O
B. 将充有NO2的玻璃球浸到热水中,气体颜色加深:2NO2(g)![]() N2O4(g) △H>0
N2O4(g) △H>0
C. 用Na2CO3溶液处理锅炉水垢中的硫酸钙:CO32- +CaSO4 =CaCO3 +SO42-
D. 以KOH溶液为电解质溶液,氢氧燃料电池的负极区pH减小:H2+2OH--2e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. 金刚石和石墨均为碳的同素异形体,它们燃烧时,若氧气不足生成一氧化碳,若充分燃烧生成二氧化碳,反应中放出的热量如图所示。
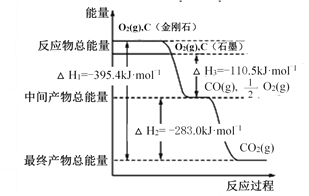
(1)等质量的金刚石和石墨完全燃烧,___________(填“金刚石”或 “石墨”)放出的热量更多,写出表示石墨燃烧热的热化学方程式:______________________________________。
(2)在通常状况下,__________________(填“金刚石”或“石墨”)更稳定,写出石墨转化为金刚石的热化学方程式:__________。
(3)12 g石墨在一定量空气中燃烧,生成气体 36 g,该过程中放出的热量为_______ 。
II. 某反应由两步反应 A、B、C 构成,它的反应能量曲线如图所示(E1、E2、E3、E4 表示活化能)。回答下列问题。

(1)A→B 过程中的 ΔH______________(填“<”或“>”)0。
(2)加入催化剂_____________________(填“能”或“不能”)改变反应的焓变。
(3)整个反应中 ΔH=_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按如图装置进行实验,下列推断正确的是( )
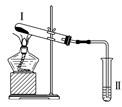
选项 | Ⅰ中试剂 | Ⅱ中试剂及现象 | 推断 |
A | 氯化铵 | 酚酞溶液不变红色 | 氯化铵稳定 |
B | 硫酸亚铁 | 品红溶液褪色 | FeSO4分解生成FeO和SO2 |
C | 涂有石蜡油的碎瓷片 | 酸性高锰酸钾溶液褪色 | 石蜡油发生了化学变化 |
D | 铁粉与水蒸气 | 肥皂水冒泡 | 铁粉与水蒸气发生了反应 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸钠(![]() ,缩写为NaA)可用作饮料的防腐剂。研究表明苯甲酸(HA)的抑菌能力显著高于A–。已知25 ℃时,HA的Ka=6.25×10–5,H2CO3的Ka1=4.17×10–7,Ka2=4.90×10–11。在生产碳酸饮料的过程中,除了添加NaA外,还需加压充入CO2气体。下列说法正确的是(温度为25 ℃,不考虑饮料中其他成分)( )
,缩写为NaA)可用作饮料的防腐剂。研究表明苯甲酸(HA)的抑菌能力显著高于A–。已知25 ℃时,HA的Ka=6.25×10–5,H2CO3的Ka1=4.17×10–7,Ka2=4.90×10–11。在生产碳酸饮料的过程中,除了添加NaA外,还需加压充入CO2气体。下列说法正确的是(温度为25 ℃,不考虑饮料中其他成分)( )
A. 相比于未充CO2的饮料,碳酸饮料的抑菌能力较低
B. 当pH为5.0时,饮料中c(HA) /c(A–)=0.16
C. 提高CO2充气压力,饮料中c(A–)不变
D. 碳酸饮料中各种粒子的浓度关系为:c(H+)=c(HCO3-)+c(CO32-)+c(OH–)–c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,在 2 L 的密闭容器中,气体 X、Y 和 Z 三种物质的物质的量随时间变化的曲线如图所示,下列描述正确的是
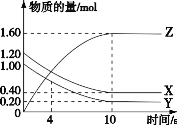
A. 容器中化学反应为 X(g)+Y(g)![]() Z(g)
Z(g)
B. 0~10 s,X 表示的平均化学反应速率为 0.04 mol/(L·s)
C. 使用催化剂只能加快 0~10 s 间的反应速率
D. 0~4 s 的平均反应速率小于 0~10 s 的平均反应速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com