
【题目】T℃时,在 2 L 的密闭容器中,气体 X、Y 和 Z 三种物质的物质的量随时间变化的曲线如图所示,下列描述正确的是
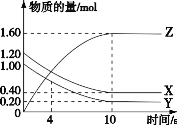
A. 容器中化学反应为 X(g)+Y(g)![]() Z(g)
Z(g)
B. 0~10 s,X 表示的平均化学反应速率为 0.04 mol/(L·s)
C. 使用催化剂只能加快 0~10 s 间的反应速率
D. 0~4 s 的平均反应速率小于 0~10 s 的平均反应速率
科目:高中化学 来源: 题型:
【题目】具有手性碳原子的物质常具有光学活性。有机物A :CH3COOCH2—![]() 具有光学活性。但当A发生了下列一系列变化后,可能会失去光学活性。①与金属钠反应;②让酯在稀硫酸作用下水解;③在铜做催化剂的条件下与氧气催化氧化;④与乙酸发生酯化反应;⑤与浓硫酸共热发生消去反应;你认为能使A失去光学活性的一组是 ( )
具有光学活性。但当A发生了下列一系列变化后,可能会失去光学活性。①与金属钠反应;②让酯在稀硫酸作用下水解;③在铜做催化剂的条件下与氧气催化氧化;④与乙酸发生酯化反应;⑤与浓硫酸共热发生消去反应;你认为能使A失去光学活性的一组是 ( )
A. ①③④ B. ①②③④ C. ②③④⑤ D. ①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】控制变量是科学研究的重要方法。相同质量的铁粉与足量稀硫酸分别在下列条件下发生反应,其中反应速率最快的是
A | B | C | D | |
t/℃ | 10 | 10 | 40 | 40 |
c(H2SO4 )/(mol/L) | 1 | 3 | 1 | 3 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G均为有机物,其中A 常用来衡量一个国家石油化工发展水平的标志性物质,它们之间有如下转化关系。
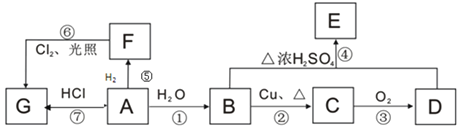
请回答下列问题:
(1)B、D中官能团的名称:B_____D_______
(2)指出下列编号对应反应的反应类型:
①_________ ⑥_______
(3)在F的同系物中最简单的有机物的空间构型为____,电子为______。
(4)H与A互为同系物,H分子中共有24个电子,写出H的结构简式:_______
(5)写出下列编号对应反应的化学反应方程式:
②____________________; ④_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸镁Mg(ClO3)2常用作催熟剂、除草剂等,实验室制备少量Mg(ClO3)2·6H2O的流程如下:
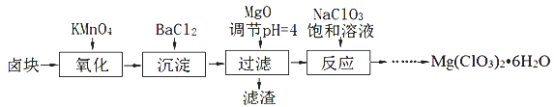
已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
②四种化合物的溶解度(S)随温度 (T)变化曲线如图所示。
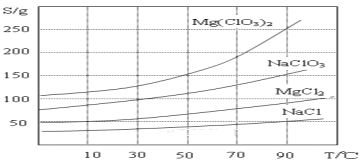
(1)过滤所需要的主要玻璃仪器有____________。
(2)加入BaCl2的目的是___________,加MgO后过滤所得滤渣的主要成分为____________。
(3)加入NaClO3饱和溶液后发生反应的化学方程式为____________。
(4)再进一步制取Mg(ClO3)2·6H2O的实验步骤依次为____________:
①蒸发结晶;②趁热过滤、洗涤;③将滤液冷却结晶;④过滤、洗涤。
(5)产品中Mg(ClO3)2·6H2O含量的测定(已知Mg(ClO3)2·6H2O的摩尔质量为299g/mol )
步骤1:准确称量3.50 g产品配成100 mL溶液。
步骤2:取10.00mL溶液于锥形瓶中,加入10.00mL稀硫酸和20.00mL1.000 mol·L-1的FeSO4溶液,微热。
步骤3:冷却至室温,用0.100 mol/L K2Cr2O7溶液滴定剩余的Fe2+至终点。
①此反应的离子方程式为:_____________________________________________。
步骤4:将步骤2、3重复两次,平均消耗K2Cr2O7溶液15.00 mL。
②产品中Mg(ClO3)2·6H2O的质量分数_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生下列反应 aA(g)![]() cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D 的浓度为原平衡的 1.75 倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D 的浓度为原平衡的 1.75 倍,下列叙述正确的是
A. A 的转化率变大 B. 平衡向正反应方向移动
C. D 的体积分数变大 D. a < c+d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:


按以下合成步骤回答问题:
(1)在a中加入15 mL苯和少量铁屑。在b中小心加入4.0 mL 液溴。再将b中液溴慢慢加入到a中,充分反应。装置a中发生的主要反应是_____________________________;装置d的作用是________________。
(2)反应过程中,a外壁温度升高,为提高原料利用率,采取以下措施:
①采用装置c进行冷凝回流,回流的主要物质有__________。
②利用温度计控制温度,适宜的温度范围为(填序号)__________。
A.>156℃ B. 59℃-80℃ C.<59℃
(3)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用10 mL水、8 mL10%的NaOH溶液、10 mL水洗涤。
此操作所需要的玻璃仪器除烧杯外,还需___________,用NaOH溶液洗涤的作用是__________;
③向分离出的粗溴苯中加入少量的无水氯化钙,静置、过滤。
(4)经过上述分离操作后,粗溴苯中还含有的主要杂质为__________,要进一步提纯,下列操作中必须的是_________(填入正确选项前的字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com