
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:


按以下合成步骤回答问题:
(1)在a中加入15 mL苯和少量铁屑。在b中小心加入4.0 mL 液溴。再将b中液溴慢慢加入到a中,充分反应。装置a中发生的主要反应是_____________________________;装置d的作用是________________。
(2)反应过程中,a外壁温度升高,为提高原料利用率,采取以下措施:
①采用装置c进行冷凝回流,回流的主要物质有__________。
②利用温度计控制温度,适宜的温度范围为(填序号)__________。
A.>156℃ B. 59℃-80℃ C.<59℃
(3)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用10 mL水、8 mL10%的NaOH溶液、10 mL水洗涤。
此操作所需要的玻璃仪器除烧杯外,还需___________,用NaOH溶液洗涤的作用是__________;
③向分离出的粗溴苯中加入少量的无水氯化钙,静置、过滤。
(4)经过上述分离操作后,粗溴苯中还含有的主要杂质为__________,要进一步提纯,下列操作中必须的是_________(填入正确选项前的字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
【答案】C6H6 +Br2![]() C6H5Br + HBr吸收HBr和Br2,防止倒吸C6H6 、Br2C分液漏斗除去未反应的Br2苯C
C6H5Br + HBr吸收HBr和Br2,防止倒吸C6H6 、Br2C分液漏斗除去未反应的Br2苯C
【解析】
(1)实验室合成溴苯是苯和液溴在铁粉做催化剂条件下发生的取代反应生成溴苯和溴化氢,溴化氢和液溴容易挥发,而苯的卤代反应是放热的,尾气中的溴化氢和溴用氢氧化钠溶液吸收,防止污染。(2)苯和溴的反应是放热的,为了减少反应物的挥发提高原料的利用率,需要将苯和溴冷凝回流。最后得到的溴苯中含有溴,用氢氧化钠反应除去。(3)溴苯中的苯利用沸点不同进行分离。
(1)苯和溴反应生成溴苯和溴化氢,方程式为:C6H6 +Br2![]() C6H5Br + HBr;溴化氢和液溴容易挥发,而反应放热,尾气中有溴化氢和溴,用氢氧化钠溶液吸收,防止污染大气,使用倒置漏斗可以防止倒吸; (2) ①反应过程中放热,会使苯和溴变成气体,为减少反应物挥发并提高原料的利用率,将苯和液溴冷凝回流。②根据表中的苯和溴的沸点,选择控制温度,确保温度在两种反应物的沸点之下,所以控制温度要低于59℃,故选C。(3) 液溴滴完后,经过下列步骤分离提纯:①向a中加入10 mL水,把可溶物溶解在水中,然后过滤除去未反应的铁屑;②滤液依次用10 mL水,8 mL10%的NaOH溶液把未反应的溴变成溴化钠和次溴酸钠,二者溶于水中,再用10 mL水洗涤,目的是洗去氢氧化钠,溴苯的密度大于水,且二者不互溶,所以用分液的方法分离,使用分液漏斗。(4). 经过分液后得到的有机物层主要为溴苯和苯,苯和溴苯利用沸点不同,苯的沸点低用蒸馏的方法分离。
C6H5Br + HBr;溴化氢和液溴容易挥发,而反应放热,尾气中有溴化氢和溴,用氢氧化钠溶液吸收,防止污染大气,使用倒置漏斗可以防止倒吸; (2) ①反应过程中放热,会使苯和溴变成气体,为减少反应物挥发并提高原料的利用率,将苯和液溴冷凝回流。②根据表中的苯和溴的沸点,选择控制温度,确保温度在两种反应物的沸点之下,所以控制温度要低于59℃,故选C。(3) 液溴滴完后,经过下列步骤分离提纯:①向a中加入10 mL水,把可溶物溶解在水中,然后过滤除去未反应的铁屑;②滤液依次用10 mL水,8 mL10%的NaOH溶液把未反应的溴变成溴化钠和次溴酸钠,二者溶于水中,再用10 mL水洗涤,目的是洗去氢氧化钠,溴苯的密度大于水,且二者不互溶,所以用分液的方法分离,使用分液漏斗。(4). 经过分液后得到的有机物层主要为溴苯和苯,苯和溴苯利用沸点不同,苯的沸点低用蒸馏的方法分离。


科目:高中化学 来源: 题型:
【题目】T℃时,在 2 L 的密闭容器中,气体 X、Y 和 Z 三种物质的物质的量随时间变化的曲线如图所示,下列描述正确的是
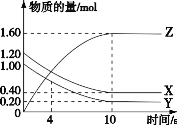
A. 容器中化学反应为 X(g)+Y(g)![]() Z(g)
Z(g)
B. 0~10 s,X 表示的平均化学反应速率为 0.04 mol/(L·s)
C. 使用催化剂只能加快 0~10 s 间的反应速率
D. 0~4 s 的平均反应速率小于 0~10 s 的平均反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D均为中学化学常见的纯净物,A是单质,它们有如图反应关系。下列说法错误的是( )

A.若A是大气中含量最多的气体,C、D是氧化物且会造成光化学污染。则D转化成C的反应化学方程为3NO2+H2O=2HNO3+2NO
B.若A、B、C分别为C(s)、CO(g)和CO2(g),且通过与O2(g)反应实现图示的转化。在同温同压且消耗含碳物质均为1mol时,反应①、②、③的焓变依次为△H 1、△H 2、△H 3,则它们之间的关系为 △H 2=△H 1+△H 3
C.若C为一元强碱且阴、阳离子所含的电子数相同,D为日常生活中常用的调味品,工业上用D制备A的化学方程式2Na2O(熔融)![]() 4Na+O2↑
4Na+O2↑
D.若A是应用最广泛的金属。④反应用到A,②、⑤反应均用到同一种气态非金属单质实验室保存D溶液的方法是加入适量铁粉与适量盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃分子中若含有双键,叁键或环,其碳原子所结合的氢原子则少于同碳原子数对应烷烃所含的氢原子数,亦具有一定的不饱和度(用W表示)。下表列出几种烃的不饱和度:
有机物 | 乙烯 | 乙炔 | 环己烷 | 苯 |
W | 1 | 2 | 1 | 4 |
据此下列说法不正确的是
A. 1molW=3的不饱和链烃再结合6molH即达到饱和
B. ![]() 的W等于6
的W等于6
C. CH3CH2CH=CH2与环丁烷的不饱和度相同
D. C4H8的不饱和度与C3H6、C2H4的不饱和度不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.中国传统文化是人类文明的瑰宝,古代文献中记载了大量古代化学的研究成果。回答下面问题:
(1)我国最原始的陶瓷约出现在距今12000年前,制作瓷器所用的原料是高岭士,其晶体化学式是Al4[Si4O10](OH)8,用氧化物表示其组成为______________。
(2)《本草纲目》中记载:“(火药)乃焰消( KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者。”反应原理为:S+2KNO3+3C![]() K2S+N2↑+3CO2↑,该反应的氧化剂是____ ,反应转移4mol电子时,被S氧化的C有____mol。
K2S+N2↑+3CO2↑,该反应的氧化剂是____ ,反应转移4mol电子时,被S氧化的C有____mol。
(3)我国古代中药学著作《新修本草》记载的药物有844种,其中有关“青矾”的描述为:“本来绿色,新出窟未见风者,正如瑁璃…烧之赤色…。”我国早期科技丛书《物理小适-金石类》 记载有加热青矾时的景象:“青矾厂气熏人,衣服当之易烂,载木不盛。”青矾就是绿矾( FeSO4·7H2O)。根据以上信息,写出“青矾”受热分解的化学方程式_________________。
Ⅱ.“钢是虎,钒是翼,钢含钒犹如虎添翼”,钒是“现代工业的味精”。钒对稀酸是稳定的,但室温下能溶解于浓硝酸中生成VO2+。
(4)请写出金属钒与浓硝酸反应的离子方程式:_______________________________。
(5)V2O5是两性氧化物,与强碱反应生成钒酸盐(阴离子为VO43-),溶于强酸生成含钒氧离子(VO2+)的盐。请写出V2O5分别与烧碱溶液和稀硫酸反应生成的盐的化学式:_____________、 _____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应能设计成原电池的是( )
A.CaCO3+2HCl═CaCl2+H2O+CO2↑B.BaCl2+Na2SO4═2NaCl+BaSO4↓
C.2NaOH+CO2═Na2CO3+H2OD.Fe+CuCl2═FeCl2+Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)已知某反应中能量变化如图所示,所得结论错误的是( )

A. 该图像可以表示氯化铵与消石灰反应的能量变化
B. 该反应过程中,一定有其他形式的能量转化成化学能
C. 该反应过程中,形成新化学键释放的总能量小于断裂旧化学键吸收的总能量
D. 因为生成物的总能量高于反应物的总能量,所以该反应一定需要加热才可进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素A、B、C、D、E的原子序数依次增大。A和C同族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成离子化合物,其阴阳离子个数比为1∶1。回答下列问题:
(1)五种元素中非金属性最强的是_______________(填元素符号)。
(2)由A和B、D、E所形成的共价化合物中,热稳定性最差的是___________(用化学式表示)。
(3)C和E形成的离子化合物的电子式为 ______ ,用电子式表示A和B形成的过程_____,A和E形成的化合物与A和B形成的化合物反应,产物的化学式为_______________
(4)D的最高价氧化物的水化物的化学式为____________________。
(5)由A和B形成的一种气体在工业上用途很广,实验室制取的方程式为____________________。
(6)单质E与水反应的离子方程式为____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com