
某小组同学利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”。实验时,先分别量取两种溶液,倒入大试管中迅速振荡混合均匀,再加入硫酸,开始计时,通过测定混合溶液褪色所需时间来判断反应的快慢(已知反应方程式为:5H2C2O4+2KMnO4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O)。该小组设计了如下方案。
| 编号 | H2C2O4溶液 | KMnO4溶液 | 硫酸溶液 | 温度/℃ | ||
| 浓度 (mol/L) | 体积 (mL) | 浓度 (mol/L) | 体积 (mL) | |||
| ① | 0.10 | 2.0 | 0.010 | 4.0 | 4mL 4mol/L | 25 |
| ② | 0.20 | 2.0 | 0.010 | 4.0 | 4mL 4mol/L | 25 |
| ③ | 0.20 | 2.0 | 0.010 | 4.0 | 4mL 4mol/L | 50 |
(1)探究温度对化学反应速率影响的组合实验编号是__________(填编号,下同);探究反应物浓度对化学反应速率影响的组合实验编号是__________。
(2)该小组同学由此实验发现反应进行一些时间后,有一时间段反应速率不断加快。同学们分析除了反应放热使体系温度升高外,可能还有其它原因,他们联想到教材上的科学探究实验,推断出反应混合溶液中的__________(填化学式)也加速了此反应的进行。
(3)上述实验①中充分反应后H2C2O4过量,假设理论上能通过用酸性KMnO4溶液滴定的方法来测定反应混合液中过量的H2C2O4,请回答下列问题:
①取用反应混合液的滴定管用__________滴定管(填“酸式”或“碱式”,下同),盛装KMnO4溶液的滴定管用__________滴定管。
②下列操作中可能使测出的H2C2O4剩余量比理论值偏低的是__________。
A. 读取酸性KMnO4溶液体积时,开始仰视读数,滴定结束时俯视读数
B. 滴定前盛放反应混合液的锥形瓶用蒸馏水洗净但没有干燥
C. 盛装KMnO4溶液的滴定管滴定前有气泡,滴定后气泡消失
D. 盛装KMnO4溶液的滴定管未润洗就直接注入酸性KMnO4溶液
③此滴定实验是否需要滴加指示剂________(填“是”或“否”);怎么确定此滴定的终点:_________。
【答案】(1)②③ ;①② ;(2)MnSO4 (3)①酸式 酸式 ②A
③否 ;当加入最后一滴酸性KMnO4溶液时,锥形瓶内溶液由无色变为浅紫色,且30s内不褪色。
【解析】
试题分析:(1)对表格中的数据进行观察得知:探究温度对化学反应速率影响的组合实验编号是②③;探究反应物浓度对化学反应速率影响的组合实验编号是①②;(2)由于在反应过程中产生了MnSO4,因此可推断出反应混合溶液中的MnSO4也加速了此反应的进行。(3)①由于反应后溶液中H2C2O4过量,即溶液显酸性,所以取用反应酸性混合液的滴定管用酸式滴定管;②A. 读取酸性KMnO4溶液体积时,开始仰视读数,滴定结束时俯视读数,则读数偏小,使测出的H2C2O4剩余量比理论值偏低,正确;B. 滴定前盛放反应混合液的锥形瓶用蒸馏水洗净但没有干燥,不能产生任何误差,错误;C. 盛装KMnO4溶液的滴定管滴定前有气泡,滴定后气泡消失,则消耗的KMnO4溶液体积偏大,因此使测出的H2C2O4剩余量比理论值偏高;错误;D. 盛装KMnO4溶液的滴定管未润洗就直接注入酸性KMnO4溶液,则消耗的标准KMnO4溶液体积偏大,因此使测出的H2C2O4剩余量比理论值偏高;错误。③由于KMnO4溶液是紫色的,当与草酸反应后产物是无色的,因此就可以利用其本身的颜色变化来显示滴定终点,故此滴定实验不需要滴加指示剂;滴定的终点的判断方法是当加入最后一滴酸性KMnO4溶液时,锥形瓶内溶液由无色变为浅紫色,且30s内不褪色。就达到了滴定终点。
考点:考查外界条件对化学反应速率的影响、滴定法在测定物质的组合、指示剂的选择、滴定终点的判断。


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案科目:高中化学 来源: 题型:
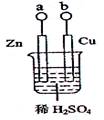
某小组为研究电化学原理,设计如右图装置,下列叙述不正确的是
A.a、b不连接时,只有锌片上有气泡逸出
B.a和b用导线连接时,铜片上发生的反应为:2H+ + 2e-= H2↑
C.a和b用导线连接或接直流电源,锌片都能溶解
D.a和b是否用导线连接,装置中所涉及的化学反应都相同
查看答案和解析>>
科目:高中化学 来源: 题型:
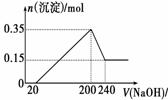 将一定质量的镁铝混合物投入200 mL硫酸中,固体全部溶解后,向所得溶液中加入5 mol/L的NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V(ml)的变化如图所示,
将一定质量的镁铝混合物投入200 mL硫酸中,固体全部溶解后,向所得溶液中加入5 mol/L的NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V(ml)的变化如图所示,
按要求填写:(1)镁和铝的总质量为 g。
(2)最初20 mL NaOH溶液的作用是 。
(3)硫酸的物质的量浓度为 。
(4)生成的氢气在标准状况下的体积为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关叙述中,不可以用氢键来解释的是
A.0℃时,水的密度大于冰的密度 B.水的熔沸点高于硫化氢的熔沸点
C.氟化氢气体极易溶于水 D.氟化氢比氯化氢稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
化学反应的快慢和限度对人类生产生活有重要的意义。
(1)请将影响表中“实例”反应速率的“条件”仿照示例填在空格横线上。
| 实例 | 影响条件 |
| ①食物放在冰箱里能延长保质期 | 温度(示例) |
| ②实验室将块状药品研细,再进行反应 | ____________ |
| ③用H2O2分解制O2时,加入MnO2 | ____________ |
| ④工业制硫酸催化氧化SO2制取SO3时,通入过量的空气 | ____________ |
(2)一定温度下,在2L体积不变的密闭容器中,X、Y、Z三种气体物质的量随时间变化的曲线如图所示:
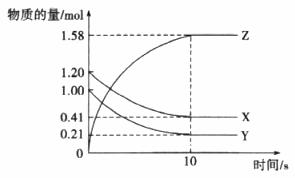
①写出该反应的化学方程式__________。
②从反应开始到10 s,用Z表示的反应速率为__________mol/(L·s)。
③该反应的化学平衡常数为__________(结果保留整数)。
④当反应进行到15 s时,向密闭容器中通入氩气,此时用Z表示的反应速率__________(填“小于”或“等于”或“大于”)10 s时用Z表示的反应速率。
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数的值。下列叙述中不正确的是( )
A.1mol乙烯与乙醇的混合物在氧气中充分燃烧,消耗氧气的分子数为一定为3NA
B.28g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA
C.常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
D.常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
要鉴别己烯中是否混有少量甲苯,正确的实验方法是( )
A.先加足量的酸性高锰酸钾溶液,然后再加入溴水
B.先加足量溴水,然后再加入酸性高锰酸钾溶液
C.分别点燃这两种液体,观察现象
D.加入浓硫酸与浓硝酸后加热
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对σ键的认识不正确的是 ( )
A. ss σ键与sp σ键的对称性相同
B. 烯烃分子中的碳碳双键的键能是碳碳单键键能的二倍
C.分子中含有共价键,则至少含有一个σ键
D.含有π键的化合物与只含σ键的化合物的化学性质不同
查看答案和解析>>
科目:高中化学 来源: 题型:
某实验小组用下列装置进行乙醇催化氧化的实验。

⑴ 实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式
__________________________________________________________________。
⑵ 甲和乙两个水浴作用不相同,乙的作用是___________________。集气瓶中收集到的气体的主要成分是_____________________。
⑶ 若试管a中收集到的液体用紫色石蕊试纸,试纸显红色,说明液体中还有____________。要除去该物质,可先在混合液中加入_________(填写字母)。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
然后再通过___________(填实验操作名称)即可除去。
⑷ 实验一段时间后,将试管a中的液体取出,加入足量的银氨溶液,再放入甲烧杯中,很快出现明显的现象。写出该反应的化学方程式 ;反应类型为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com