
某实验小组用下列装置进行乙醇催化氧化的实验。

⑴ 实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式
__________________________________________________________________。
⑵ 甲和乙两个水浴作用不相同,乙的作用是___________________。集气瓶中收集到的气体的主要成分是_____________________。
⑶ 若试管a中收集到的液体用紫色石蕊试纸,试纸显红色,说明液体中还有____________。要除去该物质,可先在混合液中加入_________(填写字母)。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
然后再通过___________(填实验操作名称)即可除去。
⑷ 实验一段时间后,将试管a中的液体取出,加入足量的银氨溶液,再放入甲烧杯中,很快出现明显的现象。写出该反应的化学方程式 ;反应类型为
【知识点】乙醇的催化氧化实验
【答案解析】
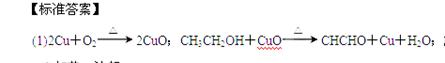
(2)冷却 氮气 (3) 乙酸 C 蒸馏 (4)银镜反应方程式 氧化反应
解析:(1)铜丝变黑是因为发生反应:2Cu+O2≜2CuO;后来变红是因为发生反应:CH3CH2OH+CuO→CH3CHO+Cu+H2O;
(2)根据反应流程可知:在甲处用热水浴加热使乙醇挥发与空气中的氧气混合,有利于下一步反应;乙处作用为冷水浴,降低温度,使生成的乙醛冷凝成为液体,沉在试管的底部;
⑶紫色石蕊试纸显红色说明试管a中的液体显示酸性,只能是含有乙酸;要出去乙酸可以利用其酸性让其与碳酸氢钠溶液反应,生成乙酸钠溶液水中,然后利用蒸馏的方法进行分离即可。
⑷试管a中的液体主要为乙醛,加入足量的银氨溶液,再放入甲烧杯中,发生了银镜反应,生成了银单质,此反应为氧化反应。
【思路点拨】本题考查了乙醇的催化氧化实验,掌握乙醇的催化反应历程是解答的关键,题目难度不大.注意培养分析问题,解决问题的能力.


科目:高中化学 来源: 题型:
某小组同学利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”。实验时,先分别量取两种溶液,倒入大试管中迅速振荡混合均匀,再加入硫酸,开始计时,通过测定混合溶液褪色所需时间来判断反应的快慢(已知反应方程式为:5H2C2O4+2KMnO4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O)。该小组设计了如下方案。
| 编号 | H2C2O4溶液 | KMnO4溶液 | 硫酸溶液 | 温度/℃ | ||
| 浓度 (mol/L) | 体积 (mL) | 浓度 (mol/L) | 体积 (mL) | |||
| ① | 0.10 | 2.0 | 0.010 | 4.0 | 4mL 4mol/L | 25 |
| ② | 0.20 | 2.0 | 0.010 | 4.0 | 4mL 4mol/L | 25 |
| ③ | 0.20 | 2.0 | 0.010 | 4.0 | 4mL 4mol/L | 50 |
(1)探究温度对化学反应速率影响的组合实验编号是__________(填编号,下同);探究反应物浓度对化学反应速率影响的组合实验编号是__________。
(2)该小组同学由此实验发现反应进行一些时间后,有一时间段反应速率不断加快。同学们分析除了反应放热使体系温度升高外,可能还有其它原因,他们联想到教材上的科学探究实验,推断出反应混合溶液中的__________(填化学式)也加速了此反应的进行。
(3)上述实验①中充分反应后H2C2O4过量,假设理论上能通过用酸性KMnO4溶液滴定的方法来测定反应混合液中过量的H2C2O4,请回答下列问题:
①取用反应混合液的滴定管用__________滴定管(填“酸式”或“碱式”,下同),盛装KMnO4溶液的滴定管用__________滴定管。
②下列操作中可能使测出的H2C2O4剩余量比理论值偏低的是__________。
A. 读取酸性KMnO4溶液体积时,开始仰视读数,滴定结束时俯视读数
B. 滴定前盛放反应混合液的锥形瓶用蒸馏水洗净但没有干燥
C. 盛装KMnO4溶液的滴定管滴定前有气泡,滴定后气泡消失
D. 盛装KMnO4溶液的滴定管未润洗就直接注入酸性KMnO4溶液
③此滴定实验是否需要滴加指示剂________(填“是”或“否”);怎么确定此滴定的终点:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是 ( )
A、乙烯、苯都可与溴水发生加成反应
B、乙醇、乙烯都可被酸性高锰酸钾溶液氧化
C、乙醇、乙酸都可以发生酯化反应
D、淀粉、油脂、蛋白质都可以发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下面有关晶体的叙述中,不正确的是( )
A.金刚石为空间网状结构,由共价键形成的碳原子环上,最小的环上有6个碳原子
B.氯化钠晶体中,每个Na+周围距离相等的Na+共有6个
C.氯化铯晶体中,每个Cs+周围紧邻8个Cl-
D.干冰晶体中,每个CO2分子周围紧邻12个CO2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
氯化硼的熔点为-107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120°,它能水解,有关叙述正确的是( )
A.氯化硼液态时能导电而固态时不导电 B.硼原子以sp杂化
C.氯化硼遇水蒸气会产生白雾 D.氯化硼分子属极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于基本营养物质的说法中正确的是
A.糖类、油脂、蛋白质都是天然高分子化合物
B.蔗糖溶液加稀硫酸水浴后,再加入少量新制的Cu(OH)2加热可产生砖红色沉淀
C.利用油脂在碱性条件下水解,可以生产甘油和肥皂
D.浓硫酸可以使蛋白质变黄 ,称为颜色反应,常用来鉴别部分蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
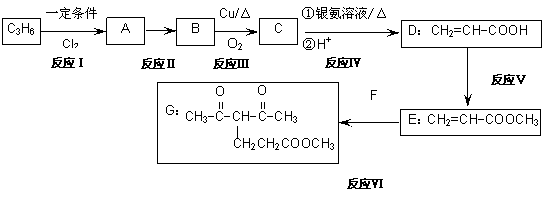 已知化合物G的合成路线如下:
已知化合物G的合成路线如下:
(1)反应Ⅰ的反应类型为_____________,反应Ⅵ的反应类型为 。
(2)写出反应Ⅱ的化学方程式_____________________。
写出反应Ⅲ-的化学方程式_____________________。
(3)已知麦克尔反应: 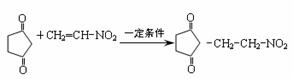 ,反应Ⅵ属于上面列出的麦克尔反应类型,且F的核磁共振氢谱有两个吸收峰,面积比为3:1,则F的结构简式为 。
,反应Ⅵ属于上面列出的麦克尔反应类型,且F的核磁共振氢谱有两个吸收峰,面积比为3:1,则F的结构简式为 。
(4)写出检验C物质中官能团的方法和现象____________________________________。
(5)比G少2个氢原子的物质具有下列性质:
①遇FeCl3溶液显紫色; ②苯环上的一氯取代物只有一种;
③1mol物质最多可消耗1mol NaOH; ④不考虑氧原子连接在一起的情况。
符合该要求的有机物有_______种,任写两种该物质的结构简式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,反应N2(g)+3H2(g) 2NH3(g)的反
2NH3(g)的反
应热和化学平衡常数分别为△H和K, 则相同温度时反应4NH3(g) 2N2(g)+6H2(g)反应热和化学平衡常数为( )
2N2(g)+6H2(g)反应热和化学平衡常数为( )
A.2△H和2K B.-2△H和 K2
C.-2△H和 K-2 D.2△H和-2K
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com