
����Ŀ����ӦA(g)��3B(g) ![]() 2C(g)��2D(g)�����ֲ�ͬ����µķ�Ӧ���ʷֱ�Ϊ��v(A)��0.15 mol��L��1��s��1 ��v(B)��0.6 mol��L��1��s��1����v(C)��0.4 mol��L��1��s��1����v(D)��0.45 mol��L��1��s��1�÷�Ӧ���еĿ���˳��Ϊ(����)
2C(g)��2D(g)�����ֲ�ͬ����µķ�Ӧ���ʷֱ�Ϊ��v(A)��0.15 mol��L��1��s��1 ��v(B)��0.6 mol��L��1��s��1����v(C)��0.4 mol��L��1��s��1����v(D)��0.45 mol��L��1��s��1�÷�Ӧ���еĿ���˳��Ϊ(����)
A.�ܣ��ڣ��ۣ���B.�ܣ��ڣ��ۣ���
C.�٣��ڣ��ۣ���D.�٣��ڣ��ۣ���
���𰸡�A
��������
�����ʵķ�Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ���B�ķ�Ӧ��������ʾÿ��ѡ���е����ʣ��ɻ�ѧ����ʽA(g)+3B(g) ![]() 2C(g)+2D(g)�ó���
2C(g)+2D(g)��
��v(B)=3v(A)=3��0.15mol��L-1��s-1=0.45mol��L-1��s-1��
��v(B)=0.6mol��L-1��s-1��
��v(B)=![]() v(C)=
v(C)=![]() ��0.4mol��L-1��s-1=0.6mol��L-1��s-1��
��0.4mol��L-1��s-1=0.6mol��L-1��s-1��
��v(B)=![]() v(D)=
v(D)=![]() ��0.45mol��L-1��s-1=0.675mol��L-1��s-1��
��0.45mol��L-1��s-1=0.675mol��L-1��s-1��
�ȽϢ٢ڢۢܵĴ�СΪ�ܣ���=�ڣ��١�
��ѡ��A��


 �ִʾ�ƪ��ͬ�����Ĵ��ϵ�д�
�ִʾ�ƪ��ͬ�����Ĵ��ϵ�д� �߽�������ϵ�д�
�߽�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2018�꣬�����˳��ˡ�����Э����ʵ���ٹ�ҵ��ս�ԣ����й�ȴ�Ӵ��˻������ȣ�����ڹ�����ҹ������εĴ���������ҹ�������ǿ��������CO2���⻯�ϳɼ״������Ĺ�ҵ�������о���ʵ�ֿɳ�����չ��
��1����֪��CO2(g)+H2(g)![]() H2O(g) +CO(g)����H1 = + 41.1 kJmol-1
H2O(g) +CO(g)����H1 = + 41.1 kJmol-1
CO(g)+2H2(g)![]() CH3OH(g)����H2=��90.0 kJmol-1
CH3OH(g)����H2=��90.0 kJmol-1
д��CO2���⻯�ϳɼ״����Ȼ�ѧ����ʽ��_______��
��2��Ϊ���CH3OH���ʣ�������Ӧ���õ�������_______������ĸ����
a.���¸�ѹ b.���µ�ѹ c.���µ�ѹ d.���¸�ѹ
��3��250�桢�ں����ܱ���������CO2(g)���⻯�ϳ�CH3OH(g)����ͼΪ��ͬͶ�ϱ�[n(H2)/n(CO2)]ʱij��Ӧ��Xƽ��ת���ʱ仯���ߡ�
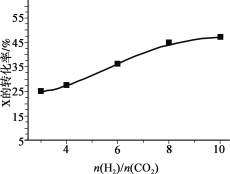
�� ��Ӧ��X��_______������CO2������H2������
�� �������_______��
��4��250�桢�����Ϊ2.0L�ĺ����ܱ������м���6mol H2��2mol CO2�ʹ�����10minʱ��Ӧ�ﵽƽ�⣬���c(CH3OH) = 0.75 mol�� L��1��
�� ǰ10min��ƽ����Ӧ����v(H2)��_______ mol��L��1��min ��1��
�� ��ѧƽ�ⳣ��K = _______��
�� �����ͷ�Ӧ�����뷴Ӧ��ת���ʺͲ����ѡ�����и߶���ء�������ͬͶ�ϱȺ���ͬ��Ӧʱ�䣬����ʵ���������£�
ʵ���� | �¶ȣ�K�� | ���� | CO2ת���ʣ�%�� | �״�ѡ���ԣ�%�� |
A | 543 | Cu/ZnO���װ� | 12.3 | 42.3 |
B | 543 | Cu/ZnO����Ƭ | 11.9 | 72.7 |
C | 553 | Cu/ZnO���װ� | 15.3 | 39.1 |
D | span>553 | Cu/ZnO����Ƭ | 12.0 | 70.6 |
�����ϱ��������ݣ���CO2�����״�������ѡ��Ϊ_______������ĸ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���㶹����һ����;�㷺�����ϣ������������㾫�Լ��������û�ױƷ�������ȡ����л���M���л���A�ϳ��㶹�ص��������£�
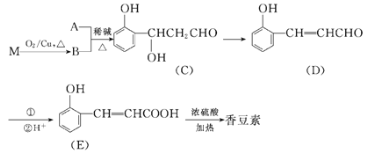
��֪������Ϣ��
��(CH3)3CCHO+CH3CHO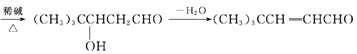
��M�ķ���ʽΪC2H6O����������3�ֻ�ѧ������ͬ����ԭ��
���㶹���к���������Ԫ��
��1����M����B�Ļ�ѧ����ʽΪ___��
��2��A�Ľṹ��ʽΪ___��
��3����E�����㶹�صĻ�ѧ����ʽΪ___��
��4��д����������������C��һ��ͬ���칹��Ľṹ��ʽ��__��
���ܷ���������Ӧ ��1molC��ȫ��Ӧ������2molNaOH
�۱�������3��ȡ���� �ܱ����ϵ�һ�ȴ���ֻ��2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ļ������ڻ�����������Ҫ�����ã�
(1)����������![]() mol������
mol������![]() mol�����ں��¡��ݻ��㶨Ϊ1L���ܱ������з�Ӧ���ɰ�����20min��ﵽƽ�⣬���������ʵ���Ϊ
mol�����ں��¡��ݻ��㶨Ϊ1L���ܱ������з�Ӧ���ɰ�����20min��ﵽƽ�⣬���������ʵ���Ϊ![]() mol��
mol��
�ٸ������µ�����ת������______�����¶���![]() �Ļ�ѧƽ�ⳣ����______
�Ļ�ѧƽ�ⳣ����______![]() ����С�������λ
����С�������λ![]() ��
��
���ڵ�25minʱ�������¶Ȳ��䣬���������Ѹ��������2L�����ֺ��ݣ���ϵ�ﵽƽ��ʱ![]() ����ת����Ϊ
����ת����Ϊ![]() ������ת���ʼ�С��ԭ����______��
������ת���ʼ�С��ԭ����______��
�ۺϳɰ���Ӧ��![]()
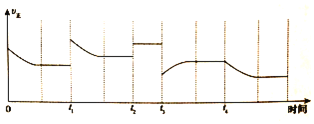
![]() ���ڷ�Ӧ������ֻ�ı�һ������������Ӧ���ʵı仯��ͼ��ʾ��
���ڷ�Ӧ������ֻ�ı�һ������������Ӧ���ʵı仯��ͼ��ʾ��![]() ʱ�ı��������______��
ʱ�ı��������______��![]() ʱ�ı��������______��
ʱ�ı��������______��
(2)��![]() ��һ�ָ���ȼ�ϣ���ǿ��ԭ�ԣ���ͨ��
��һ�ָ���ȼ�ϣ���ǿ��ԭ�ԣ���ͨ��![]() ��NaClO��Ӧ�Ƶã�д�����Ʊ���Ӧ�Ļ�ѧ����ʽ______��
��NaClO��Ӧ�Ƶã�д�����Ʊ���Ӧ�Ļ�ѧ����ʽ______��
��N2H4��ˮ��Һ�������ԣ�����������볣��![]() ����
����![]()
![]() ˮ��Һ��pH����______
ˮ��Һ��pH����______![]() ����
����![]() �Ķ��������
�Ķ��������![]() �ĵ���
�ĵ���![]() ��
��
����֪298K��101kPa�����£�
![]()
![]()
![]()
![]()
��![]() ��ȼ����
��ȼ����![]() ______��
______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������11.2 g KOH��ϡ��Һ��1 L 0.1 mol��L��1��H2SO4��Һ��Ӧ���ų�11.46kJ����������ʾ�÷�Ӧ���к��ȵ��Ȼ�ѧ����ʽΪ
A.KOH(aq)��![]() H2SO4(aq)��
H2SO4(aq)��![]() K2SO4(aq)��H2O(l) ��H����11.46 kJ��mol��1
K2SO4(aq)��H2O(l) ��H����11.46 kJ��mol��1
B.2KOH(aq)��H2SO4(aq)��K2SO4(aq)��2H2O(l) ��H����11.46 kJ��mol��1
C.KOH(aq)��![]() H2SO4(aq)��
H2SO4(aq)��![]() K2SO4(aq)��H2O(l) ��H����57.3 kJ��mol��1
K2SO4(aq)��H2O(l) ��H����57.3 kJ��mol��1
D.2KOH(aq)��H2SO4(aq)��K2SO4(aq)��2H2O(l) ��H����114.6 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й��Ȼ�ѧ����ʽ����������ȷ����
A.1mol����ȼ��������̬ˮ�Ͷ�����̼���ų��������Ǽ����ȼ����
B.��N2O4(g)![]() 2NO2(g)��H=" -56.9" kJ��mol-1����֪��1mol N2O4(g)�����ܱ������г�ַ�Ӧ��ų�����Ϊ56.9kJ
2NO2(g)��H=" -56.9" kJ��mol-1����֪��1mol N2O4(g)�����ܱ������г�ַ�Ӧ��ų�����Ϊ56.9kJ
C.�ɣ�H+(aq)��OH��(aq)��H2O(l)��H����57.3kJ/mol����֪����1mol CH3COOH����Һ�뺬1mol NaOH����Һ��ϣ��ų�����Ϊ57.3 kJ
D.��֪101kPaʱ��2C(s)��O2(g)===2CO(g) ��H����221kJ/mol����1 mol̼��ȫȼ�շų�����������110.5kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������жϲ���ȷ����
����NaA��NaB��Һ��pH�ֱ�Ϊ9��8��������һ����![]() ��
��
��![]() ��Һ���ɵ�
��Һ���ɵ�![]() ���壬
���壬![]() ��Һ���ɵ�
��Һ���ɵ�![]() ���壻
���壻
��![]() ˮ�����
ˮ�����![]() ��
��![]() ����ˮ��Һ�м�������������������к�
����ˮ��Һ�м�������������������к�![]() ��ʹˮ��ƽ�����ƣ�
��ʹˮ��ƽ�����ƣ�
���к�pH���������ͬ������ʹ�����Һ������NaOH�����ʵ�����ͬ��
����![]() ��Ϊ����ˮ�⣬����
��Ϊ����ˮ�⣬����![]() ��Һʱ�轫
��Һʱ�轫![]() �ܽ���ϡ
�ܽ���ϡ![]() �У�
�У�
A.ֻ�Т٢�B.ֻ�Тڢۢ�C.ֻ�Т٢ڢۢ�D.ȫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯��������������ԭ�����͵���( )
A.��H2Sˮ��Һ�м���NaOH������S2-����
B.��������ֽ�Ӵ����������̣�ʹ��λʱ���ڲ�����������������
C.�ϳɰ�ʱ����Һ�����룬�����ԭ�ϵ�������
D.������ˮ���ú���ɫ��dz
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
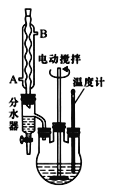
����Ŀ���������������ɱ��������Ҵ���Ũ���Ṳ���·�Ӧ�Ƶã���֪�����������ǿ��̼�ᣩ����Ӧװ����ͼ������װ��ʡ�ԣ�����Ӧԭ�����£�
 +C2H5OH
+C2H5OH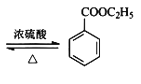 +H2O
+H2O
ʵ��������裺
����������ƿ�ڼ���12.2 g�����ᡢ25 mL�Ҵ���20 mL����4 mLŨ���ᣬҡ�ȣ������ʯ��
��װ�Ϸ�ˮ�����綯���������¶ȼƣ���������ˮ���²�Һ��ӽ�֧��ʱ���²�Һ�������Ͳ�С��������������������Ҵ�����ƿ���а���(Լ3h)��ֹͣ���ȡ�
�۽���ӦҺ����ʢ��80 mL��ˮ���ձ��У��ڽ����·�������̼���Ʒ�ĩ����Һ������̼�ݳ�����pH��ֽ�����������ԡ�
���÷�Һ©���ֳ��л��㣬ˮ����25 mL������ȡ��Ȼ��ϲ����л��㡣����ˮCaC12����ֲ�������������������ѡ����¶ȳ���140��ʱ��ֱ�ӽ���210��213�����֣�����ͨ������õ���������������12.8 mL��
�����õ����й��������£�
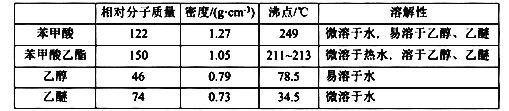
�ش��������⣺
(1)��Ӧװ���з�ˮ���Ϸ�������������______
(2)������м�Ũ�����������________���ӷ�ʯ��Ŀ����______��
(3)�������ʹ�÷�ˮ����ˮ��Ŀ����__________��
(4)������м���̼���Ƶ�Ŀ����____________ ��
(5)��������л���ӷ�Һ©����____��ѡ�����Ͽڵ����������¿ڷų�������
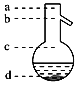
(6)����������¶ȼ�ˮ�����λ��ӦΪ��ͼ��________(��a��b��c��d)��ʾ��
(7)��ʵ�����õ��ı�������������______%��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com