
【题目】某一气态烷烃和一气态单烯烃组成的混合气体,在同温同压下对氢气的相对密度为13,标准状况下将此混合气体29.12L通入足量溴水中,溴水的质量增加21.0g.
(1)混合气体中的气态烷烃是?
(2)混合气体中单烯烃的分子式是?其结构简式是?
【答案】
(1)解:在同温同压下,混合气体对氢气的相对密度为13,故混合气体的平均相对分子质量为13×2=26,故一定含有甲烷,
答:混合气体中烷烃为CH4;
(2)解:标况下29.12L混合气体的物质的量为 ![]() =1.3mol,故混合气体的总质量为1.3mol×26g/mol=33.8g,溴水质量增重21.0g为烯烃的质量,故甲烷的质量为33.8g﹣21.0g=12.8g,故甲烷的物质的量为
=1.3mol,故混合气体的总质量为1.3mol×26g/mol=33.8g,溴水质量增重21.0g为烯烃的质量,故甲烷的质量为33.8g﹣21.0g=12.8g,故甲烷的物质的量为 ![]() =0.8mol,烯烃的物质的量为1.3mol﹣0.8mol=0.5molmol,烯烃的摩尔质量为
=0.8mol,烯烃的物质的量为1.3mol﹣0.8mol=0.5molmol,烯烃的摩尔质量为 ![]() =42g/mol,令烯烃的组成为(CH2)n,故14n=42,解得n=3,故该烯烃为C3H6,结构简式为:CH2=CH﹣CH3,
=42g/mol,令烯烃的组成为(CH2)n,故14n=42,解得n=3,故该烯烃为C3H6,结构简式为:CH2=CH﹣CH3,
答:单烯烃分子式为C3H6,结构简式为:CH2=CH﹣CH3
【解析】(1)相同条件下,密度之比等于相对分子质量之比,据此计算混合气体的相对分子质量,进而确定含有的烷烃;(2)根据n= ![]() 计算29.12L混合气体的物质的量,再根据m=nM计算混合气体的质量,溴水质量增重21.0g为烯烃的质量,进而计算烷烃的质量与物质的量,再计算烯烃,根据M=
计算29.12L混合气体的物质的量,再根据m=nM计算混合气体的质量,溴水质量增重21.0g为烯烃的质量,进而计算烷烃的质量与物质的量,再计算烯烃,根据M= ![]() 计算其摩尔质量,据此计算烯烃的分子式,书写可能的结构式.
计算其摩尔质量,据此计算烯烃的分子式,书写可能的结构式.


科目:高中化学 来源: 题型:
【题目】由CO和H2S反应可制得羰基硫(COS)。在恒容的密闭容器中发生反应并达到平衡:CO(g)+H2S(g) ![]() COS(g)+H2(g),数据如下表所示:
COS(g)+H2(g),数据如下表所示:
实验 | 温度/℃ | 起始时 | 平衡时 | |||
n(CO)/mol | n(H2S)/mol | n(COS)/mol | n(H2)/mol | n(CO)/mol | ||
1 | 150 | 10.0 | 10.0 | 0 | 0 | 7.0 |
2 | 150 | 7.0 | 8.0 | 2.0 | 4.5 | a |
3 | 400 | 20.0 | 20.0 | 0 | 0 | 16.0 |
下列说法正确的是( )
A. 上述反应是吸热反应
B. 实验1达平衡时,CO的转化率为70%
C. 实验2达平衡时,a<7.0
D. 实验3达平平衡后,再充入1.0molH2,平衡逆向移动,平衡常数值增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某温度下CH3COOH的电离常数K=1.6×10﹣5 . 该温度下,向20mL 0.01molL﹣1 CH3COOH溶液中逐滴加入0.01molL﹣1 KOH溶液,回答下列有关问题:
(1)醋酸溶液中c(H+)为 , pH约为 .
(2)用滴定管取CH3COOH溶液20.00mL放在锥形瓶中,滴加几滴酚酞,待测.滴定管在使用前除洗涤外,还应 .
(3)判断到达滴定终点的实验现象是;
(4)下列操作中,可能使所测CH3COOH溶液的浓度偏低的是
A.碱式滴定管未用标准碱液润洗就直接注入标准液
B.读取碱液体积时,开始仰视读数,滴定结束时俯视读数
C.碱式滴定管在滴定前有气泡,滴定后气泡消失
D.滴定前盛放CH3COOH溶液的锥形瓶用蒸馏水洗净后没有干燥.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请同学们根据官能团的不同对下列有机物进行分类.把正确答案填写在题中的横线上①CH3CH2OH② ![]() ③CH3CH2Br④
③CH3CH2Br④ ![]() ⑤
⑤ ![]() ⑥
⑥ ![]() ⑦
⑦ ![]() ⑧
⑧ ![]() ⑨
⑨ ![]() ⑩
⑩ ![]()
(1)芳香烃:;
(2)卤代烃:;
(3)醇:;
(4)酚:;
(5)醛:;
(6)酮:;
(7)羧酸:;
(8)酯: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如图所示的实验装置来粗略测定电石中碳化钙的质量分数.
(1)烧瓶中发生反应的化学方程式是 . 装置B和C的作用是 . 烧瓶要干燥,放人电石后应塞紧橡皮塞,这是为了
(2)所用电石质量不能太大,否则;也不能太小,否则 . 若容器B的容积为250mL,则所用的电石质量应在g左右.(从以下数据选填:0.30、0.60、1.00、1.50、2.00)
(3)为了得到比较平稳的乙炔气流,常可用代替水.
(4)实验中测得排入量筒中水的体积为V mL(1.01×105 Pa,0℃),电石质量为W g.则电石中碳化钙的质量分数是 . (不计导管中残留的水,气体中饱和水蒸气可忽略不计)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示某反应进行时,有酶参与和无酶参与的能量变化,则下列叙述正确的是( )
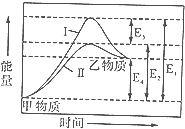
A.此反应为放能反应
B.曲线Ⅰ表示有酶参与
C.E1为反应前后能量的变化
D.酶参与反应时,所降低的活化能为E3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F均为短周期元素,原子序数依次递增.A元素原子核内无中子.B元素原子核最外层电子数是次外层电子数的2倍.C元素是地壳中含量最多的元素.D是短周期元素中金属性最强的元素.E与F的位置相邻,F的最高价氧化物的水化物为最强酸.
(1)推断B在元素周期表中的位置:第周期,第族.
(2)写出F的电子排布式: .
(3)C、D可形成淡黄色的粉末,其电子式为 .
(4)写出A与C形成的10电子微粒的化学式:、、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 2.24L甲烷气体中碳氢键的数目为0.4NA
B. lmolSO2与足量的O2反应,转移的电子数为2NA
C. 1 mol·L-1CH3COOH 与1 mol·L-1CH3COONa 溶液等体积混合,溶液中CH3COOH 和CH3COO-的总数为2NA
D. 7.8g乙炔与苯的混合物完全燃烧所消耗的O2分子数为0.75NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是中学化学中常见物质的转化关系,部分物质和反应条件略去。
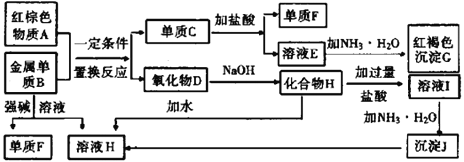
(1)如果把红棕色物质A换成黑色磁性晶体,推测出来的物质是完全一致的,请写出黑色磁性晶体与过量盐酸反应的化学方程式_______________________________。
(2)写出单质B与强碱溶液反应的离子方程式:_______________________________。把溶液Ⅰ中的阳离子完全转化为沉淀J为什么加氨水而不加氢氧化钠_______________。
(3)溶液E中加入氨水时,先生成白色沉淀L,写出生成L的离子方程式:_________________________。白色沉淀L最终变为红褐色沉淀G,写出L变为G的化学反应方程式_________________________。
(4)保存E溶液时候为什么要加入单质C,用离子方程式解释_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com