
【题目】由CO和H2S反应可制得羰基硫(COS)。在恒容的密闭容器中发生反应并达到平衡:CO(g)+H2S(g) ![]() COS(g)+H2(g),数据如下表所示:
COS(g)+H2(g),数据如下表所示:
实验 | 温度/℃ | 起始时 | 平衡时 | |||
n(CO)/mol | n(H2S)/mol | n(COS)/mol | n(H2)/mol | n(CO)/mol | ||
1 | 150 | 10.0 | 10.0 | 0 | 0 | 7.0 |
2 | 150 | 7.0 | 8.0 | 2.0 | 4.5 | a |
3 | 400 | 20.0 | 20.0 | 0 | 0 | 16.0 |
下列说法正确的是( )
A. 上述反应是吸热反应
B. 实验1达平衡时,CO的转化率为70%
C. 实验2达平衡时,a<7.0
D. 实验3达平平衡后,再充入1.0molH2,平衡逆向移动,平衡常数值增大
【答案】C
【解析】A、实验1中,开始通入20.0mol的CO和20.0molH2S,建立的平衡,与开始通入10.0mol的CO和10.0molH2S,建立的平衡互为等效平衡,通入20.0mol的CO和20.0molH2S,达到平衡, CO物质的量为(20-20×3/10)mol=14mol,温度由150℃升高到400℃,CO的物质的量由14mol→16mol,升高温度,平衡向逆反应反应方向移动,即正反应是放热反应,故A错误;B、实验1中消耗CO的物质的量为(10-7.0)mol=3mol,即CO的转化率为3/10×100%=30%,故B错误;
C、 CO(g)+H2S(g) ![]() COS(g)+H2(g)
COS(g)+H2(g)
起始:10 10 0 0
变化:3 3 3 3
平衡:7 7 3 3 ,此温度下,K=![]() ,实验2中浓度商Qc=
,实验2中浓度商Qc=![]() <K,说明反应正向移动,即a<7.0,故C正确;D、平衡常数只受温度的影响,因此再充入1.0molH2,平衡逆向移动,但化学平衡常数不变,故D错误。
<K,说明反应正向移动,即a<7.0,故C正确;D、平衡常数只受温度的影响,因此再充入1.0molH2,平衡逆向移动,但化学平衡常数不变,故D错误。


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
【题目】下列分类或归类正确的是
①硫酸、氨水、干冰、碘化银均为纯净物 ②CaCl2、NaOH、HCl、IBr均为化合物
③明矾、水银、烧碱、硫酸均为电解质 ④二氧化硫、氨气、乙醇都是非电解质
⑤碘酒、淀粉、云雾、纳米材料均为胶体
A.①③④B.②③C.②④D.②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一些常见单质、化合物之间的转化关系图,有些反应中的部分物质被略去。常温常压下,A为无色有毒气体,B为红棕色粉末,C、E为金属单质,G、J的焰色均为黄色。反应①为炼铁高炉中的重要反应;反应②可用于焊接铁轨。
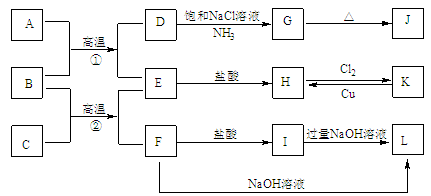
请回答下列问题:
(1)B的化学式为 ,J的化学式为 。
(2)工业上将氯气通入石灰乳中制取漂白粉,该反应的化学反应方程式为 。
(3)D→G是侯氏制碱法的主要反应,该反应的化学方程式为 。
(4)K→H是制作印刷电路板的重要反应,该反应的离子方程式为 。
(5)F→L是铝土矿提纯中的重要反应,该反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过硫酸钾(![]() )具有强氧化性(常被还原为硫酸钾),80℃以上易发生分解.实验室模拟工业合成过硫酸钾的流程如下:
)具有强氧化性(常被还原为硫酸钾),80℃以上易发生分解.实验室模拟工业合成过硫酸钾的流程如下:
(1)硫酸铵和硫酸配制成电解液,以铂作电极进行电解,生成过硫酸铵溶液.写出电解时发生反应的离子方程式________________________.
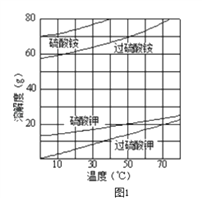
(2)已知相关物质的溶解度曲线如图1所示.在实验室中提纯过硫酸钾粗产品的实验具体操作依次为:将过硫酸钾粗产品溶于适量水中,__________________________,干燥.
(3)样品中过硫酸钾的含量可用碘量法进行测定.实验步骤如下:
步骤1:称取过硫酸钾样品0.3000g于碘量瓶中,加入30mL水溶解.
步骤2:向溶液中加入4.000g KI固体(略过量),摇匀,在暗处放置30min.
步骤3:在碘量瓶中加入适量醋酸溶液酸化,以淀粉溶液作指示剂,用0.1000molL﹣1 Na2S2O3标准溶液滴定至终点,共消耗Na2S2O3标准溶液21.00mL.(已知反应:I2+2S2O32﹣=2I﹣+S4O62﹣)
①若步骤2中未将碘量瓶“在暗处放置30min”,立即进行步骤3,则测定的结果可能_______(选填“偏大”、“偏小”、“无影响”);上述步骤3中滴定终点的现象是_________.
②根据上述步骤可计算出该样品中过硫酸钾的质量分数为_______.
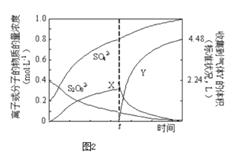
(4)将0.40mol过硫酸钾与0.20mol硫酸配制成1L溶液,在80℃条件下加热并在t时刻向溶液中滴加入少量FeCl3溶液,测定溶液中各成分的浓度如图2所示(H+浓度未画出).图中物质X的化学式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应N2(g)+3H2(g)2NH3(g)△H<0,下列研究目的和示意图相符的是( )
A | B | C | D | |
研究目的 | 压强对反应的影响(P2>P1) | 温度对反应的影响 | 平衡体系增加N2对反应的影响 | 催化剂对反应的影响 |
图示 |
|
|
|
|
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作:①取液体试剂,②取固体试剂,③溶解,④过滤,⑤蒸发。一定要用到玻璃棒的是
A. ①②③ B. ②③④ C. ①②⑤ D. ③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温常压下,在带有相同质量活塞的容积相等的甲、乙两容器里,分别充有二氧化氮和空气,现分别进行下列两上实验:(N2O42NO2△H>0) (a)将两容器置于沸水中加热
(b)在活塞上都加2kg的砝码
在以上两情况下,甲和乙容器的体积大小的比较,正确的是( )
A.(a)甲>乙,(b)甲>乙
B.(a)甲>乙,(b)甲=乙
C.(a)甲<乙,(b)甲>乙
D.(a)甲>乙,(b)甲<乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一气态烷烃和一气态单烯烃组成的混合气体,在同温同压下对氢气的相对密度为13,标准状况下将此混合气体29.12L通入足量溴水中,溴水的质量增加21.0g.
(1)混合气体中的气态烷烃是?
(2)混合气体中单烯烃的分子式是?其结构简式是?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com