
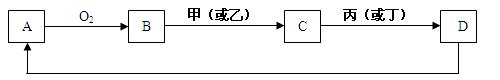
科目:高中化学 来源:不详 题型:单选题
| A.X+ | B.X2+ | C.X3+ | D.X4+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.能量守恒原理 |
| B.近似能级图中的顺序 3d 轨道能量比 4s 轨道高 |
| C.洪特规则 |
| D.泡利不相容原理 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.14 | B.31 | C.74.9 | D.121.8 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
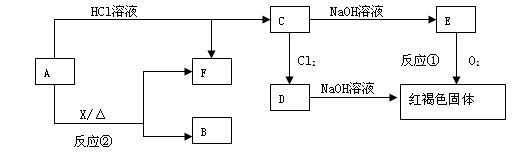
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
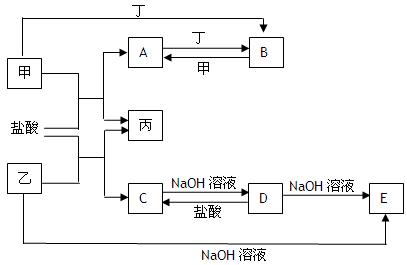
 。
。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com