
| A.能量守恒原理 |
| B.近似能级图中的顺序 3d 轨道能量比 4s 轨道高 |
| C.洪特规则 |
| D.泡利不相容原理 |
科目:高中化学 来源:不详 题型:单选题
| A.气态氢化物的稳定性:HF>HCl>HBr>HI | B.单质的氧化性:F2>Cl2>Br2>I2 |
| C.离子的还原性:F->Cl->Br->I- | D.元素的非金属性:F>Cl>Br>I |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
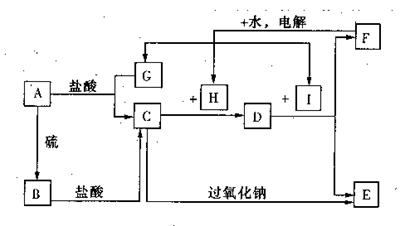
 采取的方法是 。
采取的方法是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
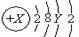 。则X、Y及该原子3p能级上的电子数分别为( )
。则X、Y及该原子3p能级上的电子数分别为( )| A.18、6、4 | B.20、8、6 | C.18、8、6 | D.15~20、3~8、1~6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.一个O4分子由两个O2分子构成 | B.O4是一种单质 |
| C.等质量的O4和O2含有相同数目的原子 | D.O4是一种化合物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
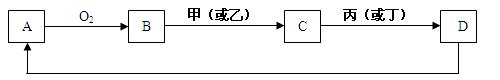
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 ;B ; H ;F
;B ; H ;F 
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com