
【题目】高聚合物G、I 可用于生产全生物降解塑料, 在“白色污染”日益严重的今天有着重要的作用。有关转化关系如下:

已知:①CH3CH2CH2Br+NaOH![]() CH3CH2CH2OH+NaBr;②H的分子中有一个含“—O—”结构的三元环;③含有“
CH3CH2CH2OH+NaBr;②H的分子中有一个含“—O—”结构的三元环;③含有“![]() ”结构的有机物分子不能稳定存在。
”结构的有机物分子不能稳定存在。
请回答下列问题:
(1)写出H的结构简式_____________。
(2)下列说法不正确的是_______________。
A.化合物G、I属于酯类
B.物质A可以发生中和反应
C.1mol D与足量Na反应放出1molH2
D.B和氯气在一定条件可以发生加成生成C3H5Cl
(3)写出由两分子 F合成六元环化合物的化学方程式_________。
(4)化合物F有多种同分异构体,写出符合下列条件F的同分异构体的结构简式_____________。
①能和NaOH反应;②能发生银镜反应
(5)依据上述合成路线,设计以乙烯为原料制备乙二醛(![]() )的合成路线(无机原料任意选择,合成路线用流程图表示)__________________。合成路线流程图示列:
)的合成路线(无机原料任意选择,合成路线用流程图表示)__________________。合成路线流程图示列:![]()
【答案】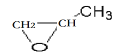 BD
BD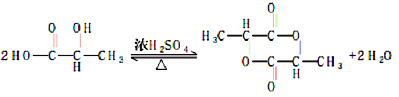 HCOO CH2CH2OH、 HCOO CH(OH)CH3 、HCOO CH2OCH3
HCOO CH2CH2OH、 HCOO CH(OH)CH3 、HCOO CH2OCH3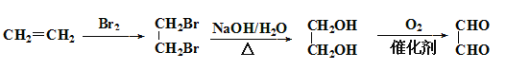
【解析】
B中含有碳碳双键,与溴水发生加成反应生成C,C在碱性条件下水解得出D为CH3CHOHCH2OH,D催化氧化得E为CH3COCOOH,E与氢气发生加成反应得F为CH3CHOHCOOH,F中含有羧基和羟基在一定条件下发生缩聚反应得G,比较A与E的分子式可知,A为CH3COHCHO。由已知②H的分子中有一个含“—O—”结构的三元环,可知H为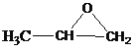 ,H与二氧化碳发生聚合反应生成聚碳酸酯多元醇。
,H与二氧化碳发生聚合反应生成聚碳酸酯多元醇。
(1)由以上分析可知,H的结构简式为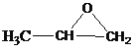 ;
;
(2)A、F为CH3CHOHCOOH,F中含有羧基和羟基,在一定条件下F发生分子间缩聚反应得G,因此G属于酯类;H为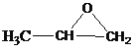 ,H与二氧化碳发生聚合反应生成聚碳酸酯多元醇I,因此I也属于酯类,故A正确;
,H与二氧化碳发生聚合反应生成聚碳酸酯多元醇I,因此I也属于酯类,故A正确;
B、由上述分析可知,A为CH3COHCHO,不能发生中和反应,故B错误;
C、D为CH3CHOHCH2OH,含有两个羟基,因此1mol D与足量Na反应放出1molH2,故C正确;
D、B中含有碳碳双键,能与氯气在一定条件可以发生加成生成C3H6Cl2,故D错误;
综上所述,本题应选BD;
(3)F为CH3CHOHCOOH中含有羟基和羧基,可以发生酯化反应,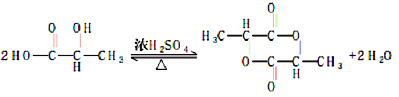 ;
;
(4)①能和NaOH反应,说明含有羧基或酯基,②能发生银镜反应,说明含有醛基,因此符合条件的同分异构体有HCOOCH2CH2OH、 HCOOCH(OH)CH3 、HCOOCH2OCH3
(5)以乙烯为原料,乙烯先与溴水发生加成反应生成1,2-二溴乙烷,1,2-二溴乙烷与氢氧化钠水溶液发生水解生成乙二醇,再经催化氧化可得乙二醛,具体流程为: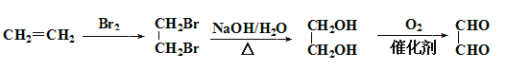 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列做法与盐类水解无关的是
A.用氯化铵溶液除铁锈
B.用热的稀硫酸溶解胆矾来配制胆矾溶液
C.用饱和氯化铁溶液制氢氧化铁胶体
D.用硝酸钾固体配制植物生长营养液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一些中学常见的物质之间的转化关系(其中部分反应产物省略),其中A和B常温下都是气体,且水溶液都有漂白性;I是一种金属单质;F、M、N均为水的白色沉淀,其中M和N不溶于稀硝酸,C和D是两种常见的强酸。请回答下列问题:
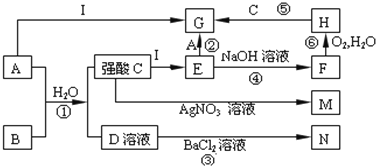
(1)写出①的化学方程式_______________________________________。
(2)写反应②的离子方程式__________________________________________。
(3)写出将A通入石灰乳的化学方程式________________________________________。
(4)在①→⑥中,属于氧化还原反应的有_______________________(填编号)
(5)将NaOH溶液加入到E中的现象为____________________________________。
(6)写出反应⑥的化学反应方程式_______________________________________。
(7)写出分别将A、B通入石蕊试液中的现象:
A__________________B__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用5.96 g NaClO固体配成100 mL溶液,向其中加入0.02 mol Na2Sx,恰好完全反应生成NaCl和Na2SO4。
(1)NaClO溶液浓度为__________。
(2)化学式Na2Sx中x的值为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,Ksp(CaSO4)=9×10-6,常温下,CaSO4在水中的沉淀溶解平衡曲线如图所示。下列判断错误的是
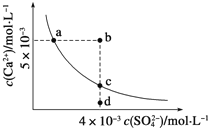
A. a、c两点均可以表示常温下CaSO4溶于水所形成的饱和溶液
B. a点对应的Ksp等于c点对应的Ksp
C. b点将有沉淀生成,平衡后溶液中c(SO42-)一定不等于3×10-3molL-1
D. 向d点溶液中加入适量CaCl2固体可以变到c点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对化学反应热现象的说法正确的是( )
A.放热反应发生时不必加热
B.化学反应的热效应数值与参加反应的物质的多少无关
C.吸热反应加热后才能发生
D.化学反应一定有能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下列反应:Fe+2Fe3+=3Fe2+ 制一个化学电池(给出若干导线和一个小灯泡,电极材料和电解液自选),画出实验装置图,注明电解质溶液名称和正负极材料,标出电子流动方向和电流方向,写出电极反应式,负极:_____________,正极:__________;装置图:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I现有①BaCl2、②金刚石、③KOH、④Na2SO4、⑤干冰、⑥碘片六种物质,按下列要求回答:
(1)熔化时不需要破坏化学键的是________(填写物质的序号,下同),熔化时需要破坏共价键的是________。
(2)属于离子化合物的是______________,只有离子键的物质是________。
(3)①的电子式是______________,⑤的电子式是_____________。
II下列粒子(分子或离子)均含有18个电子:
粒子 | A+ | B2- | C | D | E | F |
组成特点 | 单核离子 | 化合物,双核分子 | 单质, 双核分子 | 化合物,三核分子 | 化合物, 四核分子 | |
请回答下列问题:
(1)A的元素符号是____________,B2-的结构示意图是________。
(2)C的结构式为__________,已知D的单质与水反应可生成氧气及一种酸,写出该反应的化学方程式:________________________________________
(3)E的电子式是____________________;F的水溶液常用于消毒剂,F的化学式是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com