
【题目】若![]() 为阿伏加德罗常数的值,下列说法中,正确的是
为阿伏加德罗常数的值,下列说法中,正确的是
A.1mol![]() 与
与![]() 完全反应,转移的电子总数为
完全反应,转移的电子总数为![]()
B.34g氨气中含有12![]() 个
个![]() 键
键
C.常温常压下,1mol氦气含有的原子数为![]()
D.标准状况下,![]() 和
和![]() 混合后气体分子数为
混合后气体分子数为![]()
【答案】C
【解析】
A、过氧化钠与二氧化碳反应,过氧化钠发生自身氧化还原反应,氧元素化合价从![]() 价变化为0价和
价变化为0价和![]() 价;
价;
B、质量换算物质的量结合氨气分子结构计算;
C、氦气是单原子分子;
D、一氧化氮和氧气会发生反应生成二氧化氮,二氧化氮和四氧化二氮存在化学平衡;
A、过氧化钠与二氧化碳反应,过氧化钠发生自身氧化还原反应,氧元素化合价从![]() 价变化为0价和
价变化为0价和![]() 价;所以
价;所以![]() 与
与![]() 完全反应,转移的电子总数为
完全反应,转移的电子总数为![]() ,故A错误;
,故A错误;
B、氨气摩尔质量是![]() ,34g氨气物质的量为2mol,一个氨气分子含三个氮氢键,分子中含有
,34g氨气物质的量为2mol,一个氨气分子含三个氮氢键,分子中含有![]() 个
个![]() 键,故B错误;
键,故B错误;
C、氦气是单原子分子;1mol氦气含有的原子数为![]() ,故C正确;
,故C正确;
D、一氧化氮和氧气会发生反应生成二氧化氮,二氧化氮和四氧化二氮存在化学平衡;标准状况下,![]() 物质的量为
物质的量为![]() ,
,![]() 物质的量为
物质的量为![]() ,混合后发生反应:
,混合后发生反应:![]() ;生成二氧化氮
;生成二氧化氮![]() ,剩余氧气
,剩余氧气![]() ,共
,共![]() ,二氧化氮和四氧化二氮存在化学平衡,混合后气体分子数小于
,二氧化氮和四氧化二氮存在化学平衡,混合后气体分子数小于![]() ,故D错误;
,故D错误;
故选:C。


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
【题目】请回答下列问题:
(1) CH2=CHCH(CH3)2系统命名法命名为____________
(2) 4-甲基-2-乙基-1-戊烯的结构简式为__________________
(3) 支链只有一个乙基且式量最小的烷烃的结构简式为______________
(4) 某烃分子式为C6H14,若该烃不可能由炔烃与氢气加成得到则该烃的结构简式为__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列说法正确的是
A. 0.1mol/LNaHCO3溶液中:c(H+)+c(H2CO3)=c(CO32-)+c(OH-)
B. 0.1mol/LHCN和0.1mol/LNaCN的等体积混合溶液中:c(HCN)>c(Na+)>c(CN-)>c(H+)>c(OH-)
C. 0.1mol/LNa2C2O4溶液滴加HCl溶液至c(H2C2O4)=c(HC2O4-):3c(H2C2O4)>c(OH-)+c(Cl-)
D. 0.1mol/LNH4HSO4溶液滴加NaOH溶液至pH=7:c(Na+)=c(NH4+)+2c(NH3·H2O)>c(SO42-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜是人类最早使用的金属之一,铜的化合物丰富多彩。
(1) 铜与N2O4在一定条件下可制备无水Cu(NO3)2。
①基态Cu2+的电子排布式为________。
②与NO3-互为等电子体的一种分子为________(填化学式)。
(2) 邻氨基吡啶(![]() )的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。
)的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。
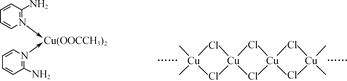
① C、N、O三种元素的第一电离能由大到小的顺序为________。
②邻氨基吡啶的铜配合物中,C原子轨道杂化类型为________。
③ 1 mol ![]() 中含有σ键的数目为________mol。
中含有σ键的数目为________mol。
(3) 铜的某种氯化物的链状结构如图所示。该氯化物的化学式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A.烷烃中除甲烷外,很多都能使酸性![]() 溶液的紫色退去
溶液的紫色退去
B.甲烷跟氯气反应无论生成![]() 、
、![]() 、
、![]() 还是
还是![]() ,都属于取代反应
,都属于取代反应
C.分子式符合![]() 的烃一定是烷烃
的烃一定是烷烃
D.甲烷能够燃烧,在一定条件下会发生爆炸,因此甲烷是矿井安全的重要威胁之一
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汞(熔点-39℃,沸点356℃)是制造电池、电极的重要原料,历史上曾用“灼烧辰砂法”制取汞。目前工业上制粗汞的一种流程图如下。
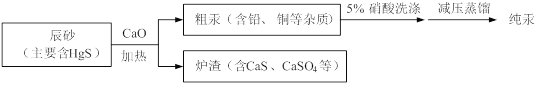
下列分析错误的是
A.洗涤粗汞可用5%的盐酸代替5%的硝酸
B.辰砂与氧化钙加热反应时,CaSO4为氧化产物
C.“灼烧辰砂法”过程中电子转移的方向和数目可表示为: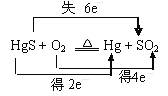
D.减压蒸馏的目的是降低汞的沸点,提高分离效率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组利用下列装置制备漂白粉,下列说法不正确的是( )
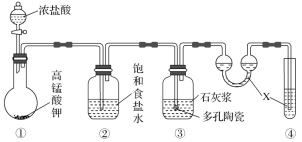
A.装置④中的X试剂为NaOH溶液
B.装置②中饱和食盐水的作用是除去Cl2中的HCl
C.装置③中的石灰浆可以用石灰水代替
D.制备漂白粉的反应是放热反应,温度较高时有副反应发生,可以将装置③放在冷水中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锡渣主要成分是SnO,还含有少量Fe、Cu、Sb、Pb、As等元素的氧化物.可用下列流程中的方法生产锡酸钠.
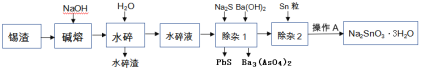
已知: ①砷酸钡难溶于水,Ksp(Ba3(AsO4)2)=10-24
②水碎液中溶质的主要成分为Na2SnO3,Na3AsO4, Na3SbO4,Na2PbO2
(1)碱熔就是在锡渣中加NaOH焙烧,SnO转变为Na2SnO3,则SnO参加反应的化学方程式为____________
(2)除杂1的目的是“除砷和铅”,加入硫化钠所发生反应的离子方程式为____________;若要使0.001mol/L的AsO43-沉淀完全(一般认为离子浓度小于10-6mol/L时即沉淀完全),需等体积加入至少____________mol/L的Ba(OH)2.
(3)除杂2中加入Sn粒的目的是____________
(4)已知Na2SnO3·3H2O可溶于水,难溶于乙醇,加热至140℃时会失去结晶水,所以最后一步从滤液中得到锡酸钠晶体的操作步骤为____________、过滤、用____________洗涤、____________.
(5)水碎渣中的铁元素主要以氧化物形式存在,回收比较容易,而铜冶炼过程中的铜渣中也有铁元素,但主要以硅酸铁的形式存在,回收方法更复杂:需先加CaO作置换剂,发生钙铁置换反应CaO+FeO·SiO2![]() CaO·SiO2+FeO,在反应过程中,加CaO的同时还需加入还原剂烟煤,则加入还原剂烟煤的作用是____________
CaO·SiO2+FeO,在反应过程中,加CaO的同时还需加入还原剂烟煤,则加入还原剂烟煤的作用是____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用锌片、铜片、发光二极管、滤纸、导线等在玻璃片制成如图所示的原电池,当滤纸用醋酸溶液润湿时,二极管发光.下列有关该电池的说法正确的是( )
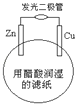
A. 铜片上的电极反应:Cu — 2e﹣ = Cu2+
B. 锌片为电池的负极
C. 外电路中电子由铜片经导线流向锌片
D. 电池工作时电能直接转化为化学能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com