
����Ŀ�����ᶡ����CH3COOCH2CH2CH2CH3���Ǿ��й���ζ���㾫����������Ӧ�ɽ������ᶡ���ĺϳɣ��й����ʵ��������ʼ������ϳɹ������£���һ���������������������ϼ��ȷ���������Ӧ���ڶ�����ϴ���ᴿ���������������ᴿ��
���� | 1������ | ���ᶡ�� | |
�۵�/�� | 16.6 | ��89.5 | ��73.5 |
�е�/�� | 117.9 | 117 | 126.3 |
�ܶ�/gcm��3 | 1.05 | 0.81 | 0.88 |
ˮ���� | ���� | ���� | ���� |

��1�������Ǻϳɺ��ᴿ���ᶡ�����й�װ��ͼ����д���ϳɺ��ᴿ���ᶡ���IJ���˳������ĸ��
C��F�������� ��
��2��Cװ���г���װ��1�����������������⣬����Ҫ������ �� װ��C�������ܵ������ǣ���
��3������F��������Ӧ��ɺ���ж�µ���ƿ�м���25mLˮ�������� �� Aװ����Na2CO3��Һ�������� ��
��4��װ��A�ķ�Һ©����Һ���Ϊ���㣬���ᶡ��Ӧ�������ϡ��£��㣮
��5����һ��������Ӧ�����п��ܵõ����л�����������д���������ʵĽṹ��ʽ����
���𰸡�
��1��E��A��D��B
��2��Ũ�����ʯ�����������ӷ�������Ͷ���
��3���ܽ�����δ��Ӧ����ʹ�����ȥ���ᶡ���й���������
��4����
��5��CH2=CH��CH2��CH3 �� CH3��CH2��CH2��CH2��O��CH2��CH2��CH2��CH3
���������⣺��1�������ᶡ���ĺϳɺ��ᴿ�IJ����֪����Ӧװ��ΪC��Ȼ��ˮϴΪF����ȡΪE��Aװ�ý���ˮϴ��ȥ�����ᣬѡD���ˣ��������ΪB����ʵ��װ�õ�˳��ΪC��F��E��A��D��B�����Դ��ǣ�E��A��D��B����2��C�г���װ��1�����������������⣬����ҪŨ��������������Ҫ��ʯ��ֹ���У�C�м��ȣ���Ӧ��ת��Ϊ���壬�������ܿ�ʹ�ӷ�������Ͷ����������������Դ��ǣ�Ũ�����ʯ�����������ӷ�������Ͷ�������3��δ��Ӧ����ʹ�������ˮ����ж�µ���ƿ�м���25mLˮ���������ܽ�����δ��Ӧ����ʹ���Na2CO3�����Ʒ�л��е����ᷴӦ��������Ϊ��ȥ���ᶡ���й��������ᣬ���Դ��ǣ��ܽ�����δ��Ӧ����ʹ�����ȥ���ᶡ���й����������4�����ᶡ�����ܶ�С��ˮ�����Էֲ�ʱ�����ᶡ�����ϲ㣻���Դ��ǣ��ϣ���5����һ����ӦΪ����������������Ũ���������»�ϼ��ȷ���������Ӧ�������ᶡ����CH3COOCH2CH2CH2CH3�������ܷ����ĸ���ӦΪ������Ũ���������µ���ȥ��Ӧ����CH2=CH��CH2��CH3 �� ����֮�䷢��ȡ����Ӧ����CH3��CH2��CH2��CH2��O��CH2��CH2��CH2��CH3 �� ���Դ��ǣ�CH2=CH��CH2��CH3 �� CH3��CH2��CH2��CH2��O��CH2��CH2��CH2��CH3 ��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������4�����ʣ� A��NaOH��Ca��OH��2��SO2��Fe��OH��3
B��Cl2��C��S��Cu
C��Hg��Cu��Zn��H2
D��H2O��HCl��H2SO4��HNO3
��1����д���пհף�
A�� | B�� | C�� | D�� | |
����� | ���������� | |||
�����ڸ��������� | SO2 | H2 | H2O |
��2��4�������ж����ڵ���ʵ���������ţ���
��3��д��ʵ�����Ʊ�Cl2�����ӷ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״�����Ϊ2l���͵�����ȼ�ϣ���ҵ��ͨ�����з�Ӧ��͢���CH4��H2OΪԭ�����Ʊ��״��� 
��1����1.0mol CH4��2.0mol H2O��g��ͨ���ݻ�Ϊ10L�ķ�Ӧ�ң���һ�������·�����Ӧ��CH4��g��+H2O��g��CO��g��+3H2��g����CH4��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��
����֪100��ʱ�ﵽƽ�������ʱ��Ϊ5min������H2��ʾ��ƽ����Ӧ����Ϊ ��
���������������������������¶ȣ���ѧƽ�ⳣ�������������С�����䡱����
��ͼ�е�P1P2�����������������=������100��ʱƽ�ⳣ��Ϊ ��
�ܱ��ַ�Ӧ��ϵΪ100�棬5min�����������г���H2O��H2��0.5mol����ѧƽ�⽫���ƶ�����������ҡ���������
��2����ѹǿΪ0.1MPa�����£���a mol CO�� 3a mol H2�Ļ�������ڴ������������Է�������Ӧ��
CO��g��+2H2��g��CH3OH��g��
�ٸ÷�Ӧ�ġ�H0����S0�����������������=������
���������ݻ����䣬���д�ʩ�������COת���ʵ��� ��
A�������¶�
B����CH3OH��g������ϵ�з������
C������He��ʹ��ϵ��ѹǿ����
D���ٳ���1mol CO��3mol H2 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������NO2��Br2����������ʵ�鲻���е��ǣ� ��
A. ����ˮB. ͨ��CCl4
C. ͨ��NaOH��ҺD. ͨ��AgNO3��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ����գ�
��1��ʵ����ͨ����MnO2��Ũ���ᷴӦ��ȡ�������䷴Ӧ�Ļ�ѧ����ʽ�� �� ����1molCl2���ɣ���������HCl�����ʵ�����mol��
��2����������������Һ��Ӧ����ƫ���ᱵ����Ӧ�����ӷ���ʽΪ��
��3��������������������������������Ӧ�Ļ�ѧ����ʽΪ ��
��4�������Ƶ�ˮ��Һ�׳�ˮ������������ͨ�������CO2 �� ��������������������壬ͬʱ�õ�һ�����Σ�д�������εĻ�ѧʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ����������ȼ�ϵ����ˮ����ϵͳԭ����ͼ��ʾ��ͼ���л���ˮ���л������C6H10O5��ʾ�������й�˵����ȷ���ǣ� �� 
A.b�缫�Ϸ���������Ӧ
B.b�缫������Һ��pH����
C.a�缫��Ӧʽ��C6H10O5+24e��+7H2O�T6CO2��+24H+
D.�м��ң�Na+�������ң�Cl����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ����Ҫ�Ļ���ԭ�ϣ�ijѧϰС������ȡ������̽�������ʣ���ش�
��1��ʵ������ȡ�����Ļ�ѧ����ʽ�� ��
��2����С��ͬѧ�������ͼ��ʾ��ʵ��װ�ã����ּг�����δ��������̽�������Ļ�ԭ�Բ������� 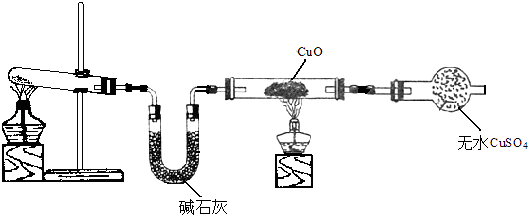
��ʵ������Ϊ����ɫCuO��Ϊ��ɫ����ɫˮCuSO4��ĩ��Ϊ��ɫ��ͬʱ����һ����ɫ���壬����������Ⱦ����д��������CuO��Ӧ�Ļ�ѧ����ʽ ��
�ڼ�ʯ�ҵ������� ��
��3����ͬѧ��Ϊ��NH3��CuO��Ӧ�ĺ�ɫ�����п��ܺ���Cu2O����֪��Cu2O��һ�ּ����������������Һ�У�Cu+���ȶ��Ա�Cu2+�Cu2O+2H+=Cu+Cu2++2H2O����̽��ʵ����ȡС����ɫ�������Թ��У����� �� ����Һ�г��� �� ��˵������Cu2O��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��ȷ���ǣ�������
A.��AgNO3��Һ�м���Cu�ۣ�Cu+Ag+�TCu2++2Ag
B.��CaCl2��Һ��ͨ��CO2��Ca2++CO2�TCaCO3��+2H+
C.����FeCl��Һ�����ˮ����Fe��OH��3���壺Fe3++3H2O ![]() Fe��OH��3�����壩+3H+
Fe��OH��3�����壩+3H+
D.CuSO4��Һ��Ba��OH��2��Һ��ϣ�Ba2++SO42���TBaSO4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ������������Ʊ�����������KI������Ũ���ᷴӦ��HI������Ũ�Ⱦ�Ϊ0.1 mol��L��1���Ȼ������������ƻ���Ʊ������������塡���ô����ʯ��ˮ���ռ���õķ����ǣ�������
A.��B.��
C.�ڢ�D.ȫ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com