
A、原子核中有6个中子的硼原子:
| ||
B、HCl的电子式: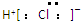 | ||
C、K+结构示意图: | ||
| D、HClO的结构式:H-O-Cl |
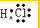 ,故B错误;
,故B错误;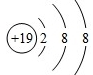 ,故C错误;
,故C错误; ,次氯酸的结构式为:H-O-Cl,故D正确;
,次氯酸的结构式为:H-O-Cl,故D正确;

科目:高中化学 来源: 题型:
| A、棉、麻、丝、合成纤维完全燃烧生成物中都含有CO2和H2O |
| B、日常生活中人们大量使用铝制品,是因为常温下铝不能与氧气反应 |
| C、兰州水污染苯超标是由于石油泄漏,污染物以烃类为主 |
| D、雾霾天车灯的通路属于丁达尔现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在食用盐中添加适量的碘酸钾 |
| B、用聚氯乙烯塑料袋包装食品 |
| C、在食品加工中科学使用食品添加剂 |
| D、研发高效低毒的农药,降低蔬菜的农药残留量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同时改变两个变量来研究反应速率的变化,能更快得出有关规律 |
| B、依据某化合物熔融状态能导电,推出此化合物中一定存在离子键 |
| C、依据丁达尔现象可将分散系分为溶液、胶体与浊液 |
| D、从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属递增的规律 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、图1表示pH相同的盐酸和醋酸加水稀释时溶液导电能力的变化 |
| B、图1表示物质的量浓度相同的盐酸和醋酸加水稀释时溶液导电能力的变化 |
| C、图2中,t℃时饱和溶液的质量分数为m% |
| D、图2中,若保持温度不变,可以通过添加溶质的方法使溶液组成从a点变为b点 |
查看答案和解析>>
科目:高中化学 来源: 题型:
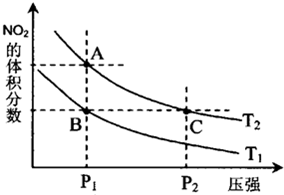 试运用所学知识,解决下列问题:
试运用所学知识,解决下列问题:| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
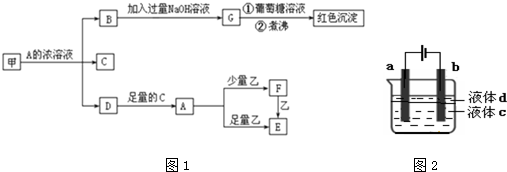
查看答案和解析>>
科目:高中化学 来源: 题型:
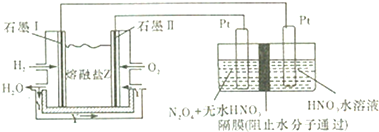
| A、石墨Ⅱ电极上发生反应的电极反应式为:O2+4e-+2CO2═2CO32- |
| B、在电解池中生成N2O5的电极反应式为:N2O4+2NO3--2e-═2N2O5 |
| C、放电时熔融盐中CO32-向石墨I电极方向移动 |
| D、每消耗11.2L氢气,理论上可以制得108g N2O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、装置Ⅰ可用于测定中和热 |
| B、装置Ⅱ装置放置一段时间后,饱和CuSO4溶液中不出现蓝色晶体 |
| C、装置Ⅲ中的石英坩埚可用于熔化氢氧化钠 |
| D、装置Ⅳ可用于吸收易溶于水的尾气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com