
【题目】炒过菜的铁锅未及时洗净(残液中含NaCl),不久便会因被腐蚀而出现红褐色锈斑。腐蚀原理如右图所示,下列说法正确的是

A. 腐蚀过程中,负极是C
B. Fe失去电子经电解质溶液转移给C
C. 正极的电极反应式为4OH―-4e-==2H2O+O2↑
D. 每生成1mol铁锈(Fe2O3·xH2O)理论上消耗标准状况下的O233.6L
【答案】D
【解析】该原电池中,Fe易失电子作负极、C作正极,负极上铁失电子生成亚铁离子,正极上氧气得电子发生还原反应,负极反应式为![]() 、正极反应式为O2+4e-+2H2O ==4OH―;从以上分析可以知道原电池反应,铁做负极被腐蚀,碳做正极,A错误;原电池中电子沿外导线从负极流向正极,不能通过电解质溶液,电解质溶液中是离子的定向移动形成闭合回路,B错误;正极电极反应是溶液中氧气得到电子发生还原反应,电极反应O2+4e-+2H2O ==4OH―,C错误;负极反应式为
、正极反应式为O2+4e-+2H2O ==4OH―;从以上分析可以知道原电池反应,铁做负极被腐蚀,碳做正极,A错误;原电池中电子沿外导线从负极流向正极,不能通过电解质溶液,电解质溶液中是离子的定向移动形成闭合回路,B错误;正极电极反应是溶液中氧气得到电子发生还原反应,电极反应O2+4e-+2H2O ==4OH―,C错误;负极反应式为![]() 、正极反应式为O2+4e-+2H2O ==4OH―,亚铁离子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁不稳定,被氧气氧化生成氢氧化铁,离子反应方程式为
、正极反应式为O2+4e-+2H2O ==4OH―,亚铁离子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁不稳定,被氧气氧化生成氢氧化铁,离子反应方程式为![]() 、化学方程式为
、化学方程式为![]() ,每生成
,每生成![]() 铁锈
铁锈![]() ,铁元素为2mol,根据铁元素守恒计算:2Fe -O2 2Fe(OH)24e- 根据上述反应关系可知,2molFe参加反应消耗氧气1mol,生成Fe(OH)2为2mol,再根据4Fe(OH)2O2关系可知,消耗2mol Fe(OH)2,消耗氧气为0.5 mol,理论上消耗标准状况下的氧气体积(1+0.5)×22.4=33.6L,D正确;正确选项D。
,铁元素为2mol,根据铁元素守恒计算:2Fe -O2 2Fe(OH)24e- 根据上述反应关系可知,2molFe参加反应消耗氧气1mol,生成Fe(OH)2为2mol,再根据4Fe(OH)2O2关系可知,消耗2mol Fe(OH)2,消耗氧气为0.5 mol,理论上消耗标准状况下的氧气体积(1+0.5)×22.4=33.6L,D正确;正确选项D。


科目:高中化学 来源: 题型:
【题目】下表列出了某短周期元素R的各级电离能数据(单位为kJ·mol-1)。下列关于元素R的判断中一定正确的是( )
I1 | I2 | I3 | I4 | …… | |
R | 577.5 | 1816.7 | 2744.8 | 11577 |
①R的主要化合价中最高正价为+3价 ②R元素位于元素周期表中第ⅡA族
③R元素第一电离能小于同周期相邻元素 ④R元素基态原子的电子排布式为1s22s22p1
A. ①② B. ②③ C. ③④ D. ①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的工业废水中含有大量的“FeSO4”、较多的Cu2+和少量的Na+。为了减少污染变废为宝,工厂计划从该废水中回收硫酸亚铁和铜。根据流程图,完成回收硫酸亚铁和铜的简单实验方案。回答下列问题:

(1)加入原料①为____________;操作②的名称为___________,该操作所用到的玻璃仪器主要有______。
(2)固体A为____________;
(3)写出加入原料①和②有关反应的离子方程式__________________、________________________。
(4)操作③获得FeSO4·7H2O,需要经过_____、_____、过滤等操作。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组同学用下列装置和试剂进行实验,探究O2与KI溶液发生反应的条件。
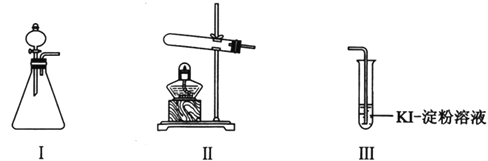
供选试剂:30% H2O2溶液、0.1mol/L H2SO4溶液、MnO2固体、KMnO4固体
(1)小组同学设计甲、乙、丙三组实验,记录如下:
操作 | 现象 | |
甲 | 向I的锥形瓶中加入______,.向I的______中加入30% H2O2溶液,连接I、Ⅲ,打开活塞 | I中产生无色气体并伴随大量白雾;Ⅲ中有气泡冒出,溶液迅速变蓝 |
乙 | 向Ⅱ中加入KMnO4固体,连接Ⅱ、Ⅲ,点燃酒精灯 | Ⅲ中有气泡冒出,溶液不变蓝 |
丙 | 向Ⅱ中加入KMnO4固体,Ⅲ中加入适量0.1mol/L H2SO4溶液,连接Ⅱ、Ⅲ,点燃酒精灯 | Ⅲ中有气泡冒出,溶液变蓝 |
(2)丙实验中O2与KI溶液反应的离子方程式是__________________________。
(3)对比乙、丙实验可知,O2与KI溶液发生反应的适宜条件是___________。为进一步探究该条件对反应速率的影响,可采取的实验措施是________。
(4)由甲、乙、丙三实验推测,甲实验可能是I中的白雾使溶液变蓝。学生将I中产生的气体直接通入下列________溶液(填序号),证明了白雾中含有H2O2。
A.酸性 KMnO4 B. FeCl2 C. Na2S D.品红
(5)资料显示:KI溶液在空气中久置过程中会被缓慢氧化:4KI +O2 +2H2O=2I2 + 4KOH。该小组同学取20 mL久置的KI溶液,向其中加入几滴淀粉溶液,结果没有观察到溶液颜色变蓝,他们猜想可能是发生了反应(写离子方程式)________________________造成的,请设计实验证明他们的猜想是否正确________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年5月,中国对“可燃冰”试采成功。“可燃冰”是天然气水合物,被称为未来新能源。回答下列问题:
(1)用Cu2Al2O4作催化剂制备乙酸
已知:![]() ,各物质相对能量大小如图。
,各物质相对能量大小如图。
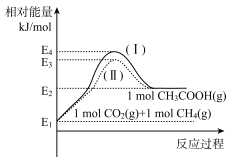
①a=____。
②反应物的活化分子浓度大小:过程I___ 过程Ⅱ(填“大于”、“小于”或“等于”)。
(2)甲烷超干催化重整(DRM)制备CO,在Ni、CaO及Fe3O4的共同催化作用下,可以获得极高浓度的CO,其机理如下:
第①步:Ni基催化![]()
第②步:Fe的还原![]()
第③步:CO2的捕获![]()
第④步:CO2的释放与还原![]()
设计第②步与第③步反应有利于实现氢物种与____的彻底分离,从勒夏特列原理的角度看,这也有利于____;过程①中,当投料比![]() = ___时,才能保持催化剂组成不变。
= ___时,才能保持催化剂组成不变。
(3)甲烷催化重整与压强的关系
已知:![]() ,现有温度相同的I、Ⅱ、Ⅲ三个恒压密闭容器,均已充入1 mol CH4(g)和1 mol CO2 (g),三个容器的反应压强分别为P1 atm、P2 atm、P3 atm,在其他条件相同的情况下,反应均进行到t min时,CO2)的平衡体积分数φ(CO2)如下左图,此时I、Ⅱ、Ⅲ三个容器中一定处于化学平衡状态的是 ___(填番号);求该温度条件下反应的平衡常数Kp=___ (计算表达式)。【已知:Kp是用分压力代替各物质的浓度计算的平衡常数,任一组分B的分压p(B)等于总压p乘以它的体积分数y(B)】
,现有温度相同的I、Ⅱ、Ⅲ三个恒压密闭容器,均已充入1 mol CH4(g)和1 mol CO2 (g),三个容器的反应压强分别为P1 atm、P2 atm、P3 atm,在其他条件相同的情况下,反应均进行到t min时,CO2)的平衡体积分数φ(CO2)如下左图,此时I、Ⅱ、Ⅲ三个容器中一定处于化学平衡状态的是 ___(填番号);求该温度条件下反应的平衡常数Kp=___ (计算表达式)。【已知:Kp是用分压力代替各物质的浓度计算的平衡常数,任一组分B的分压p(B)等于总压p乘以它的体积分数y(B)】
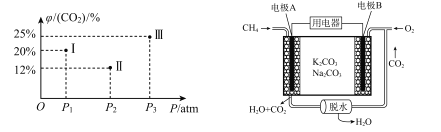
(4)甲烷用于燃料电池
已知:甲烷电池的工作原理如上有图,则负极反应方程式为 ___;当A极消耗标况下44.8 LCH4时,理论上B极转移电子的物质的量为 ___mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成。经查资料得知:Ag++ 2NH3·H2O![]() Ag(NH3)2+ 2H2O。下列分析不正确的是
Ag(NH3)2+ 2H2O。下列分析不正确的是
A. 浊液中存在沉淀溶解平衡:AgCl (s)![]() Ag+(aq)+Cl-(aq)
Ag+(aq)+Cl-(aq)
B. 实验可以证明NH3结合Ag+能力比Cl-强
C. 实验表明实验室可用氨水洗涤银镜反应后的试管
D. 由资料信息可推知:加浓硝酸后生成的沉淀为AgCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com