
����Ŀ������ֱ�������Ƽ״��Ǹ�����ս�ԵĿ��⣬Sen����CF3COOHˮ��Һ�гɹ�������ת��ΪCF3COOCH3(ˮ������CH3OH)���䷴Ӧ������ͼ��ʾ������˵����ȷ���ǣ� ��
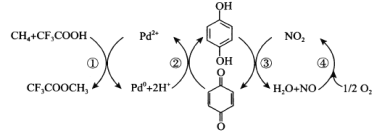
A.������Ӧ���ܷ�ӦʽΪCH4��CF3COOH��![]() O2��CF3COOCH3
O2��CF3COOCH3
B.CF3COOCH3ˮ������CH3OH�ķ�ӦʽΪCF3COOCH3��H2O��CF3COOH��CH3OH
C.Pd2���Ǹ÷�Ӧ���м����
D.ÿ����1molCH3OH�����ı�״����O2�����Ϊ22.4L
���𰸡�B
��������
A�����ݢ٢ڢܼۢӺͿɵ�������Ӧ���ܷ�ӦʽΪCH4��CF3COOH��![]() O2��CF3COOCH3+H2O����Aѡ�����
O2��CF3COOCH3+H2O����Aѡ�����
B��CF3COOCH3����ˮ�ⷴӦ�IJ���ΪCF3COOH��CH3OH��������CH3OH�ķ�ӦʽΪCF3COOCH3��H2O��CF3COOH��CH3OH����Bѡ����ȷ��
C����Ӧ����Pd2�����뷴Ӧ����Ӧ���������ɵ����ʵ�����Pd2������Pd2��Ϊ���������м�����Cѡ�����
D�����ݷ�ӦCH4��CF3COOH��![]() O2��CF3COOCH3+H2O��CF3COOCH3��H2O��CF3COOH��CH3OH�ɵ��Ƽ״��ķ�Ӧ����ʽΪCH4��
O2��CF3COOCH3+H2O��CF3COOCH3��H2O��CF3COOH��CH3OH�ɵ��Ƽ״��ķ�Ӧ����ʽΪCH4��![]() O2��CH3OH����ÿ����1molCH3OH�����ı�״����O2�����Ϊ11.2L����Dѡ�����
O2��CH3OH����ÿ����1molCH3OH�����ı�״����O2�����Ϊ11.2L����Dѡ�����
�ʴ�ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijԪ�ص�һ��ͬλ��X��ԭ��������ΪA����N�����ӣ�����![]() ԭ�����HmX���ӣ���a��HmX���������ӵ����ʵ����ǣ� ��
ԭ�����HmX���ӣ���a��HmX���������ӵ����ʵ����ǣ� ��
A. ![]() (A-N+m)molB.
(A-N+m)molB. ![]() (A-N)molC.
(A-N)molC. ![]() (A-N)molD.
(A-N)molD. ![]() (A-N+m)mol
(A-N+m)mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮ��ɽ���ǽ�ɽ��ɽ��������������ɫ��չ����̬������Ϊ�й�չʾ�������һ��������Ƭ����
��1�����Ṥҵ�ų���β������Ҫ��SO2���ж��ִ�����ʽ��
��д���ù�����ˮ����β�������ӷ���ʽ��___________________��
��β��Ҳ�������̿�MnO2�����գ�д����ͼ��ʾ����Ӧ1���Ļ�ѧ����ʽ��___________________��
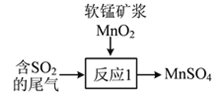
��2����������β����NO��CO�ķ���֮һ������������������װһ����ת��װ�ã�ʹNO��CO�ڴ���������ת��Ϊ�����ʡ�д���÷�Ӧ�Ļ�ѧ����ʽ��___________________��
��3��ij�������ۺϴ�����NH��ˮ��ҵ��������Ҫ��N2��Cl2��NO����������������̣�

������Ӧ1����������Cl2������Ӧ1���Ļ�ѧ����ʽΪ___________________��
�� ����Ӧ2�������ӷ���ʽΪ___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���Ӧ![]() +H2O
+H2O![]() H2CO3+OH��ƽ�ⳣ��K=2.2��108����NH4HCO3��Һ�Ͱ�ˮ��һ��������ϣ������ڽ�ȡ�����е�ZnO������Һ������������仯�ɺ��ԣ�����ʱ����ָ����Һ�������ʵ���Ũ�ȹ�ϵ��ȷ����
H2CO3+OH��ƽ�ⳣ��K=2.2��108����NH4HCO3��Һ�Ͱ�ˮ��һ��������ϣ������ڽ�ȡ�����е�ZnO������Һ������������仯�ɺ��ԣ�����ʱ����ָ����Һ�������ʵ���Ũ�ȹ�ϵ��ȷ����
A.0.2mol��L1��ˮ��c��NH3��H2O��>c��NH4+��>c��OH��>c��H+��
B.0.2mol��L1NH4HCO3��Һ��pH>7����c��NH4+��>c��HCO3-��>c��H2CO3��>c��NH3��H2O��
C.0.2mol��L1��ˮ��0.2mol��L1NH4HCO3��Һ�������ϣ�c��NH4+��+c��NH3��H2O��=c��H2CO3��+c��HCO3-��+c��CO32-��
D.0.6mol��L1��ˮ��0.2mol��L1NH4HCO3��Һ�������ϣ�c��NH3��H2O��+c��CO32-��+c��OH��=0.3mol��L1+c��H2CO3��+c��H+��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ������ͼװ�ý�����Ȫʵ�飬��֪Բ����ƿ�ڳ���X���壬��ͷ�ι���װ������YҺ�壬�ձ���װ������ZҺ�壬��������ܽ�����Ȫʵ��������Һ��һ���ܳ���������ƿ����
X���� | Y�Լ� | Z�Լ� | |
A | NO2 | H2O | H2O |
B | HCl | H2O | H2O |
C | HCl��O2������� | H2O | H2O |
D | NH3��N2������� | H2O | H2O |

A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڸ��������£��������ʼ��ת������ʵ�ֵ��У� ��
��NaHCO3(s)![]() Na2CO3(s)
Na2CO3(s)![]() NaOH(aq)
NaOH(aq)
��Al(s)![]() NaAlO2(aq)
NaAlO2(aq)![]() Al(OH)3(s)
Al(OH)3(s)
��AgNO3(aq)![]() [Ag(NH2)2]+(aq)
[Ag(NH2)2]+(aq)![]() Ag(s)
Ag(s)
��Fe2O3(s)![]() Fe(s)
Fe(s)![]() FeCl3(aq)
FeCl3(aq)
��NaCl(aq)![]() Cl2(g)
Cl2(g)![]() FeCl2(s)
FeCl2(s)
��MgCl2(aq)![]() Mg(OH)2(s)
Mg(OH)2(s)![]() MgO (s)
MgO (s)
��N2(g)![]() NH3(g)
NH3(g)![]() Na2CO3(s)
Na2CO3(s)
A.2��B.3��C.4��D.5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪2SO2(g)+O2(g)![]() 2SO3(g) ��H ����197kJ��mol��1����ͬ�¡�ͬ����������ܱ������зֱ�������壺(��)2molSO2��1molO2��(��)1molSO2��0.5molO2��(��)2molSO3��1molO2�����¡������·�Ӧ��ƽ��ʱ�����й�ϵһ����ȷ���ǣ� ��
2SO3(g) ��H ����197kJ��mol��1����ͬ�¡�ͬ����������ܱ������зֱ�������壺(��)2molSO2��1molO2��(��)1molSO2��0.5molO2��(��)2molSO3��1molO2�����¡������·�Ӧ��ƽ��ʱ�����й�ϵһ����ȷ���ǣ� ��
A.������ѹǿP��P����P����2P��
B.����������ʵ���n��n����n����n��
C.SO3����������ӣ�����������������
D.��Ӧ��������ֵQ��197��Q����Q����Q��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ΰ��Ͻ����ĸ���Һ�䷴Ӧ��Сʵ�飬���Ӧ��Ӧ�����ӷ���ʽ��д��ȷ����(����)
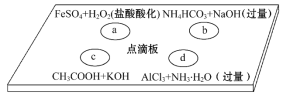
A. a��Ӧ��Fe2����2H����H2O2=Fe3����2H2O
B. b��Ӧ��HCO3-��OH��=CO32-��H2O
C. c��Ӧ��H����OH��=H2O
D. d��Ӧ��Al3����3NH3��H2O=Al(OH)3����3NH4+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ�����в�������500mL 0.200mol��L��1 Na2CO3��Һ����ش��й����⡣
ʵ�鲽�� | �й����� |
(1)��������Na2CO3������ | ��ҪNa2CO3������Ϊ_________g�� |
(2)����Na2CO3���� | ������������Ҫ�õ���������_____ |
(3)��Na2CO3����100mL�ձ��� | Ϊ�ӿ��ܽ����ʣ��ɲ�ȡ�Ĵ�ʩ��___ |
(4)���ձ��е���Һת����500mL����ƿ�� | Ϊ��ֹ��Һ������Ӧ��ȡ�Ĵ�ʩ��____________________________________________________________________________ |
(5)������ƿ�м�����ˮ���̶��� | �ڽ��д˲���ʱӦע���������______ |
(6)����Ϊ�������������Ƶ�Na2CO3��Һ��Ũ���Ƿ�Ϊ0.200mol��L��1����˵�����ɡ�________
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com