
【题目】室温下,反应![]() +H2O
+H2O![]() H2CO3+OH的平衡常数K=2.2×108。将NH4HCO3溶液和氨水按一定比例混合,可用于浸取废渣中的ZnO。若溶液混合引起的体积变化可忽略,室温时下列指定溶液中微粒物质的量浓度关系正确的是
H2CO3+OH的平衡常数K=2.2×108。将NH4HCO3溶液和氨水按一定比例混合,可用于浸取废渣中的ZnO。若溶液混合引起的体积变化可忽略,室温时下列指定溶液中微粒物质的量浓度关系正确的是
A.0.2mol·L1氨水:c(NH3·H2O)>c(NH4+)>c(OH)>c(H+)
B.0.2mol·L1NH4HCO3溶液(pH>7):c(NH4+)>c(HCO3-)>c(H2CO3)>c(NH3·H2O)
C.0.2mol·L1氨水和0.2mol·L1NH4HCO3溶液等体积混合:c(NH4+)+c(NH3·H2O)=c(H2CO3)+c(HCO3-)+c(CO32-)
D.0.6mol·L1氨水和0.2mol·L1NH4HCO3溶液等体积混合:c(NH3·H2O)+c(CO32-)+c(OH)=0.3mol·L1+c(H2CO3)+c(H+)
【答案】BD
【解析】
A.NH3H2O属于弱电解,部分电离,氨水中存在的电离平衡有:NH3H2O![]() NH4++OH-,H2O
NH4++OH-,H2O![]() H++OH-,所以c(OH-)>c(NH4+),选项A错误;
H++OH-,所以c(OH-)>c(NH4+),选项A错误;
B.NH4HCO3溶液显碱性,说明HCO3-的水解程度大于NH4+的水解,所以c(NH4+)>c(HCO3-),HCO3-水解:H2O+HCO3-![]() H2CO3+OH-,NH4+水解:NH4++H2O
H2CO3+OH-,NH4+水解:NH4++H2O![]() NH3H2O+H+,前者水解程度大,则c(H2CO3)>c(NH3H2O),选项B正确;
NH3H2O+H+,前者水解程度大,则c(H2CO3)>c(NH3H2O),选项B正确;
C.由物料守恒,n(N):n(C)=2:1,则有c(NH4+)+c(NH3H2O)=2[c(H2CO3)+c(HCO3-)+c(CO32-)],选项C错误;
D.由物料守恒,n(N):n(C)=4:1,则有c(NH4+)+c(NH3H2O)=4[c(H2CO3)+c(HCO3-)+c(CO32-)]①;电荷守恒有:c(NH4+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)②;结合①②消去c(NH4+)得:c(NH3H2O)+c(OH-)=c(H+)+4c(H2CO3)+3c(HCO3-)+2c(CO32-)③,0.2mol/LNH4HCO3与氨水等体积混合后,c(NH4HCO3)=0.1mol/L,由碳守恒有,c(H2CO3)+c(HCO3-)+c(CO32-)=0.1mol/L④,将③等式两边各加一个c(CO32-),则有c(NH3H2O)+c(OH-)+c(CO32-)=c(H+)+c(H2CO3)+3c(H2CO3)+3c(HCO3-)+3c(CO32-),将④带入③中得,c(NH3H2O)+c(OH-)+c(CO32-)=c(H+)+3c(H2CO3)+0.3mol/L,选项D正确;
答案选BD。


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
【题目】下列关于物质结构的命题中,错误的项数有
①CH3COOH分子中碳原子的杂化类型有sp2和sp3两种
②元素Ge位于周期表第四周期IVA族,核外电子排布式为 [Ar]4s24p2,属于P区
③非极性分子往往具有高度对称性,如BF3、PCl5、H2O2、CO2这样的分子
④冰中存在极性共价键和氢键两种化学键的作用
⑤Cu(OH)2是一种蓝色絮状沉淀,既溶于硝酸、氨水,也能溶于硫酸氢钠溶液中
⑥熔融态的HgCl2不导电,HgCl2稀溶液有弱的导电能力说明固态HgCl2是分子晶体,为非电解质
⑦氨水中大部分NH3与H2O以氢键(用“...”表示)结合成NH3.H2O分子,根据氨水的性质可知NH3.H2O的结构式可记为:
A. 4项 B. 5项 C. 6项 D. 7项
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】央视网2019年6月17日报道,针对近年来青蒿素在全球部分地区出现的“抗药性”难题,我国著名药学家、诺贝尔生理学或医学奖获得者屠呦呦及其团队,经过多年攻坚,提出应对“青蒿素抗药性”难题的切实可行治疗方案。从青蒿(粉末)中提取青蒿素的方法以萃取原理为基础,主要有乙醚浸提法和汽油浸提法。青蒿素为白色针状晶体,易溶于乙醇、乙醚、苯和汽油等有机溶剂,不溶于水,熔点为156~157℃,沸点为389.9℃,热稳定性差,汽油浸提法的主要工艺流程如下图所示。
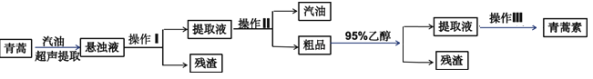
注:汽油的沸点为40~200℃。回答下列问题:
(1)超声提取的原理是在强大的超声波作用下,使青蒿细胞乳化、击碎、扩散,超声波提取的优点是___________、时间短、温度低等。
(2)操作1的名称为________,如图所示为操作Ⅱ的实验装置图(部分夹持装置已略),图中A、B、C、D错误的是_______(填标号)。
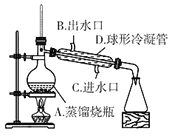
(3)已知青蒿素在95%乙醇中的溶解度随温度的升高而升高,则操作Ⅲ为____________、过滤、洗涤、干燥。
(4)通过控制其他实验条件不变,来研究原料粒度、提取时间和提取温度对青蒿素提取速率的影响,其结果如下图所示,采用的最佳原料粒度、提取时间和提取温度分别为________。
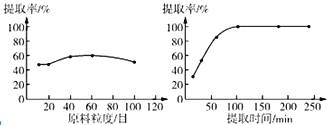
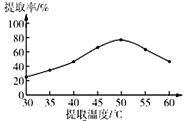
(5)将青蒿素加入滴有酚酞的NaOH溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与_________ (填标号)具有相似的性质。
A 乙醇 B 乙酸甲酯 C 乙醛 D 果糖
(6)已知青蒿素的分子式为C15H22O5(相对分子质量为282),将28.2g青蒿素样品在燃烧管中充分燃烧,将燃烧后的产物依次通过盛有足量P2O5和碱石灰的干燥管,盛有碱石灰干燥管增重的质量为______g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A.7.8 g的Na2S和Na2O2的混合物中含有阴、阳离子总数为0.3 NA
B.常温常压下,22.4 LCO2中含有NA个CO2分子
C.1.0 L 1.0 mol·L-1的NaClO水溶液中含有的氧原子数为NA
D.常温常压下,18 g羟基(-O2H)中所含的中子数为8 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】S2Cl2是橙黄色液体,少量泄漏会产生窒息性气体,喷水雾可减慢其挥发,并产生酸性悬浊液。其分子结构如图所示。下列关于S2Cl2的说法中错误的是( )

A.S2Cl2为非极性分子
B.分子中既含有极性键又含有非极性键
C.与S2Br2结构相似,熔、沸点S2Br2>S2Cl2
D.与水反应的化学方程式可能为2S2Cl2+2H2O===SO2↑+3S↓+4HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制氢气的一个重要反应是:CO(g) +H2O(g)== CO2(g)+H2(g)。
已知在25℃时:
①C(s)+![]() O2(g)
O2(g)![]() CO(g) ΔH1=111kJ·mol 1
CO(g) ΔH1=111kJ·mol 1
②H2(g)+![]() O2(g)== H2O(g) ΔH2=242kJ·mol 1
O2(g)== H2O(g) ΔH2=242kJ·mol 1
③C(s)+O2(g) == CO2(g) ΔH3=394kJ·mol 1
下列说法不正确的是
A. 25℃时,CO(g)+H2O(g)==CO2(g)+H2(g) ΔH=41kJ·mol1
B. 增大压强,反应①的平衡向逆反应方向移动,平衡常数K减小
C. 反应①达到平衡时,每生成1molCO的同时生成0.5molO2
D. 反应②断开2molH2和1molO2中的化学键所吸收的能量比形成4molO-H键所放出的能量少484kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷直接氧化制甲醇是富有挑战性的课题,Sen等在CF3COOH水溶液中成功将甲烷转化为CF3COOCH3(水解生成CH3OH),其反应机理如图所示,下列说法正确的是( )
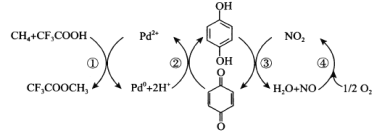
A.上述反应的总反应式为CH4+CF3COOH+![]() O2→CF3COOCH3
O2→CF3COOCH3
B.CF3COOCH3水解生成CH3OH的反应式为CF3COOCH3+H2O→CF3COOH+CH3OH
C.Pd2+是该反应的中间产物
D.每生成1molCH3OH,消耗标准状况下O2的体积为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烟气脱硫脱硝是环境治理的热点问题。
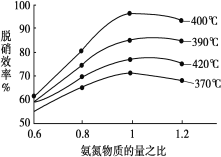
(1)氧化还原法脱硝:4NO(g)+4NH3(g)+O2(g)=4N2(g)+6H2O(g)ΔH=-1627.2kJ/mol。检验脱硝效果的重要指标是脱硝效率(脱硝过程中单位时间内NOx浓度变化占烟气初始浓度的百分比)。影响SCR系统脱硝效率的因素有很多,根据如图判断提高脱硝效率的最佳条件是__;氨氮比一定时,随温度的升高脱硝效率增大,其可能的原因是___。
(2)H2Y2-与Fe2+形成的络合物FeY2-可用于吸收烟气中的NO。原理:FeY2-(aq)+NO(g)![]() FeY2-(NO)(aq)ΔH<0
FeY2-(NO)(aq)ΔH<0
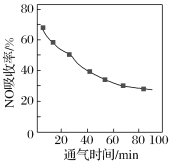
①将含NO的烟气以一定的流速通入起始温度为50℃的FeY2-溶液中。NO吸收率随通入烟气的时间变化如图。时间越长,NO吸收率越低的原因是___。
②生成的FeY2-(NO)(aq)可通过加入铁粉还原再生,其原理为FeY2-(NO)(aq)+Fe+H2O→FeY2-(aq)+Fe(OH)2+NH3(未配平)。若吸收液再生消耗14 g铁粉,则所吸收的烟气中含有NO的物质的量为__mol。
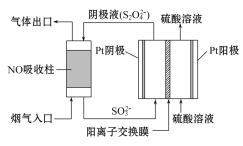
(3)以连二硫酸盐(S2O42-)为媒介,使用间接电化学法也可处理NO,装置如图所示:阴极的电极反应式为___。
(4)KMnO4/CaCO3浆液可协同脱硫,在反应中MnO4-被还原为MnO42-。
①KMnO4脱硫(SO2)的离子方程式为____。
②加入CaCO3的作用是___。
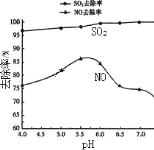
(5)利用NaClO2/H2O2酸性复合吸收剂可同时对NO、SO2进行氧化得到硝酸和硫酸而除去。在温度一定时,溶液pH对脱硫脱硝的影响如图所示:图中SO2的去除率随pH的增大而增大,而NO的去除率在pH>5.5时反而减小,请解释二者去除率不同的可能原因是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学用语表示正确的是 ( )
A.次氯酸的结构式:H-Cl-O
B.16O2-和18O2-的结构示意图:![]()
C.氮气的电子式:![]()
D.电子式表示氯化钠的形成过程:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com