
����Ŀ���������������ǻ����������ȵ����⡣
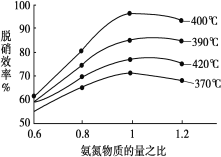
��1��������ԭ��������4NO(g)��4NH3(g)��O2(g)��4N2(g)��6H2O(g)��H��-1627.2kJ/mol����������Ч������Ҫָ��������Ч�ʣ����������е�λʱ����NOxŨ�ȱ仯ռ������ʼŨ�ȵİٷֱȣ���Ӱ��SCRϵͳ����Ч�ʵ������кܶ࣬������ͼ�ж��������Ч�ʵ����������__��������һ��ʱ�����¶ȵ���������Ч����������ܵ�ԭ����___��
��2��H2Y2����Fe2���γɵ������FeY2�����������������е�NO��ԭ����FeY2��(aq)��NO(g)![]() FeY2��(NO)(aq)��H<0
FeY2��(NO)(aq)��H<0
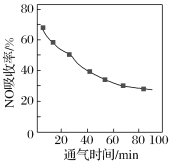
�ٽ���NO��������һ��������ͨ����ʼ�¶�Ϊ50���FeY2����Һ�С�NO��������ͨ��������ʱ��仯��ͼ��ʱ��Խ����NO������Խ�͵�ԭ����___��
�����ɵ�FeY2��(NO)(aq)��ͨ���������ۻ�ԭ��������ԭ��ΪFeY2��(NO)(aq)��Fe��H2O��FeY2��(aq)��Fe(OH)2��NH3(δ��ƽ)��������Һ��������14 g���ۣ��������յ������к���NO�����ʵ���Ϊ__mol��
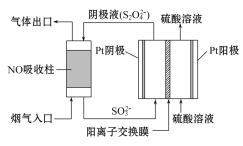
��3��������������(S2O42��)Ϊý�飬ʹ�ü�ӵ绯ѧ��Ҳ�ɴ���NO��װ����ͼ��ʾ�������ĵ缫��ӦʽΪ___��
��4��KMnO4/CaCO3��Һ��Эͬ�����ڷ�Ӧ��MnO4������ԭΪMnO42����
��KMnO4����(SO2)�����ӷ���ʽΪ____��
�ڼ���CaCO3��������___��
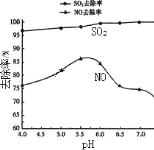
��5������NaClO2/H2O2���Ը������ռ���ͬʱ��NO��SO2���������õ�������������ȥ�����¶�һ��ʱ����ҺpH������������Ӱ����ͼ��ʾ��ͼ��SO2��ȥ������pH�����������NO��ȥ������pH��5.5ʱ������С������Ͷ���ȥ���ʲ�ͬ�Ŀ���ԭ����__��
���𰸡��¶�400�棬�������ʵ�����Ϊ1 �����¶ȣ���Ӧ���ʼӿ� ��Ӧ���ȣ��¶����ߣ�ƽ�������ƶ���������NO�����գ����ŷ�Ӧ���У�FeY2��Ũ�Ƚ��� 0.1 mol 2SO32-+4H++2e=S2O42-+2H2O 2MnO4��+SO2 +2H2O=2MnO42��+SO42��+4H+ ���ķ�Ӧ(����)���������ɵ�H+�������ڷ�Ӧ������� ����pH��������SO2�ױ���Һ���գ�pH����NO�Ļ�ԭ�Խ��ͻ�H2O2��NaClO2�����Լ��������ܽ�NO����Ϊ����
��������
����������ԭ��Ӧ�ó��������ͻ�ԭ���ı�����ϵ��������ԭ��Ӧԭ��д���ӷ���ʽ�����ɵ������Ӻ�̼��Ʒ�Ӧ�����������ӣ�����ƽ�������ƶ������ݱ�����ϵ�ó�������غ�̼��Ƶı�����ͼ����Ϣ�ó��������������������������ԭ��Ӧ��ǿ����pH�仯��Ӱ�����������ԭ���ݴ˷������н��
��1��ͼ�����¶�400�棬�������ʵ�����Ϊ1ʱ����Ч����ߣ�Ч����ѣ��¶����߷�Ӧ���ʻ����ӣ�������Ч�ʻ����ߡ�
��2������ʼ�¶�Ϊ50�棬��Ӧʱ��Խ���¶����ߣ�������Ӧ���ȣ��¶�����ʱƽ�������ƶ���������NO�����գ����ŷ�Ӧ���У�FeY2��Ũ�Ƚ��͡����ʱ��Խ����NO������Խ�͡�
�ڷ�Ӧ��FeY2��(NO)(aq)��NԪ����+2�۽��͵���3�ۣ�Fe�Ļ��ϼ���0�����ߵ�+2�ۣ���Fe��NO=5��2��������Һ��������14 g����Ϊ0.25mol�������յ�NO�����ʵ���=0.25mol��5��2=0.1 mol��
��3����ͼ��֪��������ͨ��Һ����Ҫ��SO32-��������Ҫ��S2O42-�������������缫��ӦʽΪ2SO32-+4H++2e-��S2O42-+2H2O��
��4��KMnO4����(SO2)��Ӧ��MnO4������ԭΪMnO42����2MnO4��+SO2 +2H2O=2MnO42��+SO42��+4H+����Ӧ��H+���ɣ�����̼��ƿ��������ɵ�H+��Ӧ���ٽ���Ӧ������С�
��5������ͼ�е�ת���ʺ�ȥ���ʹ�ϵ������pH����SO2����Һ���գ���ȥ��������NO��pH��5.5ʱNO��ȥ���ʼ�С��������NO��ԭ�Լ�������NaClO2��H2O2�������Լ��������ܽ�NO����Ϊ���ᡣ


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ļ�����Ӧ�ù㷺����������������Ҫ�Ŀ�����Ⱦ�Ӧ�������ŷš�
��1����CO2��NH3�ɺϳɵ�������[CO(NH2)2]
��֪����2NH3(g)+CO2(g)=NH2CO2NH4 (s) ��H=-151.5 kJ��mol-1
��NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ��H=+120.5 kJ��mol-1
��H2O(l)=H2O(g) ��H=+44 kJ��mol-1
��CO2��NH3�ϳ����أ���������Һ̬ˮ�����Ȼ�ѧ����ʽΪ______________________
��2����ҵ�ϳ������·�Ӧ���������������Ⱦ��CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) ��H�����¶�ΪT1��T2ʱ���ֱ�0.40molCH4��0.9molNO2�������Ϊ1L���ܱ������У�n��CH4���淴Ӧʱ��ı仯��ͼ��ʾ��
N2(g)+CO2(g)+2H2O(g) ��H�����¶�ΪT1��T2ʱ���ֱ�0.40molCH4��0.9molNO2�������Ϊ1L���ܱ������У�n��CH4���淴Ӧʱ��ı仯��ͼ��ʾ��
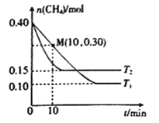
�ٸ���ͼ�жϸ÷�Ӧ����H______0������������������������������
���¶�ΪT1ʱ��0��10min��NO2��ƽ����Ӧ����v��NO2��=__________����Ӧ��ƽ�ⳣ��K=_________ ��
�۸÷�Ӧ�ﵽƽ���Ϊ����߷�Ӧ����ͬʱ���NO2��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��______�����ţ���
A�����ø�Ч���� B������CH4��Ũ�� C����С��������� D�������¶�
��3������ԭ��ط�Ӧ��ʵ��NO2���������ܷ�ӦΪ6NO2+8NH3=7N2+12H2O���������ҺΪHCl��Һ������һ��ʱ������ĵ缫��ӦʽΪ________________��
��4������һ���⻯��HN3����ˮ��Һ������������ƣ���NaN3��Һ�и�����Ũ���ɴ�С��˳��Ϊ________________�������£���amol/L��Ba(OH) 2 ��bmol/L��HN3��Һ�������ϣ���ַ�Ӧ����Һ�д���2c(Ba2+)=c��N3-���������Һ��c(HN3)=_________ mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���Ӧ![]() +H2O
+H2O![]() H2CO3+OH��ƽ�ⳣ��K=2.2��108����NH4HCO3��Һ�Ͱ�ˮ��һ��������ϣ������ڽ�ȡ�����е�ZnO������Һ������������仯�ɺ��ԣ�����ʱ����ָ����Һ�������ʵ���Ũ�ȹ�ϵ��ȷ����
H2CO3+OH��ƽ�ⳣ��K=2.2��108����NH4HCO3��Һ�Ͱ�ˮ��һ��������ϣ������ڽ�ȡ�����е�ZnO������Һ������������仯�ɺ��ԣ�����ʱ����ָ����Һ�������ʵ���Ũ�ȹ�ϵ��ȷ����
A.0.2mol��L1��ˮ��c��NH3��H2O��>c��NH4+��>c��OH��>c��H+��
B.0.2mol��L1NH4HCO3��Һ��pH>7����c��NH4+��>c��HCO3-��>c��H2CO3��>c��NH3��H2O��
C.0.2mol��L1��ˮ��0.2mol��L1NH4HCO3��Һ�������ϣ�c��NH4+��+c��NH3��H2O��=c��H2CO3��+c��HCO3-��+c��CO32-��
D.0.6mol��L1��ˮ��0.2mol��L1NH4HCO3��Һ�������ϣ�c��NH3��H2O��+c��CO32-��+c��OH��=0.3mol��L1+c��H2CO3��+c��H+��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڸ��������£��������ʼ��ת������ʵ�ֵ��У� ��
��NaHCO3(s)![]() Na2CO3(s)
Na2CO3(s)![]() NaOH(aq)
NaOH(aq)
��Al(s)![]() NaAlO2(aq)
NaAlO2(aq)![]() Al(OH)3(s)
Al(OH)3(s)
��AgNO3(aq)![]() [Ag(NH2)2]+(aq)
[Ag(NH2)2]+(aq)![]() Ag(s)
Ag(s)
��Fe2O3(s)![]() Fe(s)
Fe(s)![]() FeCl3(aq)
FeCl3(aq)
��NaCl(aq)![]() Cl2(g)
Cl2(g)![]() FeCl2(s)
FeCl2(s)
��MgCl2(aq)![]() Mg(OH)2(s)
Mg(OH)2(s)![]() MgO (s)
MgO (s)
��N2(g)![]() NH3(g)
NH3(g)![]() Na2CO3(s)
Na2CO3(s)
A.2��B.3��C.4��D.5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪2SO2(g)+O2(g)![]() 2SO3(g) ��H ����197kJ��mol��1����ͬ�¡�ͬ����������ܱ������зֱ�������壺(��)2molSO2��1molO2��(��)1molSO2��0.5molO2��(��)2molSO3��1molO2�����¡������·�Ӧ��ƽ��ʱ�����й�ϵһ����ȷ���ǣ� ��
2SO3(g) ��H ����197kJ��mol��1����ͬ�¡�ͬ����������ܱ������зֱ�������壺(��)2molSO2��1molO2��(��)1molSO2��0.5molO2��(��)2molSO3��1molO2�����¡������·�Ӧ��ƽ��ʱ�����й�ϵһ����ȷ���ǣ� ��
A.������ѹǿP��P����P����2P��
B.����������ʵ���n��n����n����n��
C.SO3����������ӣ�����������������
D.��Ӧ��������ֵQ��197��Q����Q����Q��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Һ������X�����ļ����ͨ�뵽һ������Y��Һ�У�Y��Һ��������������X�����ʵ����Ĺ�ϵ��������ͼ��ʾ���� ��

A.XΪNaOH��Һ��YΪAlCl3��Һ
B.XΪCO2��YΪCa(OH)2��Һ
C.XΪNH3��YΪAl2(SO4)3��Һ
D.XΪHCl��YΪNa[Al(OH)4]��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ΰ��Ͻ����ĸ���Һ�䷴Ӧ��Сʵ�飬���Ӧ��Ӧ�����ӷ���ʽ��д��ȷ����(����)
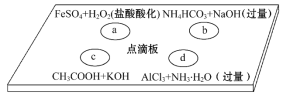
A. a��Ӧ��Fe2����2H����H2O2=Fe3����2H2O
B. b��Ӧ��HCO3-��OH��=CO32-��H2O
C. c��Ӧ��H����OH��=H2O
D. d��Ӧ��Al3����3NH3��H2O=Al(OH)3����3NH4+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£���һ���������ܱ������г���1molN2��3molH2���������з�Ӧ��N2(g)+3H2(g)2NH3(g)����Ӧ�ﵽƽ��ı�����������NH3����ƽ��Ũ�Ȳ��ı���ǣ� ��
A.�����¶Ⱥ�����ѹǿ���䣬����1molNH3(g)
B.�����¶Ⱥ�����������䣬����1molNH3(g)
C.�����¶Ⱥ�����ѹǿ���䣬����1molN2(g)
D.�����¶Ⱥ�����ѹǿ���䣬����1molAr(g)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ȼ�����(S2Cl2)��һ����Ҫ�Ļ���ԭ�ϣ��������������ı��������ȷ�ճ�������Ӳ�����ʡ��������Ͽ�֪S2Cl2�����������ʣ�
�������� | ���� | ɫ̬ | �ӷ��� | �۵� | �е� |
�綾 | ���ɫҺ�� | �ӷ� | ��76�� | 138�� | |
��ѧ���� | ��300��������ȫ�ֽ⣻ ��S2Cl2+Cl2 �������Ȼ�������Ӵ���������ȼ�յ�Σ�գ� �����Ȼ���ˮ�ֽ���ȣ��ų���ʴ�������� | ||||
��1����ȡ����S2Cl2
ʵ���ҿ�������������������110��140�淴Ӧ�Ƶ�S2Cl2��Ʒ��
������m������Ϊ___��װ��F���Լ���������___��
��װ������˳��A��___��E��D��
��ʵ��ǰ��K1��ͨ��һ��ʱ��ĵ����ž�װ���ڿ�����ʵ�����ֹͣ���Ⱥ���ͨ��һ��ʱ��ĵ�������Ŀ����___��
��Ϊ�����S2Cl2�Ĵ��ȣ�ʵ��Ĺؼ��ǿ��ƺ��¶Ⱥ�___��
��2����S2Cl2��ˮǿ�ҷ�Ӧ�������������������һ������X��ʹƷ����Һ��ɫ�����Ⱥ��ָֻ�ԭ״���ҷ�Ӧ������ֻ��һ��Ԫ�ػ��ϼ۷����仯��д���÷�Ӧ�Ļ�ѧ����ʽ___��
�ڼ�ͬѧΪ����֤������������ˮ�����ɵ���������ͨ����������ϡ����Ļ����Һ��Ʒ����Һ��NaOH ��Һ���÷���___������С������С�����ԭ����___��
��3��ijͬѧΪ�˲ⶨS2Cl2��ˮ��Ӧ�����ɵ�����X�ڻ�������е�������������������ʵ�鷽����

��W��Һ������___(����)��
a��H2O2��Һ b��KMnO4��Һ(�����ữ) c����ˮ
�ڸû������������X���������Ϊ____(�ú�V��m��ʽ�ӱ�ʾ)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com