
【题目】氮的化合物应用广泛,但氮氧化物是重要的空气污染物,应降低其排放。
(1)用CO2和NH3可合成氮肥尿素[CO(NH2)2]
已知:①2NH3(g)+CO2(g)=NH2CO2NH4 (s) △H=-151.5 kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) △H=+120.5 kJ·mol-1
③H2O(l)=H2O(g) △H=+44 kJ·mol-1
用CO2和NH3合成尿素(副产物是液态水)的热化学方程式为______________________
(2)工业上常用如下反应消除氮氧化物的污染:CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) △H,在温度为T1和T2时,分别将0.40molCH4和0.9molNO2充入体积为1L的密闭容器中,n(CH4)随反应时间的变化如图所示:
N2(g)+CO2(g)+2H2O(g) △H,在温度为T1和T2时,分别将0.40molCH4和0.9molNO2充入体积为1L的密闭容器中,n(CH4)随反应时间的变化如图所示:
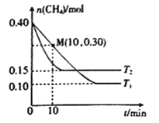
①根据图判断该反应的△H______0(填“>”、“<”或“=”)。
②温度为T1时,0~10min内NO2的平均反应速率v(NO2)=__________,反应的平衡常数K=_________ 。
③该反应达到平衡后,为在提高反应速率同时提高NO2的转化率,可采取的措施有______(填标号)。
A.改用高效催化剂 B.增加CH4的浓度 C.缩小容器的体积 D.升高温度
(3)利用原电池反应可实现NO2的无害化,总反应为6NO2+8NH3=7N2+12H2O,电解质溶液为HCl溶液,工作一段时间后,负极的电极反应式为________________。
(4)氮的一种氢化物HN3,其水溶液酸性与醋酸相似,则NaN3溶液中各离子浓度由大到小的顺序为________________;常温下,将amol/L的Ba(OH) 2 与bmol/L的HN3溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(N3-),则该溶液中c(HN3)=_________ mol/L。
【答案】2NH3(g) +CO2(g)=CO(NH2)2(s)+ H2O (l) △H=-75kJ/mol < 0.02 mol ·L-1·min-1 3.6 B 2NH3 - 6e- = N2 + 6H+ c(Na+)>c(N3﹣)>c(OH-)>c(H+) (0.5b-a)
【解析】
(1)结合盖斯定律计算①+②③得到CO2和NH3合成尿素(副产物是液态水)的热化学方程式;
(2)①先拐先平温度高,升高温度甲烷物质的量增大,说明升温平衡逆向移动;
②温度T1时,0~10min内NO2的平均反应速率v=![]() ,平衡常数K=
,平衡常数K= ![]() ;
;
③提高反应速率同时提高NO2的转化率,增大反应速率同时平衡正向进行,结合化学平衡移动原理和反应特征分析判断;
(3)正极上是二氧化氮得到电子发生还原反应,负极上是氨气失电子发生氧化反应,结合电极反应分析判断;
(4)NaN3溶液中N3水解,溶液呈碱性,结合溶液中电荷守恒分析溶液中离子浓度大小顺序;结合反应2HN3+Ba(OH)2=Ba(N3)2+2H2O的定量关系计算剩余HN3物质的量得到溶液中HN3浓度。
(1)①2NH3(g)+CO2(g)=NH2CO2NH4 (s) △H=-151.5 kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) △H=+120.5 kJ·mol-1
③H2O(l)=H2O(g) △H=+44 kJ·mol-1
结合盖斯定律计算①+②③得到CO2和NH3合成尿素(副产物是液态水)的热化学方程式:2NH3(g) +CO2(g)=CO(NH2)2(s)+ H2O (l) △H=-75kJ/mol,
故答案为:2NH3(g) +CO2(g)=CO(NH2)2(s)+ H2O (l) △H=-75kJ/mol;
(2)CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) △H,
N2(g)+CO2(g)+2H2O(g) △H,
①结合图像分析,先拐先平温度高,即T2>T1,温度越高甲烷物质的量越大,证明升温平衡逆向进行,正反应为为放热反应,△H<0,
故答案为:<;
②温度T1时,0~10min内,甲烷物质的量减小0.4mol0.3mol=0.1mol,反应的二氧化氮物质的量为0.2mol, NO2的平均反应速率v(NO2)= =0.02 mol ·L-1·min-1,
=0.02 mol ·L-1·min-1,
结合三段式计算平衡浓度得到平衡常数,平衡状态下甲烷物质的量0.1mol,

K=![]() =3.6;
=3.6;
③CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g),反应为气体体积增大的放热反应,
N2(g)+CO2(g)+2H2O(g),反应为气体体积增大的放热反应,
A、改用高效催化剂增大反应速率不改变化学平衡,转化率不变,故A不符合题意;
B、增加CH4的浓度,反应速率增大,提高NO2的转化率,故B符合题意;
C、缩小容器的体积,增大压强反应速率增大,平衡逆向进行,反应物转化率减小,故C不符合题意;
D、反应为放热反应,升高温度平衡逆向进行,反应速率增大,转化率减小,故D不符合题意;
故答案为:B;
(3)6NO2+8NH3=7N2+12H2O,正极上是二氧化氮得到电子发生还原反应,电极反应为:2NO2+8e+4H2O=N2+8OH,负极上是氨气失电子发生氧化反应,电极反应为:2NH3 - 6e- = N2 + 6H+;
(4)NaN3溶液中N3水解,溶液呈碱性,故溶液中离子浓度![]() mol/L =(0.5b-a)mol/L。
mol/L =(0.5b-a)mol/L。


科目:高中化学 来源: 题型:
【题目】以辉铜矿为原料生产碱式碳酸铜的工艺流程如图所示:
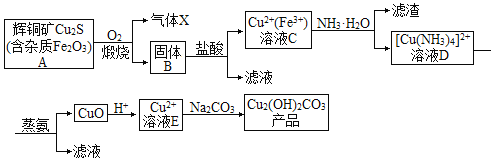
回答下列问题:
(1)若要提高辉铜矿煅烧效率可采取的措施有___(填两种)。
(2)气体X的主要成分是___(填化学式),写出该气体的一种用途___。
(3)蒸氨过程总反应的化学方程式是___。
(4)溶液E与Na2CO3溶液反应制取Cu2(OH)2CO3的离子反应方程式为___。
(5)某实验小组研究溶液E与Na2CO3溶液加料顺序及加料方式对产品的影响,实验结果如下:
实验序号 | 加料顺序及方式 | 沉淀颜色 | 沉淀品质 | 产率/% |
1 | 溶液E一次加入Na2CO3溶液中并迅速搅拌 | 浅蓝色 | 品质较好 | 87.8 |
2 | 溶液E逐滴加入Na2CO3溶液中并不断搅拌 | 暗蓝色 | 品质好 | 71.9 |
3 | Na2CO3溶液一次加入溶液E中并迅速搅拌 | 浅绿色 | 品质好 | 96.7 |
4 | Na2CO3溶液一次加入溶液E中并不断搅拌 | 浅蓝色 | 品质较好 | 102.7 |
由上表可知制取Cu2(OH)2CO3最佳加料顺序及加料方式是___(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质结构的命题中,错误的项数有
①CH3COOH分子中碳原子的杂化类型有sp2和sp3两种
②元素Ge位于周期表第四周期IVA族,核外电子排布式为 [Ar]4s24p2,属于P区
③非极性分子往往具有高度对称性,如BF3、PCl5、H2O2、CO2这样的分子
④冰中存在极性共价键和氢键两种化学键的作用
⑤Cu(OH)2是一种蓝色絮状沉淀,既溶于硝酸、氨水,也能溶于硫酸氢钠溶液中
⑥熔融态的HgCl2不导电,HgCl2稀溶液有弱的导电能力说明固态HgCl2是分子晶体,为非电解质
⑦氨水中大部分NH3与H2O以氢键(用“...”表示)结合成NH3.H2O分子,根据氨水的性质可知NH3.H2O的结构式可记为:
A. 4项 B. 5项 C. 6项 D. 7项
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用0.100 mol·L-1 AgNO3滴定50.0 mL 0.0500 mol·L-1 Cl-溶液的滴定曲线如图所示。下列有关描述错误的是

A. 根据曲线数据计算可知Ksp(AgCl)的数量级为10-10
B. 曲线上各点的溶液满足关系式c(Ag+)·c(Cl-)=Ksp(AgCl)
C. 相同实验条件下,若改为0.0400 mol·L-1 Cl-,反应终点c移到a
D. 相同实验条件下,若改为0.0500 mol·L-1 Br-,反应终点c向b方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫有多种化合物,如H2S、COS(羰基硫)、SO2等,它们对环境均有一定的影响。
(1)H2S经 K2CO3溶液吸收后,生成两种酸式盐。其中任意一种酸式盐的化学式是____。
(2)COS(羰基硫)燃烧时有SO2生成,其原理为:2COS+3O2![]() 2CO2+2SO2。若转移3.612×1024个电子,则参加反应COS(羰基硫)的物质的量是____mol。
2CO2+2SO2。若转移3.612×1024个电子,则参加反应COS(羰基硫)的物质的量是____mol。
(3)电厂排出的烟气中含有CO、SO2等。SO2能与H2S反应生成S和H2O,说明SO2具有____性。CO在催化剂存在时可与SO2反应,转化为一种固体和一种无害气体。该反应的化学方程式是___。
(4)石灰石作为脱硫剂,可有效吸收废气中的SO2,减少酸雨的产生。
①在煤炭中加入石灰石可减少燃烧时SO2的排放量,并生成CaSO4。该反应的化学方程式是____。
②你认为减少酸雨产生的途径可采取的措施是____(填序号)。
a.避免直接用高硫煤作燃料 b.把工厂的烟囱造高
c.燃料脱硫 d.开发新能源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在指定溶液中一定能大量共存的是
A. 无色透明溶液中: H+、Na+、MnO![]() 、SO
、SO![]()
B. 碱性溶液中:Na+、K+、SiO![]() 、NO
、NO![]()
C. 能溶解Al2O3的溶液中:Mg2+、Cu2+、HCO![]() 、Cl-
、Cl-
D. 含有Fe2+的溶液中:H+、Ca2+、NO![]() 、AlO
、AlO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】央视网2019年6月17日报道,针对近年来青蒿素在全球部分地区出现的“抗药性”难题,我国著名药学家、诺贝尔生理学或医学奖获得者屠呦呦及其团队,经过多年攻坚,提出应对“青蒿素抗药性”难题的切实可行治疗方案。从青蒿(粉末)中提取青蒿素的方法以萃取原理为基础,主要有乙醚浸提法和汽油浸提法。青蒿素为白色针状晶体,易溶于乙醇、乙醚、苯和汽油等有机溶剂,不溶于水,熔点为156~157℃,沸点为389.9℃,热稳定性差,汽油浸提法的主要工艺流程如下图所示。
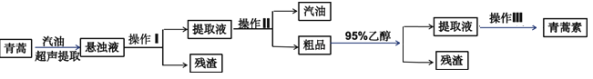
注:汽油的沸点为40~200℃。回答下列问题:
(1)超声提取的原理是在强大的超声波作用下,使青蒿细胞乳化、击碎、扩散,超声波提取的优点是___________、时间短、温度低等。
(2)操作1的名称为________,如图所示为操作Ⅱ的实验装置图(部分夹持装置已略),图中A、B、C、D错误的是_______(填标号)。
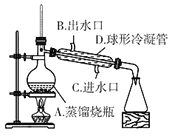
(3)已知青蒿素在95%乙醇中的溶解度随温度的升高而升高,则操作Ⅲ为____________、过滤、洗涤、干燥。
(4)通过控制其他实验条件不变,来研究原料粒度、提取时间和提取温度对青蒿素提取速率的影响,其结果如下图所示,采用的最佳原料粒度、提取时间和提取温度分别为________。
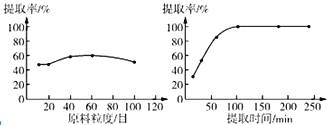
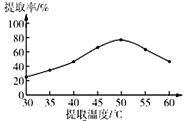
(5)将青蒿素加入滴有酚酞的NaOH溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与_________ (填标号)具有相似的性质。
A 乙醇 B 乙酸甲酯 C 乙醛 D 果糖
(6)已知青蒿素的分子式为C15H22O5(相对分子质量为282),将28.2g青蒿素样品在燃烧管中充分燃烧,将燃烧后的产物依次通过盛有足量P2O5和碱石灰的干燥管,盛有碱石灰干燥管增重的质量为______g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A.7.8 g的Na2S和Na2O2的混合物中含有阴、阳离子总数为0.3 NA
B.常温常压下,22.4 LCO2中含有NA个CO2分子
C.1.0 L 1.0 mol·L-1的NaClO水溶液中含有的氧原子数为NA
D.常温常压下,18 g羟基(-O2H)中所含的中子数为8 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烟气脱硫脱硝是环境治理的热点问题。
(1)氧化还原法脱硝:4NO(g)+4NH3(g)+O2(g)=4N2(g)+6H2O(g)ΔH=-1627.2kJ/mol。检验脱硝效果的重要指标是脱硝效率(脱硝过程中单位时间内NOx浓度变化占烟气初始浓度的百分比)。影响SCR系统脱硝效率的因素有很多,根据如图判断提高脱硝效率的最佳条件是__;氨氮比一定时,随温度的升高脱硝效率增大,其可能的原因是___。
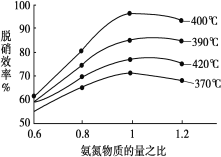
(2)H2Y2-与Fe2+形成的络合物FeY2-可用于吸收烟气中的NO。原理:FeY2-(aq)+NO(g)![]() FeY2-(NO)(aq)ΔH<0
FeY2-(NO)(aq)ΔH<0
①将含NO的烟气以一定的流速通入起始温度为50℃的FeY2-溶液中。NO吸收率随通入烟气的时间变化如图。时间越长,NO吸收率越低的原因是___。
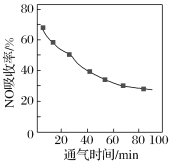
②生成的FeY2-(NO)(aq)可通过加入铁粉还原再生,其原理为FeY2-(NO)(aq)+Fe+H2O→FeY2-(aq)+Fe(OH)2+NH3(未配平)。若吸收液再生消耗14 g铁粉,则所吸收的烟气中含有NO的物质的量为__mol。
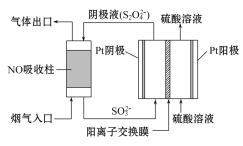
(3)以连二硫酸盐(S2O42-)为媒介,使用间接电化学法也可处理NO,装置如图所示:阴极的电极反应式为___。
(4)KMnO4/CaCO3浆液可协同脱硫,在反应中MnO4-被还原为MnO42-。
①KMnO4脱硫(SO2)的离子方程式为____。
②加入CaCO3的作用是___。
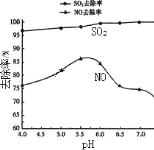
(5)利用NaClO2/H2O2酸性复合吸收剂可同时对NO、SO2进行氧化得到硝酸和硫酸而除去。在温度一定时,溶液pH对脱硫脱硝的影响如图所示:图中SO2的去除率随pH的增大而增大,而NO的去除率在pH>5.5时反而减小,请解释二者去除率不同的可能原因是__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com