
【题目】下列各反应不属于加成反应的是( )
A.![]()
B.![]()
C.
D.![]()
【答案】D
【解析】
加成反应是指有机物分子中的双键或叁键发生断裂,加进(结合)其它原子或原子团的反应;取代反应是指有机物分子里的原子或原子团被其他原子或原子团代替的反应。
A. CH2═CH2与H-OH反应时C=C双键断开,H-OH键断开,-H和-OH分别连在两个不饱和碳键上生成化合物CH3-CH2-OH,发生加成反应,故A正确;
B. CH3CH=CH2和Br2反应时C=C双键断开,Br-Br键断开,两个-Br分别连在两个不饱和碳键上生成化合物CH3CHBrCH2Br,发生加成反应,故B正确;
C. 不饱和键C=O双键断开,H-H键断开,两个-H分别跟不饱和碳原子和氧原子直接结合生成CH3-CH2-OH,发生加成反应,故C正确;
D. CH3-CH3和Cl2反应生成CH2Cl-CH2Cl和HCl属于取代反应,故D错误;
故选D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】H2和I2在一定条件下能发生反应:H2(g)+I2(g)![]() 2HI(g) △H=-a kJ·mol-1已知:下列说法正确的是( )
2HI(g) △H=-a kJ·mol-1已知:下列说法正确的是( )

A.H2、I2和HI分子中的化学键都是非极性共价键
B.相同条件下,1 mol H2(g)和1 mol I2(g)的总能量小于2 mol HI(g)的总能量
C.断开2 mol HI分子中的化学键所需能量约为(c+b+a)kJ
D.向密闭容器中加入2 mol H2(g)和2 mol I2(g),充分反应后放出的热量为2a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬是一种重要的金属元素,具有多种价态,单质铬是硬度最大的金属,熔点为![]() 。回答下列问题:
。回答下列问题:
![]() 工业上以铬铁矿
工业上以铬铁矿![]() 主要成分是
主要成分是![]() 为原料冶炼铬的流程如图所示:
为原料冶炼铬的流程如图所示:
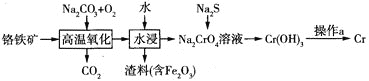
![]() 中铬元素的化合价为_________。
中铬元素的化合价为_________。
![]() 高温氧化时发生反应的化学方程式为________________。
高温氧化时发生反应的化学方程式为________________。
![]() 操作a由两种均发生了化学反应的过程构成,其分别是_________、铝热反应。
操作a由两种均发生了化学反应的过程构成,其分别是_________、铝热反应。
![]() 是两性氢氧化物,请写出其电离方程式_________________。
是两性氢氧化物,请写出其电离方程式_________________。
![]() 铬元素能形成含氧酸及含氧酸盐,若测得浓度为
铬元素能形成含氧酸及含氧酸盐,若测得浓度为![]() 的铬酸
的铬酸![]() 溶液中含铬元素的微粒浓度分别为
溶液中含铬元素的微粒浓度分别为![]() 、
、![]() 、
、![]() ,试推测
,试推测![]() 溶液呈________
溶液呈________![]() 填“酸”“碱”或“中”
填“酸”“碱”或“中”![]() 性,原因是______________。
性,原因是______________。
![]() 水中的铬元素对水质及环境均有严重的损害作用,工业上用下述方法来进行无害化处理并获得有价值的产品。
水中的铬元素对水质及环境均有严重的损害作用,工业上用下述方法来进行无害化处理并获得有价值的产品。
![]() 电解处理含有
电解处理含有![]() 的污水:用铁作电极电解污水,
的污水:用铁作电极电解污水,![]() 被阳极区生成的离子还原成
被阳极区生成的离子还原成![]() ,生成的
,生成的![]() 与阴极区生成的
与阴极区生成的![]() 结合生成
结合生成![]() 沉淀而除去。则阴极上的电极反应式为_______,若要处理
沉淀而除去。则阴极上的电极反应式为_______,若要处理![]() 浓度为
浓度为![]() 的污水,理论上需要消耗_______kg的铁。
的污水,理论上需要消耗_______kg的铁。
![]() 转化为有价值的产品磁性铁铬氧体
转化为有价值的产品磁性铁铬氧体![]() :先向含
:先向含![]() 的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气
的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气![]() 氧化部分
氧化部分![]() 并加入NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。写出
并加入NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。写出![]() 在酸性条件下被
在酸性条件下被![]() 还原为
还原为![]() 的离子方程式__________,若处理含
的离子方程式__________,若处理含![]() 不考虑其他含铬微粒
不考虑其他含铬微粒![]() 的污水时恰好消耗
的污水时恰好消耗![]() ,则当铁铬氧体中
,则当铁铬氧体中![]() 时,铁铬氧体的化学式为_______________。
时,铁铬氧体的化学式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芯片主要由单晶体硅成。下图是硅及其化合物的类价二维图,根据要求完成下列化学方程式或离子方程式。

(1)利用焦炭在电炉中还原二氧化硅的化学方程式为_______________。
(2)利用氢氟酸刻蚀玻璃的化学方程式为_______________。
(3)硅酸钠转化为原硅酸的离子方程式_______________。
(4)二氧化硅与烧碱溶液反应的化学方程式_______________。
(5)石英与纯碱在玻璃熔炉里加强热发生反应的化学方程式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用电解技术,以氯化氢为原料回收氯气的过程如图所示,下列说法不正确的是

A.H+由阳极区向阴极区迁移
B.阳极电极反应:2HCl + 2e- == Cl2 + 2H+
C.阴极电极反应:Fe3+ + e- == Fe2+
D.阴极区发生的反应有:4Fe2+ + O2 + 4H+ == 4Fe3+ + 2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在120 ℃时,以任意质量比混合的某烃的混合物和过量 O2 在一密闭容器中完全反应,测知反应前后的压强没有变化,则该混合烃可能是( )
A.CH4和C2H4B.CH4和C2H6C.C2H4和C2H6D.C2H2和C3H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,![]() 某无色可燃性气体在足量氧气中完全燃烧。将产物通入足量澄清石灰水中,得到白色沉淀的质量为
某无色可燃性气体在足量氧气中完全燃烧。将产物通入足量澄清石灰水中,得到白色沉淀的质量为![]() ;若用足量碱石灰吸收燃烧产物,则碱石灰增重
;若用足量碱石灰吸收燃烧产物,则碱石灰增重![]() 。
。
(1)计算燃烧产物中水的质量_____________。
(2)若原气体是单一气体,通过计算推断它的分子式___________________。
(3)若原气体是两种等物质的量的气体的混合物,其中只有一种是烃,请写出它们的分子式________________(只要求写出一组)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点。如图1为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔的石墨棒。当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流。
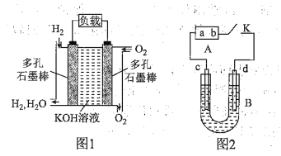
回答下列问题:
![]() 图1中通过负载的电子流动方向为________
图1中通过负载的电子流动方向为________![]() 填“向左”或“向右”
填“向左”或“向右”![]() 。
。
![]() 写出氢氧燃料电池工作时的电极反应式:正极:________,负极:________。
写出氢氧燃料电池工作时的电极反应式:正极:________,负极:________。
以该燃料电池为电源进行实验,如图2所示,B为电解槽,c、d为铁电极,B中装有一定浓度的NaOH溶液,闭合K,c电极周围逐渐析出白色沉淀。
![]() 极是电池的________
极是电池的________![]() 填“正极”或“负极”
填“正极”或“负极”![]() ,c电极的电极反应式为________。
,c电极的电极反应式为________。
![]() 若c、d为石墨电极,B中装有
若c、d为石墨电极,B中装有![]() 和
和![]() 的混合溶液,其中
的混合溶液,其中![]() 的物质的量浓度为
的物质的量浓度为![]() ,
,![]() 的物质的量浓度为
的物质的量浓度为![]() 。闭合K,c电极收集到标准状况下
。闭合K,c电极收集到标准状况下![]() 的一种气体甲。在收集气体甲的过程中电解明显分为两个阶段,请写出相应的电解总化学方程式:第一阶段:________ ;第二阶段:________;d电板理论上收集到的气体体积是________
的一种气体甲。在收集气体甲的过程中电解明显分为两个阶段,请写出相应的电解总化学方程式:第一阶段:________ ;第二阶段:________;d电板理论上收集到的气体体积是________![]() 标准状况下
标准状况下![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾中含有多种污染物,包括氮氧化物![]() 、CO、
、CO、![]() 等。它们可以通过化学反应得到一定的消除或转化。
等。它们可以通过化学反应得到一定的消除或转化。
![]() 氮硫的氧化物的转化:
氮硫的氧化物的转化: ![]()
已知:![]()
![]()
![]() ,则
,则![]() _______
_______![]() 。
。
一定条件下,将![]() 与
与![]() 以一定比例置于恒温恒容的密闭容器中发生上述反应,下列能说明反应达到平衡状态的有_______。
以一定比例置于恒温恒容的密闭容器中发生上述反应,下列能说明反应达到平衡状态的有_______。
![]() 混合气体的密度不变
混合气体的密度不变 ![]() 混合气体的颜色保持不变
混合气体的颜色保持不变
![]() 和NO的体积比保持不变
和NO的体积比保持不变 ![]() 反应速率
反应速率![]()
![]() 碳氧化物的转化:
碳氧化物的转化:
![]() 可用于合成甲醇,反应方程式为:
可用于合成甲醇,反应方程式为:![]() ,在一恒温恒容密闭容器中充入
,在一恒温恒容密闭容器中充入![]() 和
和![]() 进行上述反应。测得CO和
进行上述反应。测得CO和![]() 浓度随时间变化如图1所示。
浓度随时间变化如图1所示。

则![]() 内,氢气的反应速率为____
内,氢气的反应速率为____![]() 第
第![]() 后,保持温度不变,向该密闭容器中再充入
后,保持温度不变,向该密闭容器中再充入![]() 和
和![]() ,则平衡_______
,则平衡_______![]() 填“正向”、“逆向”或“不”
填“正向”、“逆向”或“不”![]() 移动。
移动。
![]() 通过电解CO制备
通过电解CO制备![]() ,电解液为碳酸钠溶液,工作原理如图2所示,写出阴极的电极反应式_____。若以甲醇燃料电池作为电源,则生成标准状况下
,电解液为碳酸钠溶液,工作原理如图2所示,写出阴极的电极反应式_____。若以甲醇燃料电池作为电源,则生成标准状况下![]() 需要消耗
需要消耗![]() 的质量为_______。
的质量为_______。

![]() 硫氧化物的转化:硫的氧化物与一定量氨气、空气反应,可生成硫酸铵。硫酸铵水溶液呈酸性的原因是________________
硫氧化物的转化:硫的氧化物与一定量氨气、空气反应,可生成硫酸铵。硫酸铵水溶液呈酸性的原因是________________![]() 用离子方程式表示
用离子方程式表示![]() 室温时,向
室温时,向![]() 溶液中滴入NaOH溶液至溶液呈中性,则所得溶液中微粒浓度大小关系:
溶液中滴入NaOH溶液至溶液呈中性,则所得溶液中微粒浓度大小关系:![]() ____
____![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]() 。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com