
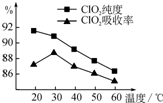
 某研究小组用黄铁矿(FeS2)、氯酸钠和硫酸溶液混合反应制备ClO2气体,再用水吸收该气体可得ClO2溶液.在此过程中需要控制适宜的温度,若温度不当,副反应增加,影响生成
某研究小组用黄铁矿(FeS2)、氯酸钠和硫酸溶液混合反应制备ClO2气体,再用水吸收该气体可得ClO2溶液.在此过程中需要控制适宜的温度,若温度不当,副反应增加,影响生成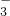 氧化成SO
氧化成SO ,请写出制备二氧化氯(ClO2)的离子方程式:______.
,请写出制备二氧化氯(ClO2)的离子方程式:______.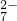 +6Fe2+═2Cr3++6Fe3++7H2O
+6Fe2+═2Cr3++6Fe3++7H2O ×100%=56.25%
×100%=56.25%

科目:高中化学 来源: 题型:
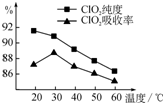 某研究小组用黄铁矿(FeS2)、氯酸钠和硫酸溶液混合反应制备ClO2气体,再用水吸收该气体可得ClO2溶液.在此过程中需要控制适宜的温度,若温度不当,副反应增加,影响生成
某研究小组用黄铁矿(FeS2)、氯酸钠和硫酸溶液混合反应制备ClO2气体,再用水吸收该气体可得ClO2溶液.在此过程中需要控制适宜的温度,若温度不当,副反应增加,影响生成- 3 |
2- 4 |
2- 7 |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年云南省玉溪一中高二下学期期末考试化学试卷(带解析) 题型:实验题
(14分)某研究小组模拟工业上以黄铁矿为原料制备硫酸的第一步反应:
4FeS2+11O2 2Fe2O3+8SO2,进行以下实验,并测定该样品中FeS2样品的纯度(假设其它杂质不参与反应)。
2Fe2O3+8SO2,进行以下实验,并测定该样品中FeS2样品的纯度(假设其它杂质不参与反应)。
实验步骤:称取研细的样品4.000g放入上图b装置中,然后在空气中进行煅烧。为测定未反应高锰酸钾的量(假设其溶液体积保持不变),实验完成后取出d中溶液10mL置于锥形瓶里,用0.1000mol/L草酸(H2C2O4)标准溶液进行滴定。
(已知:5SO2 + 2KMnO4 + 2H2O ="=" K2SO4 + 2MnSO4 + 2H2SO4 )
请回答下列问题:
(1)称量样品质量能否用托盘天平 (填“能”或“不能”);
(2)装置a的作用是 ;
(3)上述反应结束后,仍需通一段时间的空气,其目的是 ;
(4)滴定时,发生反应的离子方程式为 ,已知滴定管初读数为0.10mL,末读数如上图所示,消耗草酸溶液的体积为 mL;
(5)该样品中FeS2的纯度为 ;
(6)若用下图装置替代上述实验装置d,同样可以达到实验目的的是 。(填编号)
查看答案和解析>>
科目:高中化学 来源:2013届云南省高二下学期期末考试化学试卷(解析版) 题型:实验题
(14分)某研究小组模拟工业上以黄铁矿为原料制备硫酸的第一步反应:
4FeS2+11O2 2Fe2O3+8SO2,进行以下实验,并测定该样品中FeS2样品的纯度(假设其它杂质不参与反应)。
2Fe2O3+8SO2,进行以下实验,并测定该样品中FeS2样品的纯度(假设其它杂质不参与反应)。

实验步骤:称取研细的样品4.000g放入上图b装置中,然后在空气中进行煅烧。为测定未反应高锰酸钾的量(假设其溶液体积保持不变),实验完成后取出d中溶液10mL置于锥形瓶里,用0.1000mol/L草酸(H2C2O4)标准溶液进行滴定。

(已知:5SO2 + 2KMnO4 + 2H2O == K2SO4 + 2MnSO4 + 2H2SO4 )
请回答下列问题:
(1)称量样品质量能否用托盘天平 (填“能”或“不能”);
(2)装置a的作用是 ;
(3)上述反应结束后,仍需通一段时间的空气,其目的是 ;
(4)滴定时,发生反应的离子方程式为 ,已知滴定管初读数为0.10mL,末读数如上图所示,消耗草酸溶液的体积为 mL;
(5)该样品中FeS2的纯度为 ;
(6)若用下图装置替代上述实验装置d,同样可以达到实验目的的是 。(填编号)

查看答案和解析>>
科目:高中化学 来源:模拟题 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com