
【题目】氢氧燃料电池是一种化学电源,如图所示,以石墨为电极,两极分别通入氢气和氧气,KOH溶液为电解质溶液,下列说法不正确的是

A. a电极是该电池的正极
B. 电池工作时,电子从a电极流出经导线流向b电极
C. 工作一段时间后,电解质溶液碱性减弱
D. b极的电极反应式为:O2+2H2O+4e-=4OH-
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】在一定条件下,充分燃烧一定量的丁烷放出热量为Q kJ(Q>0),经测定完全吸收生成的CO2需消耗 5 mol·L-1的KOH溶液100 mL,恰好生成正盐,则此条件下反应C4H10(g)+O2(g)===4CO2(g)+5H2O(g)的ΔH为
A.+8Q kJ·mol-1 B. -16Q kJ·mol-1
C.-8Q kJ·mol-1 D. +16Q kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)常温下某溶液中由水电离出的离子浓度符合c(H+)·c(OH﹣)=1×10﹣20的溶液,其pH为 ,此时水的电离受到 .
(2)在某温度下,H2O的离子积常数为1×10﹣13 mol2·L﹣2,则该温度下:100mL 0.1mol·L﹣1H2SO4溶液与100mL 0.4mol·L﹣1的KOH溶液混合后,pH= .
(3)已知一溶液有4种离子:X+、Y﹣、H+、OH﹣,下列分析结果肯定错误的是 .
A.c(Y﹣)>c(X+)>c(H+)>c(OH﹣)
B.c(X+)>c(Y﹣)>c(OH﹣)>c(H+)
C.c(H+)>c(Y﹣)>c(X+)>c(OH﹣)
D.c(OH﹣)>c(X+)>c(H+)>c(Y﹣)
(4)在25℃下,将a mol·L﹣1的氨水与0.01mol·L﹣1的盐酸等体积混合,反应时溶液中c(NH4+)=c(Cl﹣).则溶液显 (填“酸”“碱”或“中”)性;用含a的代数式表示NH3·H2O的电离常数Kb= .
(5)水溶液中的行为是中学化学的重要内容.已知下列物质的电离常数值:HClO:Ka=3×10﹣8;H2CO3:Ka1=4.3×10﹣7;Ka2=5.6×10﹣11;84消毒液中通入少量的CO2,该反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种元素的原子序数大小顺序为C>A>B>D>E,A、C同周期,B、C同主族;A与B形成离子化合物,A2B中所有离子的电子数相同且电子总数为30;D和E可形成4核10电子分子。回答:
(1)写出五种元素的名称:A____B____C____D___E_____
(2)用电子式表示离子化合物A2B的形成过程:___________________________
(3)写出D元素形成的单质的结构式____________
(4)A、B两元素组成的化合物A2B2中存在的化学键是____________,写出A2B2与CO2反应的化学反应方程式________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组探究元素周期律,甲根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成N、C、Si的非金属性强弱比较的研究;乙根据置换反应的规律,利用下图装置完成O元素的非金属性比S强的研究。回答:
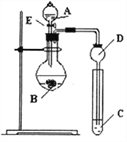
(1)图中A装置名称是______________。
(2)从以下所给物质中选出甲同学设计的实验所用到物质:
①稀HNO3溶液 ②稀盐酸 ③碳酸钙 ④Na2SiO3 溶液 ⑤SiO2
试剂A与C分别为_________(填序号);试管中发生反应的离子方程式为_______________.有同学认为此实验不能说明N、C、S的非金属性强弱,你认为原因是_________________
(3)乙同学设计的实验所用到试剂A为________;如果C试剂为硫化氢的水溶液,则试管中可以观察到的现象为_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往1.0 mol·L-1KI溶液中加入固体I2,发生反应:I2(aq)+I- (aq)![]() I3-(aq) △H;I-的物质的量浓度c(I-)随温度T的变化曲线如图所示。已知反应第一次达到平衡时用时10s,则下列说法正确的是
I3-(aq) △H;I-的物质的量浓度c(I-)随温度T的变化曲线如图所示。已知反应第一次达到平衡时用时10s,则下列说法正确的是

A.该反应的△H>0
B.a、c两点对应的I-反应速率相等
C.b点时0~10s I-的平均反应速率为0.04mol·L-1·s-1
D.d点时该反应在对应温度下处于平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于乙烯说法正确的是
A. 乙烯使酸性高锰酸钾溶液及溴的四氯化碳溶液褪色原理相同
B. 工业利用乙烯水化法制乙醇,是发生了取代反应
C. 水果运输中为延长果实的成熟期,常在车厢里放置浸泡过高锰酸钾溶液的硅藻土
D. 乙烯在空气中燃烧,发生火焰明亮并带有浓烟的火焰
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com