
【题目】某兴趣小组同学利用氧化还原反应:2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如下原电池,盐桥中装有饱和溶液。下列说法正确的是( )
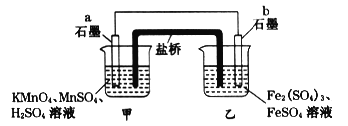
A. a电极上发生的反应为:MnO4-+8H++5e-═Mn2++4H2O
B. 外电路电子的流向是从a到b
C. 电池工作时,盐桥中的SO42-移向甲烧杯
D. b电极上发生还原反应
【答案】A
【解析】试题分析:A、总电极反应式:2MnO4-+10Fe2++16H+=2Mn2++10Fe3++8H2O,a极是正极得电子,电极反应式=总电极反应式-b极反应式,得出:2MnO4-+16H++10e-=2Mn2++8H2O,化简得:MnO4-+8H++5e-=Mn2++4H2O,A正确;B、根据A的分析,外电路电子流向是从b流向a,B错误;C、根据原电池的工作原理:阴离子向负极移动,阳离子向正极移动,SO42-向b极移动,C错误;D、根据原电池的工作原理:负极失电子,发生氧化反应,正极得电子发生还原反应,b极上电极反应式:Fe2+-e-=Fe3+,D错误,答案选A。


科目:高中化学 来源: 题型:
【题目】电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开。在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。已知:3I2+6OH-=IO3-+5I-+3H2O,下列说法不正确的是( )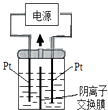
A.右侧发生的电极反应式:2H2O+2e-=H2↑+2OH-
B.电解结束后,右侧溶液中含有IO3-
C.电解槽内发生反应的总化学方程式:KI+3H2O=KIO3+3H2↑
D.如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学方程式不变。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.放热反应在任意条件下都能自发进行
B.已知热化学方程式2A(g)+B(g) ![]() 2C (g)△H=-QkJ/mol (Q >0)将2molA(g)和1molB(g)置于一密闭容器中充分反应后放出QkJ的热量
2C (g)△H=-QkJ/mol (Q >0)将2molA(g)和1molB(g)置于一密闭容器中充分反应后放出QkJ的热量
C.1mol/L的盐酸与1mol/L的氨水、11mol/L的NaOH溶液等体积混合,充分反应,后者比前者放出的热量多
D.BaCl2溶液中加过量H2SO4 , 溶液中一定不存在Ba2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三种短周期元素在周期表中的位置关系如图所示,下列说法正确的是( )
X | ||
Y | ||
Z |
A.无法确定X,Y,Z是何种元素
B.Z元素没有负价
C.均是非金属元素
D.均能形成双原子分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某密闭容器中加入0.30![]()
![]() 、0.10
、0.10![]()
![]() 和一定量的
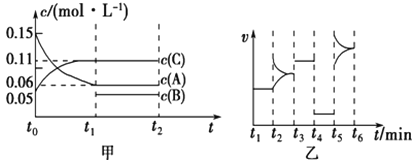
和一定量的![]() 三种气体,一定条件下发生反应,各物质浓度随时间变化如甲图所示[
三种气体,一定条件下发生反应,各物质浓度随时间变化如甲图所示[![]() 阶段的
阶段的![]() 变化未画出]。乙图为
变化未画出]。乙图为![]() 时刻后改变条件平衡体系中正、逆反应速率随时间变化的情况,且四个阶段都各改变一种反应条件(浓度、温度、压强、催化剂)且互不相同,
时刻后改变条件平衡体系中正、逆反应速率随时间变化的情况,且四个阶段都各改变一种反应条件(浓度、温度、压强、催化剂)且互不相同, ![]() 阶段为使用催化剂。下列说法不正确的是
阶段为使用催化剂。下列说法不正确的是
A. 若![]() ,则用
,则用![]() 的浓度变化表示的
的浓度变化表示的![]() 阶段的平均反应速率为0.004
阶段的平均反应速率为0.004![]()
B. ![]() 阶段改变的条件一定为减小压强
阶段改变的条件一定为减小压强
C. 若该容器的容积为2![]() ,则
,则![]() 的起始的物质的量为0.02
的起始的物质的量为0.02![]()
D. 若![]() 阶段,容器内
阶段,容器内![]() 的物质的量减少了0.03
的物质的量减少了0.03![]() ,而此过程中容器与外界的热交换总量为
,而此过程中容器与外界的热交换总量为![]() ,则该反应的热化学方程式为:
,则该反应的热化学方程式为: ![]()
![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上采用的一种污水处理方法如下:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3 . Fe(OH)3具有吸附性,可吸附污物而沉积下来,有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用该原理处理污水,设计装置如图所示.下列说法正确的是( )

A. 为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时,循环的物质A为CO2
B. 甲装置中阴极的反应为Fe﹣2e﹣═Fe2+
C. 为了增加污水的导电能力,应向污水中如入适量的NaOH溶液
D. 当乙装置中有1.6 g CH4参加反应,则C电极理论上生成气体在标准状况下为4.48 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在人类社会的发展进程中,金属起着重要的作用.下列说法正确的是( )
A.地球上绝大多数金属元素是以游离态存在于自然界中的
B.在化学反应中,金属容易失去电子,是还原剂
C.多数合金的熔点高于组成它的成分的金属的熔点
D.硅单质是良好的半导体,所以它是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓硫酸中H3AsO3与SnCl2反应的离子方程式为:3SnCl2+12Cl-+2H3AsO3+6H+=2As+3SnCl62-+6M
①氧化剂是H3AsO3;②还原性:Cl->As;
③每生成7.5gAs,还原剂失去的电子为0.3 mol;
④M为OH-;⑤ SnCl62-是氧化产物。
关于该反应的说法中正确的组合是( )
A.①③⑤
B.①③
C.①②④⑤
D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果酸的结构简式为: ![]() ,下列说法正确的是( )
,下列说法正确的是( )
A.苹果酸能被氧化成三元羧酸
B.1 mol苹果酸可与3 mol NaOH发生中和反应
C.含1 mol苹果酸的稀溶液与足量金属Na反应生成1.5molH2
D.2分子苹果酸相互反应,可形成结构为六元环、七元环或八元环的酯类物质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com