
����Ŀ����ҵ�ϲ��õ�һ����ˮ�����������£�������ˮ��pH��5.0��6.0֮�䣬ͨ���������Fe��OH��3 �� Fe��OH��3���������ԣ�����������������������о���ˮ�����ã��������������ݰ���ˮ�����������ˮ���γɸ����㣬��ȥ����Ʋ���������㣬�����˸�ѡ���������ã�ij����С���ø�ԭ��������ˮ�����װ����ͼ��ʾ������˵����ȷ���ǣ�������

A. Ϊ��ʹ��ȼ�ϵ�س�ʱ���ȶ����У���صĵ�������Ӧ�����ȶ�����ع���ʱ��ѭ��������AΪCO2
B. ��װ���������ķ�ӦΪFe��2e���TFe2+
C. Ϊ��������ˮ�ĵ���������Ӧ����ˮ������������NaOH��Һ
D. ����װ������1.6 g CH4�μӷ�Ӧ����C�缫���������������ڱ�״����Ϊ4.48 L
���𰸡�A
����������װ��Ϊ���أ���װ��Ϊԭ���װ�ã�ԭ��ع���ʱ��ͨ������һ��Ϊ����������������Ӧ�������缫��Ӧ��CH4+4CO32--8e-=5CO2+2H2O��ͨ��������һ��Ϊ������������ԭ��Ӧ��������ӦΪO2+2CO2+4e-=2CO32-��������FeΪ����������Fe-2e-=Fe2+�������ĵ缫��ӦΪ��2H++2e-=H2�������������Ӿ��л�ԭ�ԣ��ܱ����������������ۣ�4Fe2++10H2O+O2=4Fe(OH)3��+8H+���Դ˽�������
A�������������̼����Ϊ����ʣ������缫��Ӧ��CH4+4CO32--8e-=5CO2+2H2O��������ӦΪO2+2CO2+4e-=2CO32-������ѭ�����õ�����ֻ�ж�����̼����A��ȷ��B��������FeΪ����������Fe-2e-=Fe2+����B����C��������ˮ��pH��5.0��6.0֮�䣬ͨ���������Fe(OH)3����ʱ�������ʹ����������ǿ�ĵ���ʱ����ǿ�����ˮ�ġ������Ի������Ե��Σ������������ƻᵼ����Һ�ʼ��ԣ���C����D�����ݵ�صĸ����缫��Ӧ��CH4+4CO32--8e-=5CO2+2H2O������װ������1.6 gCH4�μӷ�Ӧ����0.1mol����μӷ�Ӧʱ����0.8mol����ת�ƣ������ĵ缫��ӦΪ��2H++2e-=H2��������������44.8L(��״��)��2mol����������������ת�Ƶ��ӵ����ʵ���Ϊ4mol����C�缫���������������ڱ�״����Ϊ8.96L����D����ѡA��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵķ���������ǣ� ��
A.�����CO2 NO SO2 H2O
B.�NaOH KOH Ba(OH)2 Na2CO3
C.���NH4Cl NH4NO3 (NH4)2SO4 NH3H2O
D.���������Na2O CaO Mn2O7 MgO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£����������ܱ������зֱ�������������Ӧ����H2(g)+I2(g) ![]() 2HI(g) ��C(s)+H2O(g)
2HI(g) ��C(s)+H2O(g) ![]() CO(g)+H2(g)������״̬�ܱ�������Ӧ���ﵽƽ��״̬����( )
CO(g)+H2(g)������״̬�ܱ�������Ӧ���ﵽƽ��״̬����( )
a�������ʵ�Ũ�Ȳ���
b������������ѹǿ����
c�������������ܶȲ���
d��������������ɫ����
e������ֵ����ʵ���������������������
A.abc
B.ade
C.ac
D.ae
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��﮿��������������Ϊ�綯������ʵ�ô����豸������ԭ��ʾ��ͼ���£�����������ȷ����
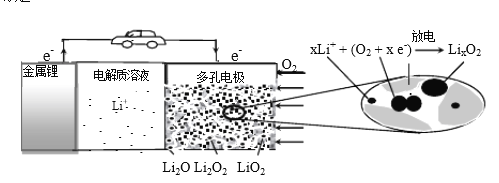
A. �õ�ع���ʱLi+���ƶ�
B. Li2SO4��Һ�����õ�ص������Һ
C. ��س��ʱ��Խ���������Li2O ����Խ��
D. ��ع���ʱ�������ɷ���: 2Li+ +O2+ 2e-=Li2O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС��ͬѧ����������ԭ��Ӧ��2KMnO4+10FeSO4+8H2SO4��2MnSO4��5Fe2(SO4)3��K2SO4��8H2O�������ԭ��أ�������װ�б�����Һ������˵����ȷ���ǣ� ��
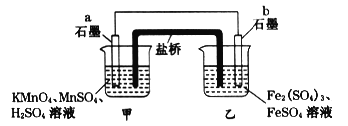
A. a�缫�Ϸ����ķ�ӦΪ��MnO4-+8H++5e-�TMn2++4H2O
B. ���·���ӵ������Ǵ�a��b
C. ��ع���ʱ�������е�SO42-������ձ�
D. b�缫�Ϸ�����ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼװ�ã�A��B�е缫Ϊ��Ķ��Ե缫��C��DΪ����ʪ��Na2SO4��ֽ���ϵIJ��У���Դ��a��b��������A��B�г���KOH��Һ������KOH��Һ��ˮ���У��ж�K1 �� �ϱ�K2��K3ֱͨ���磬�ش��������⣺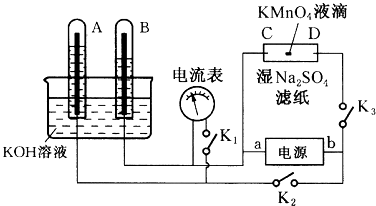
��1���жϵ�Դ��������aΪ����
��2����ʪ��Na2SO4��Һ��ֽ�����ĵ�KMnO4Һ�Σ���һ��ʱ�䣬����Ϊ��
��3�������һ��ʱ���A��B�о��������Χ�缫����ʱ�ж�K2��K3 �� �ϱ�K1 �� ���������ָ��(���ǻ��)ƫת����ƫת�����ʱA���缫��ӦʽΪ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������в����У�һ������²�����Ӵ�����(����)
A.����ʱ����������������ֽ
B.����Ͳ��ʳ����Һ������4.3 mL��Һ
C.����ʱ���ձ��ڱ���©���¶�
D.�ý�ͷ�ι����Թ��ڵμ�Һ��ʱ����ͷ�ιܼ�����Թ��ڱ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴ӦmA(g)��nB(g) ![]() pC(g)�ﵽƽ��������¶ȣ�B��ת���ʱ����Сѹǿ��C�����������С��
pC(g)�ﵽƽ��������¶ȣ�B��ת���ʱ����Сѹǿ��C�����������С��
(1)����>��������������<����գ��÷�Ӧ����H______0��m��n______p��
(2)��������������С���������������(������������)�������¼���B����A��ת����________�������¶ȣ���ƽ��ʱB��C��Ũ��֮��c(B)/c(C)��________�����������ƽ��ʱ��������������ʵ���________��
(3)��A��C��Ϊ��ɫ���壬BΪ��ɫ���壬����������������dz��������������գ������¼���C��ƽ���������ɫ________������ѹ����������ƽ��������ɫ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���и���Ԫ����A,B��Ԫ�ص�ԭ�����������п��γ�AB2�����ӻ�������ǣ� ��
��6��8 ��12��17 ��20��9 ��11��17��
A.�٢�
B.�٢�
C.�ڢ�
D.�ۢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com