
【题目】以反应5H2C2O4+2MnO4-+6H+===10CO2↑+2Mn2++8H2O为例探究“外界条件对化学反应速率的影响”。实验时,分别量取H2C2O4溶液和酸性KMnO4溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢。
编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL | ||
① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
下列说法不正确的是
A. 实验①、②、③所加的H2C2O4溶液均要过量
B. 实验①测得KMnO4溶液的褪色时间为40 s,则这段时间内平均反应速率υ(KMnO4)=2.5×10-4mol·L-1·s-1
C. 若生成a L CO2(标准状况),该反应转移的电子数为aNA/22.4
D. 实验①和②起初反应均很慢,过了一会儿速率突然增大,可能是生成的Mn2+对反应起催化作用
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
【题目】把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的浊液中逐滴加入1molL﹣1 HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如图所示,试回答:
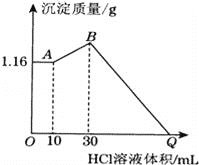
(1)写出混合物溶于水时发生反应的离子方程式________________________________________________。
(2)写出AB段反应的离子方程式__________________。B点的沉淀物的化学式为______________。
(3)求原混合物中AlCl3的物质的量____________,NaOH的质量________________。
(4)求Q点加入的HCl溶液体积.______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】植物油和水、酒精和水、碘的饱和水溶液,这三组混合物的分离方法分别是( )
A. 过滤、蒸馏、分液 B. 分液、蒸馏、萃取
C. 萃取、蒸馏、过滤 D. 萃取、过滤、蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关,下列说法正确的是( )
A.明矾净水时发生了化学及物理变化,能起到杀菌、消毒的作用
B.淀粉溶液、豆浆、雾、碳素墨水均可发生丁达尔现象
C.合金、光导纤维、碳纤维、玻璃钢都属于复合材料
D.光化学烟雾、臭氧层空洞、温室效应、酸雨(硝酸型)的形成都与氮氧化物有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气、铝、铁都是重要的还原剂,已知下列反应的热化学方程式,下列关于反应的焓变判断正确的是
2H2(g)+O2(g)===2H2O(g) △H1
3H2(g)+Fe2O3(s)===2Fe (s)+ 3H2O(g) △H2
2Fe(s)+ 3/2O2(g)===Fe2O3(s) △H3
2Al(s)+3/2O2(g)===Al2O3(s) △H4
2Al(s)+ Fe2O3(s)===Al2O3(s)+2Fe(s) △H5
A. △H1<0;△H3>0 B. △H5<0;△H4<△H3
C. △H1=△H2+△H3 D. △H3=△H4+△H5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学式为AB的离子晶体,已知5r(A2+)=4r(B2-)(各类离子晶体与![]() 关系如下图所示),经测定其密度为
关系如下图所示),经测定其密度为![]() g·cm-3,其摩尔质量为Mg·mol-1,则下列有关该晶体的说法正确的是( )
g·cm-3,其摩尔质量为Mg·mol-1,则下列有关该晶体的说法正确的是( )
r+/r- | 配位数 | 实例 |
0.225~0.414 | 4 | ZnS |
0.414~0.732 | 6 | NaCl |
0.732~1.0 | 8 | CsCl |
>1.0 | 12 | CsF |
A.该晶体结构与ZnS晶体相似
B.该晶体每个晶胞中有2个A2+和B2-
C.该晶体晶胞的边长为 cm
cm
D.A2+离子紧邻的B2-构成的空间结构为立方体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是人类社会不断发展的核心驱动力。下列说法正确的是
A.D、T核聚变发电过程中不产生新元素
B.光催化CO2和H2O合成甲醇为放热反应
C.可燃冰是天然气水合物,属于清洁能源
D.流水、地热能发电的能量转化形式相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
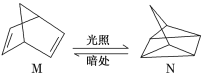
ΔH=+88.6 kJ/mol则M、N相比,较稳定的是________。
(2)已知CH3OH(l)的燃烧热ΔH=-238.6 kJ/mol,CH3OH(l)+![]() O2(g)===CO2(g)+2H2(g) ΔH=-a kJ/mol,则a________238.6(填“>”、“<”或“=”)。
O2(g)===CO2(g)+2H2(g) ΔH=-a kJ/mol,则a________238.6(填“>”、“<”或“=”)。
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:____________________。
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)===2Al2O3(s)+3TiC(s) ΔH=-1 176 kJ/mol,则反应过程中,每转移1 mol电子放出的热量为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com