
【题目】![]() 浓硝酸和
浓硝酸和![]() 铜反应,铜完全溶解,生成的气体颜色由深变浅
铜反应,铜完全溶解,生成的气体颜色由深变浅![]() 生成
生成![]() 、
、![]() ,共收集到
,共收集到![]() 气体
气体![]() 标准状况
标准状况![]() ,剩余酸用NaOH中和,共耗去
,剩余酸用NaOH中和,共耗去![]() 氢氧化钠
氢氧化钠![]() 。则浓
。则浓![]() 物质的量浓度为
物质的量浓度为![]()
![]()
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
【答案】A
【解析】
![]() 与一定量浓硝酸反应,Cu完全反应,反应生成气体的颜色逐渐变浅,得到的气体为NO和
与一定量浓硝酸反应,Cu完全反应,反应生成气体的颜色逐渐变浅,得到的气体为NO和![]() ,反应中硝酸起氧化剂与酸性作用,起酸性作用的硝酸生成
,反应中硝酸起氧化剂与酸性作用,起酸性作用的硝酸生成![]() ,起氧化剂作用的硝酸得到NO和
,起氧化剂作用的硝酸得到NO和![]() ,根据元素守恒进行计算。
,根据元素守恒进行计算。
![]() 与一定量浓硝酸反应,Cu完全反应,反应生成气体的颜色逐渐变浅,得到的气体为NO和
与一定量浓硝酸反应,Cu完全反应,反应生成气体的颜色逐渐变浅,得到的气体为NO和![]() ,反应中硝酸起氧化剂与酸性作用,起酸性作用的硝酸生成
,反应中硝酸起氧化剂与酸性作用,起酸性作用的硝酸生成![]() ,起氧化剂作用的硝酸得到NO和
,起氧化剂作用的硝酸得到NO和![]() ,
,
根据N原子守恒,反应中作氧化剂的硝酸的物质的量![]() ,
,
反应中起酸作用的硝酸的物质的量![]() ,
,
剩余硝酸消耗NaOH的物质的量为:![]() ,则反应后剩余硝酸的物质的量为
,则反应后剩余硝酸的物质的量为![]() ,
,
所以原浓硝酸中含有硝酸的物质的量为:![]() ,
,
则浓![]() 物质的量浓度为:
物质的量浓度为:![]() ,
,
故答案选A。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】碳酸镁晶须是一种新型吸波隐形材料中的增强剂。某工厂以MgCl2(含少量杂质FeCl2、FeCl3)为原料制备碳酸镁晶须(MgCO3·H2O)的工艺流程如下:

已知:Fe3+、Fe2+、Mg2+生成氢氧化物沉淀时的pH
注:Fe(OH)2沉淀呈絮状,不易从溶液中除去。
物质 | 开始沉淀 | 沉淀完全 |
Fe(OH)3 | 2.7 | 3.7 |
Fe(OH)2 | 7.6 | 9.6 |
Mg(OH)2 | 9.9 | 11.0 |
(1)写出“氧化”过程中发生的离子反应方程式_______________。
(2)pH调节的范围___________,滤渣的主要成分___________(填化学式)。
(3)操作X包括过滤、洗涤、烘干,证明碳酸镁晶须已经洗涤干净的方法______________。
(4)水浸后溶液中Fe2+、Fe3+含量的测定
①取水浸后溶液100.00 mL,测得Cl-的浓度为0.455 mol·L-1,向其中缓缓通入氯气使Fe2+恰好完全转化为Fe3+,测得此时溶液中Cl-的浓度为0.460 mol·L-1(溶液体积变化忽略不计)。
②另取水浸后溶液100.00 mL,向其中加入过量的1 mol·L-1NaOH溶液,充分反应后过滤、洗涤、灼烧,冷却后,称得固体粉末的质量为0.96 g。试通过计算确定水浸后溶液中Fe2+、Fe3+的物质的量浓度(写出计算过程)。 _______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列能用勒夏特列原理解释的是( )
A.H2、I2、HI平衡混合气加压后颜色变深
B.工业上由氢气和氮气合成氨是在较高温度下进行的
C.Fe(SCN)3溶液中加入固体KSCN后颜色变深
D.SO2催化氧化成SO3的反应,往往需要使用催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温下气体反应达到化学平衡,平衡常数K=c(A)·c2(B)/[c2(E)·c(F)],恒容时,若温度适当降低,F的浓度增加,下列说法正确的是( )
A. 增大c(A)、c(B),K增大
B. 降低温度,正反应速率增大
C. 该反应的焓变为负值
D. 该反应的化学方程式为2E(g)+F(g)![]() A(g)+2B(g)
A(g)+2B(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量的铝粉和铁粉的混合物与一定量很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中逐滴加入![]() 溶液,所加NaOH溶液的体积
溶液,所加NaOH溶液的体积![]() 与产生沉淀的物质的量
与产生沉淀的物质的量![]() 关系如下图所示,下列说法不正确的是
关系如下图所示,下列说法不正确的是 ![]()
![]()
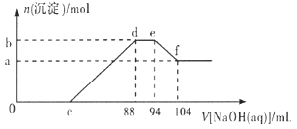
A.稀硝酸与铝粉、铁粉反应,其还原产物为硝酸铵
B.c点对应溶液的体积为![]()
C.b点与a点的差值为![]()
D.样品中铝粉和铁粉的物质的量之比为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有NaNO3和HCl的混合溶液400mL,向混合溶液中逐渐加入过量的Fe粉,如图所示。(反应中HNO3只被还原成NO)下列说法正确的是

A. 硝酸钠的物质的量浓度为2.5mol/L
B. 标况下,反应过程共产生22.4L的气体
C. 整个反应过程中每步转移的电子之和为4mol
D. 将反应后的混合物过滤,滤液蒸发结晶所得固体为 NaCl和FeCl2的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】300 ℃时,将2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g)![]() 2C(g)+2D(g) ΔH,2 min末达到平衡,生成0.8 mol D。
2C(g)+2D(g) ΔH,2 min末达到平衡,生成0.8 mol D。
(1)300 ℃时,该反应的平衡常数表达式为:K=_______。已知K300 ℃<K350 ℃,则ΔH______0(填“>”或“<”)。
(2)在2 min末时,B的平衡浓度为_______,D的平均反应速率为_______。
(3)若温度不变,缩小容器容积,则A的转化率______(填“增大” “减小”或“不变”),原因是_______。
(4)如果在相同的条件下,上述反应从逆反应方向进行,开始时加入C、D各4/3 mol。若使平衡时各物质的物质的量浓度与原平衡相同,则还应该加入B_______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关.
(1)下列生活用品中,其主要材料属于天然纤维的是_________(填字母序号);
A.塑料保鲜薄 B.橡胶手套 C.棉布围裙
(2)我们常用的洗涤剂清洗餐具上的油污,这是因为洗涤剂具有_________的功能;
(3)食用水果、蔬菜主要补充人体所需的_________;
(4)国家禁止在面粉中添加增白剂过氧化钙CaO2,过氧化钙中氧元素的化合价为_______;
(5)农业上降低土壤酸性的是_________(填化学式);
(6)生活中要用到大量的钢铁,写出赤铁矿(主要成分Fe2O3)冶炼成铁的化学方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年是“国际化学元素周期表年”。1869年门捷列夫把当时已知的元素根据物理、化学性质进行排列,准确预留了甲、乙两种未知元素的位置,并预测了二者的相对原子质量,部分原始记录如下。下列说法错误的是
B=11 | Al=27.4 | ?=68(甲) |
C=12 | Si=28 | ?=70(乙) |
N=14 | P=31 | As=75 |
O=16 | S=32 | Se=79.4 |
F=19 | Cl=35.5 | Br=80 |
A.元素甲位于现行元素周期表第四周期第ⅢA族
B.原子半径比较:甲![]() 乙
乙![]()
C.元素乙的简单气态氢化物的稳定性强于![]()
D.推测乙可以用作半导体材料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com