
【题目】A、B、C、D、E是原子序数依次增大的五种短周期元素.A原子的电子层数与它的核外电子总数相同,A与C、B与D分别为同主族,B和C的最外层电子数之和与E的最外层电子数相同,A与E形成的化合物化学式为AE,其分子中含18个电子,请回答下列问题:
(1)E元素单质的化学式为_____、D元素的简单离子的结构示意图为______.
(2)由A、B、C三种元素形成的化合物的电子式为______,这种化合物形成的晶体中所含的化学键类型有______.
(3)A、B、D三种元素形成的一种化合物和A、B形成的一种化合物能发生氧化还原反应,反应的化学方程式为________________________________
(4)把单质E通入碳酸氢钠溶液中发生反应,写出总反应的离子方程式________________________________
【答案】 Cl2 
![]() 离子键 、共价建 H2SO3+H2O2=H2SO4+H2O HCO3-+Cl2=Cl-+HClO+CO2
离子键 、共价建 H2SO3+H2O2=H2SO4+H2O HCO3-+Cl2=Cl-+HClO+CO2
【解析】A、B、C、D、E是原子序数依次增大的五种短周期元素。A原子的电子层数与它的核外电子总数相同,则A为H元素;A与E形成的化合物化学式为AE,其分子中含18个电子,则E原子含有17个电子,故E为氯元素;A与C同主族,B和C的最外层电子数之和与E的最外层电子数相同,则B的最外层电子数为7-1=6,B与D分别为同主族,原子序数B小于D,则B为O元素,D为S元素;C原子序数大于氧元素,C与氢元素为同主族,故C为Na元素,则
(1)氯元素单质的化学式为Cl2,硫元素的简单离子的结构示意图为 ;(2)由A、B、C三种元素形成的化合物为NaOH,氢氧化钠是离子化合物,由钠离子与氢氧根离子构成,电子式为
;(2)由A、B、C三种元素形成的化合物为NaOH,氢氧化钠是离子化合物,由钠离子与氢氧根离子构成,电子式为![]() ;晶体中钠离子与氢氧根离子之间形成离子键,氢氧根离子中氢原子与氧原子之间形成共价键;(3)A、B、D三种元素形成的一种化合物和A、B形成的一种化合物能发生氧化还原反应,说明亚硫酸和双氧水,反应的化学方程式为H2SO3+H2O2=H2SO4+H2O;(4)氯气溶于水生成盐酸和次氯酸,盐酸和碳酸氢钠反应生成氯化钠、水和CO2,则把氯气通入碳酸氢钠溶液中发生反应的总反应的离子方程式为HCO3-+Cl2=Cl-+HClO+CO2。
;晶体中钠离子与氢氧根离子之间形成离子键,氢氧根离子中氢原子与氧原子之间形成共价键;(3)A、B、D三种元素形成的一种化合物和A、B形成的一种化合物能发生氧化还原反应,说明亚硫酸和双氧水,反应的化学方程式为H2SO3+H2O2=H2SO4+H2O;(4)氯气溶于水生成盐酸和次氯酸,盐酸和碳酸氢钠反应生成氯化钠、水和CO2,则把氯气通入碳酸氢钠溶液中发生反应的总反应的离子方程式为HCO3-+Cl2=Cl-+HClO+CO2。


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
【题目】常温下,将 pH=3 的硫酸与 pH=9 的 NaOH 溶液混合,若要得到 pH = 7 的溶液,混合时硫酸与 NaOH 溶液的体积比为( )
A.1: 200 B. 200 : 1 C. 100 : 1 D.1:100
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用二氧化碳生产化工产品,有利于二氧化碳的大量回收,二氧化碳和乙二醇在ZnO或锌盐催化下可合成碳酸乙烯酯。

(1)锌基态原子核外电子排布式为_________________。
(2)锌盐水溶液中Zn2+可与H2O之间形成 [Zn(H2O)6]2+,其中提供空轨道的是______________(填微粒符号)。
(3)碳酸乙烯酯中碳原子杂化轨道类型为________;1mol碳酸乙烯酯中含有的σ键数目为________。
(4)阴离子X-与CO2互为等电子体且X-内含共价键和氢键,则X-的化学式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酰紫草素具有抗菌、抗炎、抗病毒、抗肿瘤等作用,它的结构简式如右图所示,下列有关乙酰紫草素的说法错误的是
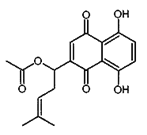
A. 该分子中含有1个手性碳原子
B. 能与FeCl3溶液发生显色反应
C. 1mol 乙酰紫草素最多可与2molBr2反应
D. 1mol乙酰紫草素最多可与2molNaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 在相同条件下PH=5的CH3COOH溶液和PH=5的NH4Cl溶液中,水的电离程度前者比后者大
B. 反应NH3(g)+HCl(g) ![]() NH4Cl(s)能自发进行,则该反应ΔH>0
NH4Cl(s)能自发进行,则该反应ΔH>0
C. 锌与稀硫酸反应时加入少量硫酸铜,反应加快的主要原因是Cu2+水解增大了c(H+)
D. 一定条件下,反应2SO2(g)+O2(g) ![]() 2SO3(g) ΔH<0达到平衡后,升高体系温度,反应重新达到平衡前,有2v正(O2)<v逆(SO3)
2SO3(g) ΔH<0达到平衡后,升高体系温度,反应重新达到平衡前,有2v正(O2)<v逆(SO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活、社会密切相关,下列有关说法中正确的是
A. 地沟油经过加工处理后可用来制生物柴油和肥皂
B. 用填埋法处理未经分类的生活垃圾
C. 大量使用薪柴为燃料,践行低碳生活
D. 含PM2.5(直径小于或等于2.5微米的颗粒物)的空气能产生丁达尔效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将质量相等的铁片和铜片用导线相连浸入500mL硫酸铜溶液中构成如图1的装置:
(以下均假设反应过程中溶液体积不变)。
(1)铁片上的电极反应式为______________,铜片周围溶液会出现___________的现象。
(2)若2 min后测得铁片和铜片之间的质量差为1.2g,计算:导线中流过的电子的物质的量为_________________mo1;
(3)金属的电化学腐蚀的本质是形成了原电池。如下图所示,烧杯中都盛有稀硫酸。


①图2 B中的Sn为________极,Sn极附近溶液的pH(填增大、减小或不变)___________。
②图2 C中被腐蚀的金属是___________。比较A、B、C中纯铁被腐蚀的速率由快到慢的顺序是______。
(4)人们应用原电池原理制作了多种电池,以满足不同的需要。燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:

①氢氧燃料电池的总反应化学方程式是:___________________。
②电池工作一段时间后硫酸溶液的浓度_____________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Sorbicillin (简称化合物X)是生产青霉素时的一个副产品,其结构简式如右下图所示。 下列有关化合物X的说法正确的是

A. 分子中所有碳原子可能处于同一平面
B. 1 mol化合物X可以与2 mol Na2CO3反应
C. 1mol化合物X可以与浓溴水发生取代反应消耗3molBr2
D. 化合物X与H2完全加成,每个产物分子中含有4个手性碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在酸性的无色透明溶液中能够大量共存的是( )
A.NH4+、Fe3+、SO42﹣、Cl﹣
B.Mg2+、Ag+、CO32﹣、Cl﹣
C.K+、NH4+、SO42﹣、Cl﹣
D.K+、Na+、NO3﹣、HCO3﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com