
 .有机物X的键线式为
.有机物X的键线式为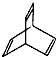
 .
.分析 (1)根据键线式的书写特点,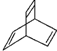 的分子式为C8H8,有机物Y是X的同分异构体,且属于芳香烃,则Y的结构简式:
的分子式为C8H8,有机物Y是X的同分异构体,且属于芳香烃,则Y的结构简式: ,
, 在一定条件能发生聚合反应生成聚苯乙烯;
在一定条件能发生聚合反应生成聚苯乙烯;
(2)X与足量的H2在一定条件下反应可生成环状的饱和烃Z,其结构对称,含2种位置的H.
解答 解:(1)有机物Y是X的同分异构体,且属于芳香烃,则Y的结构简式: ,
, 在一定条件能发生聚合反应生成聚苯乙烯,方程式为:
在一定条件能发生聚合反应生成聚苯乙烯,方程式为: ;
;
故答案为: ;
;
(2)X与足量的H2在一定条件下反应可生成环状的饱和烃Z,其结构对称,含-CH2、-CH上方2种位置的H,则Z的一氯代物有2种;
故答案为:2.
点评 本题考查同分异构现象和同分异构体、加聚反应等,难度较大,注意掌握等效氢原子的判断方法.


 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:解答题

 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
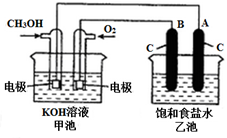 甲醇是一种可再生能源,具有广泛的开发和应用前景.如图是用甲醇燃料电池电解饱和食盐水的装置示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O
甲醇是一种可再生能源,具有广泛的开发和应用前景.如图是用甲醇燃料电池电解饱和食盐水的装置示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O查看答案和解析>>
科目:高中化学 来源: 题型:解答题
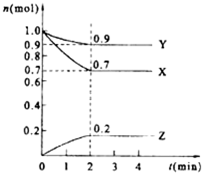 某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示.
某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示. 2Z;
2Z;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 实验目的 | |
| A | 制乙炔时用饱和食盐水代替水 | 加快化学反应速率 |
| B | CH4与SO2混合气体通过盛有溴水的洗气瓶 | 除去中CH4的SO2 |
| C | 甲烷与乙烯的混合气体通过盛有酸性高锰酸钾的洗气瓶 | 除去甲烷中的乙烯 |
| D | 将浓硫酸、乙醇混合加入试管中,加热,然后将导管末端插入酸性KMnO4溶液中,观察现象; | 检验是否有乙烯生成 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 甲烷可用氧化铁作催化剂实现选择性地催化脱硝.
甲烷可用氧化铁作催化剂实现选择性地催化脱硝.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com