
�⼰�仯������������ռ����Ҫ��λ��
(1)�ӵ�ʳ���к��е����(KIO3)����ҵ���Ե�ⷨ�Ʊ�����أ�����豸��ͼ��ʾ���Ƚ�һ�����ĵ����ڹ�������������Һ��������Ӧ��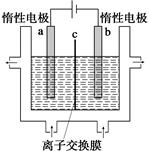
3I2��6KOH=5KI��KIO3��3H2O���ٽ�����Һ���� (����������)������������������Һ��������һ������ʹ�� (������)���ӽ���Ĥ�������������ĵ缫��Ӧʽ�� ��
(2)�⻯�ⲻ�ȶ����ֽⷴӦ���Ȼ�ѧ����ʽ��2HI(g)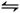 I2(g)+H2(g) ��H="+9.48" kJ��mol��1��֪��S��0
I2(g)+H2(g) ��H="+9.48" kJ��mol��1��֪��S��0
�ٸ÷�Ӧ����( )
A���κ��¶Ⱦ��Է� B���κ��¶Ⱦ����Է� C�������Է� D�������Է�
��һ�������£���Ӧ��һ�����л������ܱ������дﵽƽ�⣬����˵���в���ȷ����( )
A�����£���С�����ƽ�ⳣ������
B�����£���С�����ƽ�ⲻ�ƶ�����ɫ����
C�����ݣ����£�����Ӧ���ʺ�����Ӧ���ʾ�����
D�����ݣ�����������Ͷ��2mol HI���ﵽƽ��ʱ����9.48 kJ ������
��һ���¶��£�ƽ�ⳣ��K=1/4����2L�������У�����4molHI������Ӧ�ﵽƽ�⣬HI��ת���� ��
��1������ �� I-+6OH-��6e-=IO3-+3H2O ��2����C��D ��0.5
���������������1��������֪��ⷨ�Ʊ�����ص�ԭ��Ϊ��KOH���ڵ��������KI��KIO3�Ļ��Һ����Ӧ��ʵ���ǵ����ӷ���ʧ���ӵ�������Ӧ���������ɵ�������ӣ���ϵ��ԭ�����ص���������ʧ���ӵ�������Ӧ������KI��KIO3�Ļ��ҺӦ�������Դ��������������������װ���е�a���������ݵ缫����ʽ��дԭ��ԭ���غ�͵���غ㣬�缫��ӦʽΪ��I-+6OH-��6e-=IO3-+3H2O���ü�����Ӧ����OH����Ӧ�м�����������KOH��Һ���䣬���ӽ���ĤӦ����������ͨ����Ϊ�����ӽ���Ĥ��
��2���ٸ÷�Ӧ��H��0����S��0�����ݷ�Ӧ������оݿ�֪����ʱ��H��T��S<0�����Է����У�ѡC.
��A��ƽ�ⳣ����Ӱ������Ϊ�¶ȣ���ȷ��B���÷�Ӧ������������ϵ����ȣ����£���С�����ƽ�ⲻ�ƶ����������ʵ�Ũ��������ɫ�����ȷ��C�����·�Ӧ���ʼӿ죬��ȷ��D�����淴Ӧ���ص��Dz��ܽ��е��ף�Ͷ��2mol HI���ﵽƽ��ʱ���յ�����С��9.48 kJ������
�� ��ת���ĵ⻯��Ϊx���������η��ó������ʵ�ƽ��Ũ�ȣ�����ƽ�ⳣ������ʽ����⻯���ƽ��Ũ�ȣ�����ת���ʼ��㹫ʽ����ɵá�
���㣺������ԭ�������淴Ӧ���ص㡢�������������ƽ���Ӱ�켰ƽ�����


 �����Ծ���Ԫ���Ծ�ϵ�д�
�����Ծ���Ԫ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
���ô�������Ӧ��SO2ת��ΪSO3�ǹ�ҵ����������Ĺؼ����衣
��֪��SO2��g���� O2��g��
O2��g�� SO3��g�� ��H����98 kJ��mol��1��
SO3��g�� ��H����98 kJ��mol��1��
��1��ij�¶��¸÷�Ӧ��ƽ�ⳣ��K��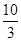 �����ڴ��¶��£���100 L�ĺ����ܱ������У�����3.0 mol SO2(g)��16.0 mol O2(g)��3.0 mol SO3(g)����Ӧ��ʼʱv������ v���棩�����������������������
�����ڴ��¶��£���100 L�ĺ����ܱ������У�����3.0 mol SO2(g)��16.0 mol O2(g)��3.0 mol SO3(g)����Ӧ��ʼʱv������ v���棩�����������������������
��2��һ���¶��£���һ�����������Ϊ2 L���ܱ������г���2.0 mol SO2��1.0 molO2���ﵽƽ��������Ϊ1.6 L����SO2��ƽ��ת����Ϊ ��
��3���ڣ�2���еķ�Ӧ�ﵽƽ��ı�������������ʹSO2(g)ƽ��Ũ�ȱ�ԭ����С���� ������ĸ����
| A�������¶Ⱥ�����������䣬����1.0 mol O2 |
| B�������¶Ⱥ�������ѹǿ���䣬����1.0 mol SO3 |
| C�������¶� |
| D���ƶ�����ѹ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
KI��Һ����������������������Ӧ����������ʵ���¼��
| ʵ���� | �� | �� | �� | �� | �� |
| �¶ȣ��棩 | 30 | 40 | 50 | 60 | 70 |
| ��ɫʱ�䣨s�� | 160 | 80 | 40 | 20 | 10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�������������ʡ����ᡢ����ȵ���Ҫԭ�ϡ�
��1��ʵ����ģ��ϳɰ����ں��º����ܱ������а��ռס��ҡ������ַ�ʽ�ֱ�Ͷ�ϣ���λ��mol /L����ƽ��ʱ��ü�������H2��ת����Ϊ20%��
| | N2 | H2 | NH3 |
| �� | 1 | 3 | 0 |
| �� | 0.5 | 1.5 | 1 |
| �� | 0 | 0 | 4 |
 CO(NH2)2 (l) + H2O (l)���÷�Ӧ��ƽ�ⳣ�����¶ȹ�ϵ���£�
CO(NH2)2 (l) + H2O (l)���÷�Ӧ��ƽ�ⳣ�����¶ȹ�ϵ���£�| T / �� | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
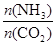 ��x����ͼ�ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ��������x����������ԭ���� ��
��x����ͼ�ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ��������x����������ԭ���� ��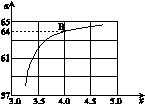
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ӦaA��g��+bB��g�� cC��g������H��0���ڵ��������½��С��ı�������Ӧ�������ڢ����ϵ�и�����Ũ����ʱ��仯����������ͼ��ʾ��
cC��g������H��0���ڵ��������½��С��ı�������Ӧ�������ڢ����ϵ�и�����Ũ����ʱ��仯����������ͼ��ʾ�� 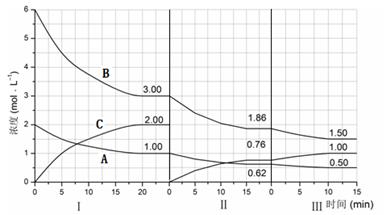
�ش����⣺
��1����Ӧ�Ļ�ѧ����ʽ�У�a��b��cΪ ��
��2��B��ƽ��ת���ʦ�����B����������B����������B���������� ����ֵ�� ��
��3���ɵ�һ��ƽ��ڶ���ƽ�⣬ƽ���ƶ��ķ����� ����ȡ�Ĵ�ʩ�� ��
��4���Ƚϵڢ�η�Ӧ�¶ȣ�T2���͵ڢ�η�Ӧ�¶ȣ�T3���ĸߵͣ�T2 T3 ���<������>��=�������жϵ������� ��
��5���ﵽ������ƽ����������������һ�����ٶ�10min��ﵽ�µ�ƽ�⣬������ͼ�������߱�ʾ��IV����ϵ��B���ʵ�Ũ����ʱ��仯�����ƣ�ע��ֻ�뻭��B��Ũ����ʱ��仯���ߣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��һ�������£����淴ӦA2(g)+B2(g)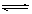 2C(g)��һ���ܱ������дﵽƽ��ʱ,���c(A2)=0��5mol��L-1��c(B2)=0��1mol��L-1��c(C)=1��6mol��L-1����
2C(g)��һ���ܱ������дﵽƽ��ʱ,���c(A2)=0��5mol��L-1��c(B2)=0��1mol��L-1��c(C)=1��6mol��L-1����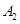 ��
��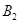 ��C����ʼŨ�ȷֱ�Ϊa mol��L-1��b mol��L-1��g mol��L-1��ȷ����
��C����ʼŨ�ȷֱ�Ϊa mol��L-1��b mol��L-1��g mol��L-1��ȷ����
(l)a��gӦ����Ĺ�ϵʽΪ_____________��
(2)����Ӧ������Ӧ����ʼ���У���g=_________,a�����ֵΪ__________��
(3)����Ӧ���淴Ӧ����ʼ���У���b=_________��a����СֵΪ_________��
(4)b��ȡֵ��ΧΪ___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�ϳɰ���ҵ�Թ��ú���ᷢչ������Ҫ�����塣��ԭ��Ϊ��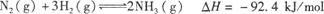 ���ݴ˻ش��������⣺
���ݴ˻ش��������⣺
��1���ٸ÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK= ��
�ڸ����¶ȶԻ�ѧƽ���Ӱ����ɿ�֪�����ڸ÷�Ӧ���¶�Խ�ߣ���ƽ�ⳣ����ֵԽ ��
��2��ij�¶��£�����10 mol N2��30 mol H2�������Ϊ10 L���ܱ������ڣ���Ӧ�ﵽƽ��״̬ʱ����û�������а����������Ϊ20��������¶��·�Ӧ��K= (���÷�����ʾ)��
��˵���÷�Ӧ�ﵽ��ѧƽ��״̬���� (����ĸ)��
a�������ڵ��ܶȱ��ֲ��� b��������ѹǿ���ֲ���
c��v��(N2)=2v��(NH3) d�����������c(NH3)����
��3�����ںϳɰ���Ӧ���ԣ������й�ͼ��һ����ȷ����(ѡ�����) ��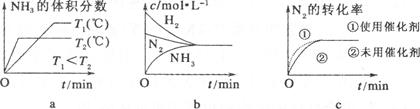
��4����ͬ�¶��£��к����ܱ�����A�ͺ�ѹ�ܱ�����B���������о�����1 mol N2��3 mol H2����ʱ�������������ȡ���һ�������·�Ӧ�ﵽƽ��״̬��A��NH3���������Ϊa���ų�����Q1kJ��B��NH3���������Ϊb���ų�����Q2kJ����a b(���������������=������ͬ)��Q1 Q2��Q1 92��4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(14��)ij��ѧ��Ӧ2A(g) B(g)+D(g)�����ֲ�ͬ�����½��У�B��D��ʼŨ��Ϊ�㣬��Ӧ��A��Ũ��(mol/L)�淴Ӧʱ��(min)�ı仯����������������ݣ����������գ�
B(g)+D(g)�����ֲ�ͬ�����½��У�B��D��ʼŨ��Ϊ�㣬��Ӧ��A��Ũ��(mol/L)�淴Ӧʱ��(min)�ı仯����������������ݣ����������գ�
| ʵ�� ��� | �¶�/�� | ʱ��/min | ||||||
| 0 | 10 | 20 | 30 | 40 | 50 | 60 | ||
| 1 | 800�� | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800�� | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800�� | c 3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820�� | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(14��)��ҵ���������Ҫ��Ӧ��4NH3(g)+5O2(g)  4NO(g)+6H2O(g)��H=-akJ/mol(a��0)
4NO(g)+6H2O(g)��H=-akJ/mol(a��0)
(1)�����4molNH3��5molO2���������У��ﵽƽ��ʱ���ų�����0.8akJ����Ӧʱת�Ƶĵ�����Ϊ
mol
(2)�������������䣬���й�ϵͼ�д������ ��ѡ����ţ�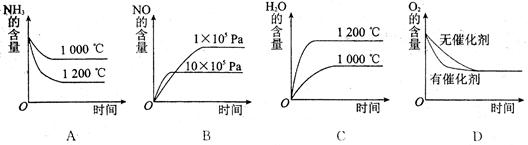
(3)t��ʱ�����ݻ��̶����ܱ������з���������Ӧ�������ڸ����ʵ�Ũ�����±�
| Ũ��(mol/L) ʱ��(min) | c(NH3) | c(O2) | c(NO) | c(H2O) |
| �� ʼ | 4.0 | 5.5 | 0 | 0 |
| ��2min | 3.2 | x | 0.8 | 1.2 |
| ��4min | 2.0 | 3.0 | 2.0 | 3.0 |
| ��6min | 2.0 | 3.0 | 2.0 | 3.0 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com