
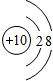 ,故答案为:
,故答案为: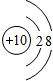 ;
;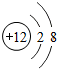 ,故答案为:
,故答案为: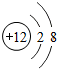 ;
; ,故答案为:
,故答案为: ;
; 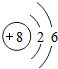 ,
,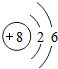 .
.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
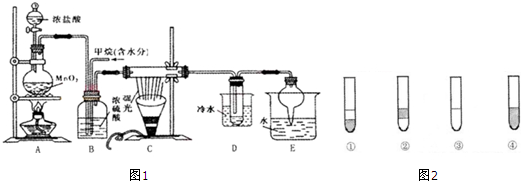
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示为NaCl晶体的晶胞示意图.
如图所示为NaCl晶体的晶胞示意图. 查看答案和解析>>
科目:高中化学 来源: 题型:
12 6 |
13 6 |


查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.2mol/L 盐酸 15mL |
| B、5mol/L 硝酸 12mL |
| C、0.15mol/L 硫酸 8mL |
| D、18mol/L 硫酸 15mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 药品 | 选用试剂 | 操作方法 |
| A | 乙烷(乙炔) | 酸性高锰酸钾溶液 | 洗气 |
| B | 乙烷(乙烯) | 氢气 | 高温、高压、催化剂 |
| C | 乙酸乙酯(乙酸) | 浓的氢氧化钠溶液 | 分液 |
| D | 硝基苯(硝酸) | 氢氧化钠溶液 | 分液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、沸点:NH3>AsH3>PH3 |
| B、熔点:MgCl2>SiO2>CO2 |
| C、酸性:H3PO4>H2SO4>HClO4 |
| D、碱性:LiOH>NaOH>KOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com