

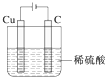
| 序号 | 反应 | 平衡常数 |
| 1 | Au+6HNO3(浓)═Au(NO3)3+3NO2↑+3H2O | <<1 |
| 2 | Au3++4Cl-═AuCl4- | K |
| 10-14 |
| 10-8 |
| 2.2×10-20 |
| (1×10-6)2 |
 ,
, .
.


科目:高中化学 来源: 题型:
| A、保持容器体积不变,向其中充入1mol H2,反应速率加快 |
| B、保持压强不变,向其中充入N2,气体颜色不变 |
| C、保持体积不变,充入1 mol I2,平衡正向移动,气体颜色变浅 |
| D、升高温度,逆反应速率增大,正反应速率减小,平衡逆向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ca2++2OH-=Ca(OH)2↓ CaCO3+2NaOH=Ca(OH)2↓+Na2CO3 |
| B、Ba2++SO42-=BaSO4↓ Ba(OH)2+H2SO4=BaSO4↓+2H2O |
| C、Ag++Cl-=AgCl↓ AgNO3+NaCl=AgCl↓+NaNO3 |
| D、Fe3++3OH-=Fe(OH)3↓ FeCl3+3NH3?H2O=Fe(OH)3↓+3NH4Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
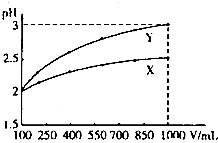
| A、X为弱酸,VX<VY |
| B、Y为强酸,VX>VY |
| C、X为强酸,VX>VY |
| D、Y为弱酸,VX>VY |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 碳及其化合物是一类种类繁多的大家族.
碳及其化合物是一类种类繁多的大家族.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ca2+、Mg2+的总含量 |
| B、Ca2+的含量 |
| C、Mg2+的含量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com